 2007年初中毕业班综合练习卷
2007年初中毕业班综合练习卷
化 学
(考试时间:70分钟; 满分:60分)
| 题号 | 一 | 二 | 三 | 四 | 总分 |
| 得分 |
可能用到的相对原子质量:H―1 C―12 O―16 Na―23 Fe―56 Ba―137
一、选择题(每小题2分,共20分。每小题只有一个选项符合题意,请将该选项的字母填在相应的括号内。)
1.在一些课外读物中常见下列词汇,其中不能用来描述相关物质真实颜色的是 ( )
A. 黑色粉末 B. 绿色食品 C. 蓝色晶体 D. 银白色金属
2.具有可燃性和还原性的固体单质是 ( )
A. CO B. CO2 C. H2 D. C
3.m g硫在足量的氧气中完全燃烧,生成二氧化硫的质量 ( )
A. 小于m g B. 大于m g C. 等于m g D. 无法判断
4 . 下列实验基本操作,错误的是 ( )
A. 往酒精灯里添加酒精要使用漏斗
B. 用滴管滴加液体时,不要将滴管伸入试管内
C. 取用砝码要用镊子,添加顺序一般由大到小
D. 实验室里剩余的药品要放回原试剂瓶
5.农作物生长需要氮、磷、钾等营养元素。下列化肥中,属于复合肥料的是 ( )
A. 尿素[CO(NH2)2] B. K2SO4 C. NH4H2PO4 D. NH4NO3
6.用100 t含氧化铁80%的赤铁矿石,可炼出铁的质量 ( )
A. 14 t B. 20 t C. 56 t D. 80 t
7.通过下列类型的反应:①化合反应;②分解反应 ;③置换反应; ④复分解反应,其中能产生氢气的是
( )
A . ①④ B. ①②③ C. ②③ D. ①②③④
8.在通常状况下,鉴别氢气和氧气不可以使用的方法是 ( )
A. 分别观察颜色、状态,闻气味 B. 分别吹肥皂泡
C. 分别将燃着的木条伸入气体中 D. 分别通过灼热的氧化铜
9.下列四种物质中,其中有一种能和其他三种物质发生反应,该物质是 ( )
A. CO2 B. CuSO4溶液 C. 稀盐酸 D. 氢氧化钠溶液
10. 除去下列物质中的杂质(括号内),使用“――”后的试剂,其中不正确的是 ( )
A. O2(SO2)―― NaOH溶液 B. C ( CuO) ―― 稀硫酸
C. NaCl ( Na2SO4) ―― 硝酸钡溶液 D. CuO ( KNO3) ―― 水
![]() 二、填空题(本题共25分)
二、填空题(本题共25分)
11. 某元素M的原子结构示意图为则m= ,M元素为 元素(选填“金属”或“非金属”)。
12. 某同学做了一个家庭小实验:在一个烧杯底部放入一支短蜡烛,并铺一层纯碱,点燃蜡烛后,沿烧杯壁倒入一些醋(主要成分是醋酸),可观察到的实验现象是
 和
,由此可推知二氧化碳的用途之一是
。
和
,由此可推知二氧化碳的用途之一是
。
13. 强光照射氢气与氯气(Cl2)的混合气体时会发生爆炸,其反应的微观过程可用右图表示:
(1)写出该反应的化学方程式:
。
(2)分析该微观过程模拟图,你能总结出的一个结论是 。
 14.“水”在化学世界中举足轻重。
14.“水”在化学世界中举足轻重。
(1)水的化学式为H2O,关于“H2O”的含义,四位同学表达了如下图所示的四种说法,请你将说法③、④省略的部分填写在横线上。
说法③:表示水由
;
说法④:表示每个水分子由
。
(2)与水有关的化学反应很多很多,请你任举一个,用化学方程式表示:
。
15. 生活中的化学可以说无处不在。请你仿照示例,将有关问题补充完整。
| 生活中的化学问题 | 解释相应问题的化学方程式 | |
| 示 例 | 用石灰浆抹墙,久之变硬 | Ca(OH)2 + CO2 = CaCO3 +H2O |
| (1) | ||
| (2) |
16. A、B、C三个烧杯中装有等质量的水,在相同
 温度下,向A、B、C烧杯中分别加入25 g、15 g、5 g
温度下,向A、B、C烧杯中分别加入25 g、15 g、5 g
KNO3固体,充分溶解后、静置,现象如右图所示,回答下列问题:
(1) 中的溶液一定是饱和溶液,你的判断依据是 。
(2) 中的溶液一定是不饱和溶液。
(3)欲将A烧杯中未溶解的KNO3固体继续溶解,可以采取的方法是 或
。
17. 高锰酸钾是一种暗紫色的固体,可溶于水。溶于水时电离成为K+ 和MnO―4。加热干燥的高锰酸钾,可以制得极纯的氧气(4 KMnO4![]() 4
MnO2 + 2 K2O + 3 O2↑)。回答下列问题:
4
MnO2 + 2 K2O + 3 O2↑)。回答下列问题:
(1)上述变化所属的基本反应类型是 。
(2)KMnO4中,锰元素的化合价为 。
(3)高锰酸钾的物理性质有(任写一点) 。
(4)上述反应的生成物中,属于氧化物的有 。
(5)将紫色的高锰酸钾溶液滴入水中,发现它在水中扩散开来,这说明钾离子和高锰酸根离子 。
(6)t℃时,KMnO4的溶解度为6 g。则t℃时,要将6 g KMnO4固体完全溶解,最少需要水 g。
三、实验题(本题共10分)。
18. 人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”。
(1)按上述顺序写出其元素符号: 。
(2)从“五金”中任选两种金属,设计一个简单实验判断二者金属活动性的强弱。
| 实验步骤 | 实验现象 | 实验结论 |
19.(1)左下图是小李通过实验检验锌与盐酸反应产生的氢气中含有的杂质。
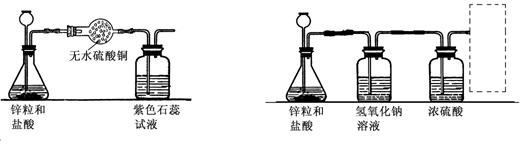
①实验中观察到无水硫酸铜变蓝色,说明制取的氢气中含有 ;又观察到紫色石蕊试液变红色,说明制得的氢气中含有 。
②图中的石蕊试液也可换成 溶液,此时观察到的现象是
。
(2)已知浓硫酸具有很强的吸水性,是一种常用的干燥剂。右上图是小李设计的制取干燥、纯净氢气的装置。
① 其中氢氧化钠溶液的作用是 。
② 虚线框内连接的最佳收集装置是( )。
A. 向上排空气集气装置 B. 用干瘪的气囊作为集气装置
C. 向下排空气集气装置 D. 排水集气装置
四、计算题(本题共5分)
20. 现有氢氧化钠和碳酸钠的混合物20 g,将它们溶于水制成溶液,然后慢慢滴加溶质质量分数为10%的氢氧化钡溶液至沉淀不再产生为止,沉淀经过滤、洗涤、干燥后,称得质量为19.7 g。有关反应的化学方程式为 Na2CO3 + Ba(OH)2 = BaCO3↓+2 NaOH。计算:
(1)滴加氢氧化钡溶液的质量;
(2)20 g混合物中含有氢氧化钠的质量。
化学参考答案及评分标准
说明:1.本答案供评卷时使用,考生若写出其它正确答案,可参照评分标准给分。
2.化学专用名词中出现错别字、元素符号书写不规范的都要参照评分标准扣分。
3.书写化学方程式,写对化学式给0.5分,全对给1分。
一、每小题2分,共20分。
| 题 号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答 案 | B | D | B | D | C | C | C | A | D | C |
二、本题共25分,每一个空格均为1分。
11. 12 金属
12. 有气泡产生 片刻后蜡烛熄灭 灭火剂
13. (1) H2
+ Cl2![]() 2
HCl
2
HCl
(2)例如:在化学反应前后,元素种类不变
14.(1)氢元素和氧元素组成 2个氢原子和1个氧原子构成
(2)例如:CaO + H2O = Ca(OH)2
| (1) | 用盐酸除去铁锈 | Fe2O3 + 6 HCl = 2 FeCl3 + 3 H2O |
| (2) | 燃烧天然气 | CH4 + 2O2 |
15.例如:
16. (1) A 烧杯中残留有KNO3固体
(2)C
(3)升高温度 加入水
17.(1)分解反应
(2)+7
(3)例如:可溶于水
(4)MnO2、K2O
(5)在不停地运动
(6)100
三、本题共10分,每一个空格均为1分。
18.(1)Au Ag Cu Fe Sn
(2)
| 往一试管内放入几支洁净的铁钉,再加入适量的硫酸铜溶液,静置一会儿 | 铁钉表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色 | 铁的金属活动性比铜强 |
19.(1)①水蒸气 氯化氢
②AgNO3溶液 产生白色沉淀
(2)①除去氢气中的少量氯化氢气体
②B
四、本题共5分。
20.解:设滴入溶液所含Ba(OH)2的质量为x,20 g混合物中含有Na2CO3的质量为y。
Na2CO3+Ba(OH)2=BaCO3↓+2NaOH
106 171 197
y x 19.7 g
![]()
![]()
x = 17.1g (1分)
Ba(OH)2溶液的质量=![]()
=171 g (1分)
![]()
![]()
y = 10.6 g (1分)
20 g混合物中含氢氧化钠的质量为
20 g -10.6 g
= 9.4 g (1分)
答:(略)。 (计算格式1分)