化学计算
可能用到的相对原子质量:P 31 O 16 S 32 Fe 56 Zn 65 Cu 64 Ag 108 N 14
Na 23 Ba 137 Cl 35.5 Mg 24 Ca 40 Al 27 K 39
一、选择题(共计30分,每题只有一个正确答案)
1、金属M的相对原子质量为70,它在化合物中只有一种化合价,已知它的磷酸盐的相对分子质量为165,它的硫酸盐的相对分子质量为( )
A .166 B. 236 C .428 D. 不知道化学式,无法计算
2、含相等质量氧元素的CO2和SO2两种气体,碳元素与硫元素的质量比为 ( )
A. 1∶1 B.3∶4 C. 11∶16 D. 3∶8
3、在天平两端的托盘上,各放一个盛有20g 19.6%的稀硫酸的烧杯,并使天平平衡,然后在其中一个烧杯中加入10g铁,另一个烧杯中放入锌,要使反应后天平仍保持平衡,放入锌的质量应是 ( )
A. 5.6g B .6.5g C .10g D. 13g
4、燃烧某有机物A2.3g,生成4.4g CO2和2.7g H2O,则组成有机物A的元素 ( )
A.只含碳、氢两种元素 B.一定含有碳、氢、氧三种元素
C.一定含有碳、氢两种元素,可能含有氧元素 D.不能确定
5、2004年以来,我国一些地方相继发生因“毒鼠强”(化学式为C4H8N4S2O4)中毒造成人员伤亡的事件,“毒鼠强”是一种剧毒物。下列关于它的组成叙述正确的是( )
A.它的一个分子由4个碳原子、4个氢分子、2个氮分子和2个二氧化硫分子构成
B.它的分子由4个碳原子、8个氢原子、2个氮原子、2个硫原子、4个氧原子构成
C.它的相对原子质量为240
D.它的组成元素碳、氢、氮、硫、氧的质量比为6∶1∶7∶4∶8
6、某CO和CO2的混合气体中,含氧64%,将该混合气体10g通过足量灼热氧化铜,使其充分反应,再将反应后的气体通入到足量的石灰水中,所得沉淀最接近的数据是 ( )
A .10g B. 20g C .30g D. 22.7g
7、在化学反应![]() 中,X表示某物质的化学式,则X可能是 ( )
中,X表示某物质的化学式,则X可能是 ( )
A .CH4 B. CH4O C .H2S D .C2H6O
8、在一定温度下,把ag物质加入bg水中,则所得溶液的质量为( )
A. 小于(a+b)g B.等于(a+b)g
C. 大于(a+b)g D.不大于(a+b)g
9、已知60℃时硝酸钾溶解度为110g,则60℃时50g硝酸钾饱和溶液中溶质、溶剂、溶液的质量的最简比为 ( )
A. 10∶11∶21 B. 11∶10∶21 C .21∶10∶11 D. 110∶100∶210
10、某同学欲配制6%的食盐水80g,在称量食盐中,他把食盐和砝码的位置放颠倒了(1g以下用游码),其他各步操作均正确,那么他实际上所配制的食盐水的质量分数为 ( )
A. 4.1% B. 6.0% C. 14.3% D. 3.2%
11、在常温下,向100g5%的氯化钠溶液中加入5g氯化钾粉末,完全溶解后,氯化钠的质量分数将 ( )
A.增大 B.减小 C.不变 D.无法判断
12、某氢氧化钠溶液中Na+和水分子个数比为1∶20,则该溶液中溶质的质量分数为 ( )
A. 6% B. 4.8% C .10% D. 69%
13、在一定质量的硫酸溶液中加入氯化钡溶液直到反应完全,产生沉淀的质量与原硫酸溶液的质量相等,则原硫酸溶液的质量分数为( )
A. 42% B .36% C. 30% D.24%
 14、某金属氧化物跟足量的盐酸反应,生成氯化物和水的分子个数之比为2∶3,该金属元素的化合价为 ( )
14、某金属氧化物跟足量的盐酸反应,生成氯化物和水的分子个数之比为2∶3,该金属元素的化合价为 ( )
A .+1 B. +2 C. +3 D. +4
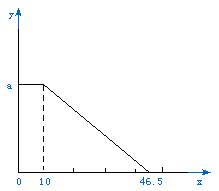
15、某固体物质有NaOH和MgCl2组成,
取一定量的该混合物溶于水有沉淀生成。
在所得悬浊液中逐滴加入10%盐酸,发现
沉淀的质量(y)与加入盐酸的质量(x)
有如右图所示的关系,则沉淀物质A等于
( )
A. 0.759g B. 2.9g C. 3.69g D .4.49g
二、填空题(共计22分,4~8小题每空2分)
1、钙是人体必需的元素,它是构成骨骼、牙齿的重要成分,人们可以从牛奶、蔬菜等食物中得到所需的钙元素,如果从食物中摄取的钙元素不足,还可以用含葡萄糖酸钙、碳酸钙等含钙的药物来补充,俗称“补钙”。
⑴葡萄糖酸钙[化学式是Ca(C6H11O7)2]的相对分子质量是 ,其中钙、碳、氢、氧四种元素的质量比是 。
⑵某人每天需用含1g碳酸钙的药物“补钙”,则他每天补充的钙元素是 g。
2、1999年,比利时的“二恶英污染鸡”事件轰动全球。焚烧生活垃圾也会产生二恶英。二恶英是含碳、氢、氧、氯元素的有机物,其中毒性较大的一种化学式为C12H4O2Cl4,此物质中碳、氢元素的原子个数比为 ,氧、氯元素的质量比为 。
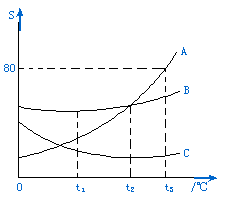 3、右图为A、B、C三种物质的溶解
3、右图为A、B、C三种物质的溶解
度随温度变化的曲线图,S(溶解
度)单位为g,t(温度)单位为℃。
⑴在t3℃时,三种物质的溶解度由小
到大的排列顺序是 。
在 ℃时,A、B两物质的溶解度相等。
⑵随着温度升高,A、B、C三种物质的饱
和溶液中有溶质从溶液中析出的物质
是 。
⑶要将A物质从它的饱和溶液中析出,应采用的方法是 ;如果A物质中混有少量B物质,要将A从混合物中分离出来的方法是 。(填“蒸发结晶”“冷却结晶”)
4、在天平两端的烧杯中,分别盛有等质量的等溶质质量分数的硫酸,调平后,向两烧杯中分别加入等质量的镁和铜铝合金,反应停止后(两边酸都过量),天平仍保持平衡,则铜铝合金中,铜与铝的质量比为 。
5、反应A+2B=C+D中,生成物C和D的质量比为1∶3,若反应物A与B在反应中共消耗2.4g,则生成物C的质量为 g。
6、10g氢气和氧气的混合气体,在一密闭容器内点火爆炸后,冷却至室温,发现仍有1g剩余气体,则原混合气体中氢气最多可能是 g。
7、20g硫酸溶液跟32.33g氯化钡溶液恰好完全反应,滤出反应溶液里的沉淀,得到50g溶液,则所得溶液中溶质的质量分数为 。
8、在KCl和MgCl2的混合物中,钾与镁的原子个数比为2∶1,则混合物中钾元素与镁元素的质量比为 ,KCl与MgCl2的质量比为 。
三、计算题(共计10分,每小题5分)
1、为了对氯化钾样品(含少量KNO3)进行分组分析,甲、乙、丙三位同学分别进行实验,他们的实验数据如下表,请仔细观察和分析数据,回答下列问题:
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量/g | 20 | 10 | 10 |
| 加入AgNO3溶液的质量/g | 100 | 100 | 150 |
| 反应后所得的沉淀质量/g | 14.35 | 14.35 | 14.35 |
⑴三位同学中,哪一位所用的KCl和AgNO3刚好互相完全反应(填写编号) 。
⑵三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),其中有一位同学所得的滤液中只含有一种溶质,此溶液的溶质质量分数是多少?(小数点后保留两位数字)
|
(1)阿莫西林相对分子质量:
(2)如果一个体重25公斤的
儿童患病需要服用阿莫西林,每天要
服多少粒?(按最高剂量计算)
参考答案
一、选择题(每题2分,共30分)
1―5 CDCBC
6―10 CBDBA
11―15 BCACB
二、填空题(1―3题每空1分,4―8题每空2分,共22分)
1、⑴ 430 20∶72∶11∶112 ⑵ 0.4
2、3∶1 16∶71
3、⑴ SC<SB<SA t2 ⑵ C ⑶ 冷却结晶 冷却结晶
4、1∶3
5、0.6
6、2
7、1.46%
8、39∶12 149∶95
三、计算题(每题5分,共10分)
1、⑴ 乙(1分) ⑵ 10.56%(4分)
2、⑴ 425(2分) ⑵ 10(3分)