��ʮһ��Ԫ�λ��ʻ���������
һ��ѡ���⣺
1������ʳ�Ρ�ʳ�ס�����ȼ�ͥ�����������ʣ�������ɵ�ʵ���Ƿ������� ��������A����ˮ�� B������ʳ�κʹ��� C��������Һ�Ƿ�ʼ��� D��֤����۷���ʱ��������
2���������ʵ����ơ���������ѧʽ��һ�µ��ǡ����������������������������� ��������A�������ơ�ʯ��ʯ��CaO�������� B���������ơ��ռCa��OH��2
C��̼���ơ��մ�Na2CO3�������� D��̼��ơ���ʯ�ҡ�Ca��OH��2
3�������и��������ʻ�ϣ������������һ�����ʾ���������ַ�Ӧ����ˣ���ֽ��ֻ��һ�ֲ�������ǡ����������������������������������������������������� ��������
A��Fe��Ag��CuSO4���������������������� B��Na2CO3��Һ��ʯ��ˮ������
C��MgSO4��Һ��Ba��NO3��2��Һ�����ᡡ��D��BaCl2��Һ��Ag NO3��Һ��ϡ����
4�����д�ԭ����ȡ�ϴ������ղ����ʵ������У���������ȷ�������Ͽ��С������Ϻ������ǡ��� ��������������������������������������������������������������������
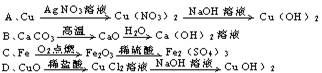 ��
��
5����嫵ĺ�������������ˮ��������̲��ŷḻ�Ļ�ѧ��Դ�����Ȼ��ơ��Ȼ�þ���廯þ�ȴ����Ļ��������������Ϣ�ж�����˵���д�����ǡ����������� ��������
�� A������˵��ˮ�к��д������Σ����������ָʳ��
�� B�������ĺ�ˮ�еμ�Ag NO3��Һһ���������ɫ����
�� C�������ĺ�ˮ�еμӴ�����Һһ���������ɫ����
�� D��������ĵķ������ɰѺ�ˮ�䵭ˮ
6�����л�ѧ����ʽ������������д��ȷ���ǡ������������������������������� ��������
�� A������ϡ���ᷴӦ��2Fe+6HCl=2FeCl3+3H2��
�� B����ϡ����ϴȥ�������Թܱ��ϵ�ͭ��Cu+H2SO4=CuSO4+H2��
�� C��ʵ���Ҽ���CO2�ķ�����CO2+Ca��OH��2=CaCO3��+H2O
�� D����ȥNaOH��������Na2 CO3��Na2 CO3+2HCl=2NaCl+H2O+CO2��
7��ij�����ų��ķ�ˮʹ��ɫʯ���죬��ˮ�к��϶��CuCl2�������塢�����ũ���ﶼ�к����ӻ��ս���ͭ�ͻ��������ĽǶȿ��ǣ��к�ʵ�ʵķ����ǡ����������� ��������
�� A��Na2 SO4��MgCl2���� B��NaCl��HCl���� C��NaOH��Fe����D����ʯ�Һ�����
8���������ᡢ�Ȼ��ơ��Ȼ���������������ƿ��ɫ��Һ����һ���Լ�һ���Ծ��ܰ������������Լ��ǡ����������������������������������������������������� ��������A�����ᱵ�������� ��B��̼�ᱵ�������� C����������������D��̼���
9�����и��������а��ᡢ��Ρ����ʵ�˳�����е��ǡ��������������������� ��������
A��H2SO4��Na2O��MgCl2��C�������� B��NaHCO3��Ba��OH��2��NaCl��Zn
C��HNO3��KOH��Na2CO3��O2��������C��HCl��KOH��Na2CO3��SiO2
10�����з������ܴﵽĿ�ĵ��ǡ����������������������������������������� ��������
A���ü��ȵķ�������Na2CO3�л����NaOH
B������������ɳ���NaCl��Һ�л����NaOH
C�������������ۿɳ���FeSO4��Һ�л��������H2SO4
D����ϡ�����ϴˮ���е�ˮ��
11��һЩҽ�ú��ػ������ˮ��Һ�ܸ���������Һ��Ӧ�����ɲ�����ϡ����İ�ɫ�������Ʋ�ú��ػ������ǡ��������������������������������������������������� ��������
A��KNO3������ B��K2CO3������C��KCl������D��KOH
12���������ֳ�������θ��ҩ��ǩ����ͼ��ʾ��ҩƷ�����������ʾ����к�θ��������ᡣ���й�������ҩƬ�к�θ��������Ƚϣ���ȷ���ǡ����������������������� ��������

A����=��=�ۡ��� B���٩��ک��ۡ����� C���۩��ک��١�����D���ک��۩���
13���±���С��ͬѧ�ö��ַ������������ʵ������������ȫ��ȷ���ǡ������� ��������
| ��������� | �����Լ��� | ||
| ����һ | ������ | ||
| A | ľ̿�ۺ�����ͭ | �۲���ɫ | ͨCO������ |
| B | NaCl ��Һ��Na2CO3��Һ | ϡ���� | Zn |
| C | NaHCO3��K2 SO4 | ��Ca��OH��2��ĥ������ζ | ϡ���� |
| D | ϡHCl��KCl��Һ | Fe2O3 | ��ɫ��̪ |
14�����������ǩ����ƿ�Լ�����֪���Ƿֱ��������������ʵ���Һ����Ba��OH��2��
��Na2 SO4����FeCl3����KCl����Ba�� NO3��2�������������Լ���������ķ�����������������ʡ���������������ʵ��Ⱥ�˳������ǡ��������������������� ��������
A���ۢ٢ڢݢܡ��� B���ݢ٢ۢڢܡ��� C���ܢۢ٢ڢݡ�����D���ݢ٢ܢۢ�
��������⣺
15����������ϡ���ᵹ��ʢ���������ۺ�����Cu��OH��2���Թ����ȣ����ú���ˣ���ֽ�����µ�������__________����Һ�����������_________��
16��A��B��C��D������Һ�����Ƿֱ���HCl��Na2 CO3��Ba��OH��2��Na2 SO4�������������ʱ������������A+B�������壻A+C���ɳ�����C+D���ɳ�����B+D����Ӧ����A��B��C��D�ֱ��ǣ�A_________��B________��C________��D_________��
17�����м��ֻ��ʣ�������K2SO4��NH4HCO3��NH4NO3��Ca3��PO4��2������ͨ���۲���Լ����������___________��ͨ������ζ���Լ����������__________��ͨ������ˮ��Һ�м���Ba��OH��2��Һ���Լ����������__________________��
18������һϴ���ļ��������ط��벣�����С�
�� �ڽ�խ�������ֽ������뱭�ף�����Ϊ��β��ܽ��������뱭�ף����������
������____________________________________________________________________��
�� �����е���ʳ�ף�ʹҺ����ڼ���Լ1cm��������ֹԼ����Ӻ��DZ���ۼ��˺ܶ�С���ݣ������������������е�������_______��
�� ��5min���Զ��ϸ�������ˮ������³�����˲��Ϸ������Դ�����ͬѧ�ֱ��������½��ͣ����нϿ�ѧ����______���ף���������ۼ��ڼ������棬�������ſ�Һ�����������������ң����Ƿ�����Ӧʹ�����������ᡣ�������ᷢ����Ӧʹ��Һ�ܶȼ�С��
 19��ijʵ��������һʢ��ɫ��Һ���Լ�ƿ�����ǩ������ͼ11-2��ʾ��������Ը��Լ��������벢���ʵ����֤��
19��ijʵ��������һʢ��ɫ��Һ���Լ�ƿ�����ǩ������ͼ11-2��ʾ��������Ը��Լ��������벢���ʵ����֤��
�� ���룬���Լ�������____________��Һ��__________��Һ��
�� ������һ�ֲ�����ʵ�������֤��
| ʵ�鲽�� | ʵ������ | ���� |
20��С��ͬѧ�ڲμ�ѧУ��չ���ۺ�ʵ����У�����ѧУ����һ�һ�������ˮ�����������ͬѧ�ڿ���������ռ������������ϣ��Ÿû������ŷŵ���ˮ��Ҫ�ɷ������ᡣ��ȡδ����������ˮˮ�����������PH����Ӧ��_______�ⶨ������IJ�����______________
________________________________________________________________________��
��Ϊ��֤��Һ���Ƿ����ᣬС��ͬѧ��������ʵ�飬һ���Ǽ���H+������ѡ�õ��Լ���
____________����һ���Ǽ���Cl��������ѡ�õ��Լ���__________________��
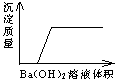 21����һ���������������ᡢ̼���ơ����ᡢ�Ȼ�李�����ͭ���������е�һ�ֻ�����ɣ������Һ�еμ�Ba��OH��2��Һ���������������������Ba��OH��2�����ϵ��ͼ��ʾ���ݴ˻ش𣺡���������������������������������
21����һ���������������ᡢ̼���ơ����ᡢ�Ȼ�李�����ͭ���������е�һ�ֻ�����ɣ������Һ�еμ�Ba��OH��2��Һ���������������������Ba��OH��2�����ϵ��ͼ��ʾ���ݴ˻ش𣺡���������������������������������
�� �û����Һ��һ�����е�������________________��һ
�����Ậ�е�������__________________�����ܺ��е���
����______________���ơ� ����Ϊ���������ʵ������ǣ�
__________________________________________________
___________________����������ȷ�����ܺ��е������Ƿ���ڻ��ڣ�_____
________________________________________________________________________��
22�������̽��ҪҪ�õ����ѧ֪ʶ�����±��г������������Ħ���������ڱ�����д����Ħ�����������������ָ�ᡢ��Ρ������
| ��ͯ���� | �������� | ������ | |
| ��Ħ���� | �������� | ̼��� | ������ |
| ������� |
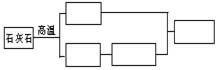 �� ��������Ʋ⣬����Ħ�������ܽ�����________���������е�Ħ����̼��ƿ���ʯ��ʯ���Ʊ����������һ���Ʊ�̼��Ƶ�ʵ�鷽����
�� ��������Ʋ⣬����Ħ�������ܽ�����________���������е�Ħ����̼��ƿ���ʯ��ʯ���Ʊ����������һ���Ʊ�̼��Ƶ�ʵ�鷽����
�١��� ������Ʊ����̵�����ͼ���ڷ�����������
�Ļ�ѧʽ��
�� д���йصĻ�ѧ����ʽ��__________________��
______________________��_______________________��
�� ���۸�ʵ�鷽�����ŵ��ǣ�____________________________________________________��
�� �����������Ƿ���̼���ε�ʵ�鷽����______________________________________
__________________________________________________________________________��
�� ijѧ��Ϊ�˲ⶨһ����̼���ΪĦ������������̼��Ƶĺ��������ձ���ȡ�����������100��0g�����ձ�������ϡ����������������ų�������ȥ����200��0g����Ӧ��ϺƵ��ձ������ʵ�����Ϊ278��0g�������֪����������̼��Ƶ���������Ϊ
________��
23��Ϊ֤�����ڱ�¶�ڿ����е�NaOH��Һ�Ѿ����ֱ��ʣ���ֱ�ѡ�����ֲ�ͬ���������Լ��������ʵ�鷽������ƣ�����дʵ�鱨�档
| ʵ�鷽�� | ����һ | �������ѡ���Լ���ʵ������ |
| ����һ | ȡ��2ml���Թ��� | |
| ������ | ȡ��2ml���Թ��� | |
| ������ | ȡ��2ml���Թ��� |
24����һ�����ŷŵķ�ˮ����AgNO3��Fe��NO3��3��Ca��NO3��2��Ϊ������ˮ����ֹ����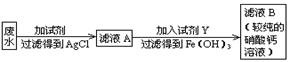 ��Ⱦ�����Ϊ����������������̣�
��Ⱦ�����Ϊ����������������̣�
�� ��ش𣺢�XӦѡ��_____________���� ��YӦѡ��_____________������д���õ��õ����������Ļ�ѧ����ʽ��_____________________________________��
25��ij��������ȡ����ͭ����������;������ͭ��ϡ���ᷴӦ����ѧ����ʽΪ��
3Cu+8HNO3��ϡ��==3Cu��NO3��2+2NO��+4H2O���ɵ�һ�������ڿ��������ױ������ɶ�����������ͭ��Ũ���ᷴӦ��������ͭ��ͬʱ�����ɶ���������ˮ����Ӧ�Ļ�ѧ����ʽΪ��__________________________________________���Իش𣺢�һ�������������������Ǵ�����Ⱦ���������Ҫ�����ܼ����ŷš���Ҫ�Ƶõ���������ͭ������;���ã�________��˵�����ɣ�________________________________________���ȸ�����ѧ֪ʶ���һ����ȡ����ͭ�ĸ�������;����________________________________________
_________________________________________________________________________��
26��ij��������һʯ�Ͳ�Ʒ������4.9��,��ȥ���Ƕ�����NaOH��Һ�������Щ���ᡣ
�� ��Ҫ���100kgʯ�Ͳ�Ʒ�������kgNaOH��
�� �ó����м������죬����Ca��OH��2��Щ���ᣬÿ����100kg����ʯ�ͣ����Խ�Լ����Ԫ���ѣ�����NaOH��Ca��OH��2�г��۸������
| ���� | NaOH | Ca��OH��2 |
| �۸�Ԫ/kg�� | 24��00 | 6��00 |
 27��ij���ʱ�ǩ��ͼ��ʾ������ʽ���㣬�Խ���������⣺
27��ij���ʱ�ǩ��ͼ��ʾ������ʽ���㣬�Խ���������⣺
�� ������̼��к�����̼����淋����������Ƕ��٣��˱�
ǩ�Ƿ��д���
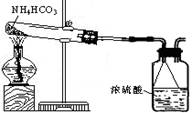
�� ���ݹ��ұ���̼炙��ʵ�NH4HCO3������
�õ���95�����º�ͬѧ����ͼ��ʾװ�ú����·�
Ӧ����������ʵ�飨�������ʲ�������Ӧ����
NH4HCO3![]() NH3��+H2O+CO2��
NH3��+H2O+CO2��
NH3+H2SO4==��NH4��2SO4 ʵ�������±���
| ʵ����� | 1 | 2 | 3 | ƽ��ֵ |
| ʹ����Ʒ��������g�� | �������� | �������� | �������� | �������� |
| ������Һ���ӵ�������g�� | �������� | �������� | �������� | �������� |
�١��� ����С©����������ʲô��_______________________________________________��
�ڡ��� �º���Ϊ��Ӧ��������Һ���ӵ������ǰ�����NH3�������������ݳº�ķ���������ʵ��ƽ��ֵ������û�����̼����淋�����������
�� �������ܷ�˵�����ֻ��ʺϸ������˵��ԭ��_____________________________
_________________________________________________________________________��
�ο��𰸣�
һ��1 C 2 C 3 C 4 B 5 A 6 C 7D 8D 9C 10A 11C 12C 13C 14A
����15 Cu��Fe ����Fe2+��16 Na2CO3��HCl��Ba��OH��2��Na2SO4 17 Ca3��PO4��2��
����NH4HCO3��K2SO4��NH4NO3��18 �Ž�������б���Ѽ������ڱ��ڣ�Ȼ�������ѱ���ֱ�����ü������������ײ�����CO2 ���Ǽס�19 ��Na2CO3 ��Na2SO4
��
| ʵ�鲽�� | ʵ������ | ���� |
| ��ȡ��Ʒ�������Թ��� ������Ʒ�м�ϡ���� �۽�����������ͨ�����ʯ��ˮ | �����ݲ����� ʯ��ˮ����� | ֤����Na2CO3 |
20 ��PH��ֽ����һСƬPH��ֽ���ڲ���Ƭ�ϣ��ò�����պȡ����Һ������PH��ֽ�ϣ�����������ɫ�����ա���ʯ����Һ��AgNO3��Һ��ϡHNO3��21 ��
HCl��Cu��NO3��2��H2SO4��Na2CO3��NH4Cl����Na2CO3��HCl���ܹ��棬H2SO4��Ba��OH��2�����ij����������ᡣ��ȡ��Ӧ�����Һ���ȣ����ų��д̼�����ζ�����壬��֤����NH4Cl������û��NH4Cl��22 �ż�Ρ�����������ܡ�
�Ǣ�CO2��CaO��Ca��OH��2��CaCO3 ��CaCO3![]() CaO+CO2����
CaO+CO2����
CaO+H2O==Ca��OH��2��Ca��OH��2+CO2==CaCO3��+H2O����CO2����õ�������ã���Լԭ�ϣ����������ɱ�����ȡ��������������Թ��У������м�ϡ���ᣬ������������ͨ�����ʯ��ˮ��ʯ��ˮ����ǣ�֤����̼���Ρ���50����
23 ��ϡ���ᣬ�������ݣ�������������Һ��������ɫ���������Ȼ�����Һ��������ɫ������24 ��CaCl2��Һ����Ca��OH��2��Һ��
��2Fe��NO3��3+3Ca��OH��2==2Fe��OH��3��+3Ca��NO3��2
25 �� Cu+4HNO3��Ũ��==Cu��NO3��2+2NO2��+2H2O���� �ţ��űȢ����ĵ������٣���������Ⱦ���٣���2Cu+O2![]() 2CuO��CuO+2HNO3==Cu��NO3��2+H2O
2CuO��CuO+2HNO3==Cu��NO3��2+H2O
26 ��4kg����75.6Ԫ�� 27 �� 113.4�����д��Ƣ��������������������壬ͬʱ�ɷ�ֹ���ᵹ������98.8���� �Dz��ܣ���ΪŨ�������ص����������Dz���NH3��������������H2O��������