化学综合练习(六)
一、选择题(每小题只有一个正确答案)
1. 下列著名诗句中隐含有化学变化的是
A. 白玉做床,金做马 B. 千里冰封,万里雪飘
C. 野火烧不尽,春风吹又生 D. 夜来风雨声,花落知多少
2. 2005年中央电视台春节联欢晚会上,各省市用对联的形式向观众拜年,其中青海省的上联是:水泽源流江河湖海;甘肃省的下联是:金银铜铁镍铬铅锌。金、银、铜、铁、镍、铬、锌属于
A. 金属 B. 非金属 C. 氧化物 D. 化合物
3. 市售的“脑黄金”(DHA)是从深海鱼油中提取的,其主要成分的化学式为:C35H51COOH,则该物质属于
A. 单质 B. 氧化物 C. 化合物 D. 混合物
4. 在太空舱里,为了保持舱内O2、CO2气体含量的相对稳定,常用NiFe2O4作催化剂将宇航员呼出的CO2转化为O2。NiFe2O4中铁为+3价,则Ni的化合价为
A. +1 B. +2 C. +3 D. +4
5. 下图所示的实验操作正确的是
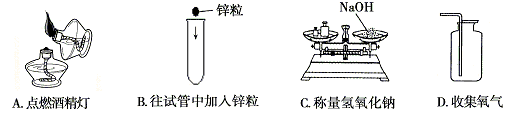
6. 当夜来香花开时,从花旁走过能闻到花香,这一现象说明
A. 分子是可分的 B. 分子能发生化学变化
C. 分子间的间隔不变 D. 分子是在不断运动的
7. 从保护环境的角度出发,下列做法错误的是
A. 植树造林 B. 就地焚烧垃圾
C. 汽车改用清洁燃料 D. 工厂废气经处理达标后再排放
8. 我国计划在2007年发射一颗绕月探测卫星,其任务之一是寻找一种新能源——氦3。氦3原子核是由一个中子和两个质子构成的,其原子核外电子数为
A. 1 B. 2 C. 3 D. 6
9. 下列各组物质在溶液中能大量共存的是
A. FeCl3、Na2SO4、HCl B. NaOH、NaCl、HNO3
C. MgSO4、NaNO3、KOH D. Na2CO3、KNO3、HCl
10. 已知完全中和一定量的某盐酸,需8%的氢氧化钾溶液100g。若改用100g 8%的氢氧化钠溶液,则反应后溶液的pH
A.大于7 B.小于7 C.等于7 D.无法确定
二、选择题(每小题有1~2个正确答案)
11. 化学是一门以实验为基础的自然科学,通过实验可以得知物质的组成、结构、性质及其变化规律。下列通过实验得出的结论正确的是
A. 水能电分解时生成氢气和氧气,说明水是由氢气和氧气组成的
B. 通过在显微镜下观察木炭,得知木炭具有疏松多孔的结构
C. 白磷可以在氧气中燃烧,说明氧气具有可燃性
D. 将紫色石蕊液分别滴入稀盐酸、稀硫酸中,紫色石蕊均变红,说明酸一般能使 紫色石蕊变红
12. 根据所学化学知识判断,下列说法缺乏科学依据的是
A. 盛放酒精、浓氨水的瓶子要塞紧瓶塞 B. 可用汽油洗涤衣服上的油污
C. 可用硫酸铜作饮用水的消毒剂 D. 石墨可作干电池的电极材料
13. 你认为下列实验方案中,可行的是
A. 按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物
B. 向某未知溶液中加入AgNO3溶液,产生白色沉淀,证明溶液是盐酸
C. 用磷在密闭容器中燃烧,除去密闭容器内空气中的氧气
![]()
![]() D. 将pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH
D. 将pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH
14. 将一定量的铝粉和氧化铜混合加热,化学方程式为:3CuO + 2Al 3Cu+Al2O3,反应结束后,为了检验氧化铜是否完全反应,取少量反应后的固体,加入足量稀硫酸充分反应后,将铁片插入溶液中。下列叙述的现象能说明氧化铜没有完全反应的是
①加入稀硫酸后,有气泡生成 ②加入稀硫酸后,溶液中有红色不溶物质
③加入稀硫酸后,没有气泡生成 ④插入溶液中的铁片表面有红色物质出现
A. 只有④ B. ②③ C. ③④ D. ①③④
15. 在a、b两个烧杯内分别盛有等质量且质量分数相同的稀硫酸。现有两片质量相等的锌片,将其中一片放入a烧杯内,另一片先煅烧成氧化锌后再放入b烧杯内。过一会儿两烧杯内的固体都完全溶解,此时
A. a、b两烧杯中硫酸锌的质量相等 B. a烧杯溶液中硫酸锌的质量分数大
C. b烧杯中硫酸锌的质量大 D. b烧杯溶液中硫酸锌的质量分数大
三、(本大题共5题)
16. 我们在初中化学里学过的一些物质,在实际生活中有重要的用途。现有以下物质:A. 不锈钢; B.氧气; C. 生石灰(氧化钙); D. 活性炭; E. 二氧化碳;
F. 水; G. 醋酸; H. 熟石灰(氢氧化钙);I. 锌; J. 盐酸。
请根据它们的用途,用字母代号填空(每种物质限选一次):
(1) 可供急救病人呼吸; (6) 是最常用的溶剂;
(2) 可用于制造炊具; (7) 可用来降低土壤的酸性;
(3) 可用作温室气体肥料; (8) 可用于金属表面除锈;
(4) 可用作某些食品的干燥剂; (9) 可用作干电池负极材料;
(5) 可用作冰箱的除臭剂; (10)通常的食醋中含有约3%~5%的 。
 17. 下图为四种粒子的结构示意图,请用对应的序号填空:
17. 下图为四种粒子的结构示意图,请用对应的序号填空:
(1)属于同种元素的粒子是________。
(2)具有相对稳定结构的粒子是_____。
(3)某元素R形成碱的化学式为R(OH)3,R对应的原子结构示意图可能是______。
 18. 在煤气中加入的少量有特殊气味的乙硫醇(C2H5SH)也可以燃烧,其反应的化学方程式为2C2H5SH
+9O2 4CO2+2X+6H2O,则X的化学式是___________。
18. 在煤气中加入的少量有特殊气味的乙硫醇(C2H5SH)也可以燃烧,其反应的化学方程式为2C2H5SH
+9O2 4CO2+2X+6H2O,则X的化学式是___________。
![]() 19. 某种牵牛花(如图所示)清晨是粉红色,下午却变为蓝紫色,这是由于牵牛花中含有一种遇酸变红,遇碱变蓝的色素。牵牛花清晨呈粉红色是因为经过一夜的呼吸作用,细胞内的_________含量增高,细胞液呈酸性;白天则由于_________作用,细胞内CO2含量降低,花由粉红色逐渐变成蓝紫色,该色素的这种性质与实验室中常用的指示剂_________性质相似。
19. 某种牵牛花(如图所示)清晨是粉红色,下午却变为蓝紫色,这是由于牵牛花中含有一种遇酸变红,遇碱变蓝的色素。牵牛花清晨呈粉红色是因为经过一夜的呼吸作用,细胞内的_________含量增高,细胞液呈酸性;白天则由于_________作用,细胞内CO2含量降低,花由粉红色逐渐变成蓝紫色,该色素的这种性质与实验室中常用的指示剂_________性质相似。
20. 有一不纯的硫酸铵样品(杂质中不含氮元素),经分析知道其中含氮的质量分数为18.9%,则样品中含(NH4)2SO4的质量分数为____________。
四、(本大题共3题)
21. 从铁、二氧化碳、高锰酸钾、氯化铁溶液、水、氢氧化钠溶液、稀盐酸中选出适当物质,分别写出符合下列要求的化学反应方程式,每种物质只能用一次。
(1)化合反应________________________;(2)分解反应________________________;
(3)置换反应________________________;(4)复分解反应______________________。
22.(1)用铜片和银片来比较铜和银的金属活动性大小,可以选用的试剂是__________,该反应属于化学反应基本类型中的_____________反应。
(2)为了检验KCl溶液中是否含有少量BaCl2,可选用的试剂是_______。
 (3)除去NaCl固体中混有的泥沙,应通过溶解、______、______、_____四步实验操作。
(3)除去NaCl固体中混有的泥沙,应通过溶解、______、______、_____四步实验操作。
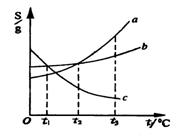
23. 右图是α、b、c三种物质的溶解度曲线,则:
(1)a、b两种物质的溶解度相等的温度是 0C;
(2)t30C时,三种物质的溶解度由大到小的顺序是 。
五、(本大题共3题)
24. 现有如下仪器或装置,供你选择:

(1)写出图中A、B仪器的名称:A ;B 。
(2)实验室制取二氧化碳气体,所需的药品是 和 ;反应的化学方程式为 。其发生装置可选择 (填字母)进行组装,请你分析不用E装置收集二氧化碳气体的原因 。
 (3)上述制取二氧化碳气体的发生装置,还可用于实验室制取的气体是
,写出该反应的化学方程式
。
(3)上述制取二氧化碳气体的发生装置,还可用于实验室制取的气体是
,写出该反应的化学方程式
。
25. 化学晚会上小豆把一张白纸的正反两面向大家展示清楚,然后把白纸用电吹风的热风吹片刻,不一会,白纸上出现了一只小黑猫,大家惊奇不已,你知道这是怎么回事吗?请你用学过的化学知识来解释:(1)小豆事先用_________画了一只猫;
(2)使白纸出现黑猫的物质是_____;表现该物质具有______性。
26. 在一密闭容器内有氧气、二氧化碳、水蒸气及一种未知物质M,在一定条件下充分反应,测得反应前后各物质的质量如下:
| 物质 | 氧气 | 二氧化碳 | 水蒸气 | M |
| 反应前质量/g | 100 | 1 | 1 | 46 |
| 反应后质量/g | 4 | 89 | 55 | x |
(1)根据质量守恒定律,你认为x的值应为_________;(2)未知物质M一定含有的元素为_________;(3)已知未知物质M的相对分子质量为46,推出其化学式为_________;
(4)该反应的化学方程式为_____________________________________________。
六、(本大题共3题)
27. 请指出下列操作可能造成的不良后果:
(1)胶头滴管取用试剂后,将其倒置 ;
(2)倾倒液体药品时,试剂瓶标签没有向着手心 ;
(3)加热固体时,试管口没有略向下倾斜 ;
(4)蒸发溶剂时,未用玻璃棒搅拌 。
28. 阅读材料并回答问题:
材料一:通常食醋中约含3%~5%的醋酸。醋酸的化学式为CH3COOH,在温度高于16.6℃时是一种无色液体,易溶于水,醋酸具有酸的通性。
材料二:钙是人体中的一种常量元素,人们每日必须摄入一定量的钙。动物的骨头中含有磷酸钙,但磷酸钙难溶于水,却能跟酸反应生成可溶性的钙盐。
(1)在10℃时,醋酸的状态是_____________;
(2)生活中能否用铝制品来盛放食醋?________;原因是____________________ ;
(3)人们在熬骨头时,常常会加入少量食醋?这样做的理由是 。
 29. 甲、乙、丙是三种单质,其中甲、丙是固体,乙是气体;A、B、C、D、E都是化合物,其中E是B的水溶液,常存在于大量燃烧煤所导致的酸雨中,而很多建筑物因含有D,易受酸雨的侵蚀。上述物质的相互转化关系如下图所示(部分产物已略去):(1)写出下列物质的化学式:A________,D________;(2)写出反应乙+丙→B的化学方程式:
。
29. 甲、乙、丙是三种单质,其中甲、丙是固体,乙是气体;A、B、C、D、E都是化合物,其中E是B的水溶液,常存在于大量燃烧煤所导致的酸雨中,而很多建筑物因含有D,易受酸雨的侵蚀。上述物质的相互转化关系如下图所示(部分产物已略去):(1)写出下列物质的化学式:A________,D________;(2)写出反应乙+丙→B的化学方程式:
。
七、(本大题共2题)
30. 某地一不法商贩销售的“尿素”中,经检验含氮的质量分数为28%。求:
(1)已知尿素的化学式为CO(NH2)2,则尿素中氮元素的质量分数是多少?(精确到0.1%)
(2)该商贩所售每袋“尿素”(50kg)中,实际含尿素多少千克?
 31. 实验室中浓硫酸的商标如下图所示。请根据有关信息计算:
31. 实验室中浓硫酸的商标如下图所示。请根据有关信息计算:

(1)该试剂瓶中硫酸溶液的质量是___________g。(1克)
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,需这种浓硫酸多少克?
(3)取足量的稀硫酸与6.5g锌充分反应,可制得氢气多少克?
综合练习六参考答案:
1.C 2.A 3.C 4.B 5.D 6.D 7.B 8.B 9.A 10.A 11.BD 12.C 13.C 14.A 15.AB
16. (1)B;(2)A;(3)E;(4)C;(5)D;(6)F;(7)H;(8)J ;(9)I;(10)G
17.(1)B和D;(2)A和D;(3)C
18. SO2
19. CO2;光合;石蕊试液
![]() 20. 89.1%
20. 89.1%
21.(1)CO2 + H2O === H2CO3;(2)2KMnO4 K2MnO4 + MnO2 + O2↑;
(3)Fe + 2HCl === FeCl2 + H2↑;(4)3NaOH + FeCl3 === Fe(OH)3↓ + 3NaCl
22.(1)AgNO3溶液[或Hg(NO3)2等可溶性汞盐溶液] 置换反应;
(2)稀硫酸(或可溶性硫酸盐溶液、可溶性碳酸盐溶液);
(3)过滤 蒸发 结晶
23.(1)t20C;(2)α>b>c
24.(1)试管 铁架台;
(2)稀盐酸 大理石(或石灰石);CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ A B D(或C D) CO2能溶于水;
(3)氢气(或H2) Zn + H2SO4 = ZnSO4 + H2↑(合理答案均可)
![]() 25.(1)稀硫酸 (2)浓硫酸 脱水
25.(1)稀硫酸 (2)浓硫酸 脱水
26.(1)0;(2)C、H、O;(3)C2H6O;(4)C2H6O+3O2 2CO2 + 3H2O
27.(1)腐蚀橡胶头;(2)药品腐蚀标签;(3)试管破裂;(4)液体飞溅
28.(1)固态;(2)不能 因为铝会与食醋中的醋酸反应;
![]() (3)使不溶于水的磷酸钙转变为可溶性钙盐,便于人体吸收
(3)使不溶于水的磷酸钙转变为可溶性钙盐,便于人体吸收
29.(1)CO2 CaCO3;(2)S + O2 SO2
30.(1)46.7%;(2)30g
31.(1)920g;(2)20g;(3)0.2g