秘密★启用前
初中毕业生化学二模考试试题
化 学
本试卷分为选择题和非选择题两部分;第一部分1至4页,第二部分5至8页,共8页,满分100分。考试时间80分钟。
注意事项:
1.答卷前,考生务必在答题卡第1面和第3面上用黑色字迹的钢笔或签字笔填写自己的考生号、姓名;同时填写考场试室号、座位号,再用2B铅笔把对应这两个号码的标号涂黑。
2.选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号;不能答在试卷上。
3.非选择题必须用黑色字迹钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内的相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案,改动的答案也不能超出指定的区域;不准使用铅笔、圆珠笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁,考试结束时,将本试卷和答题卡一并交回。
5.全卷共三大题29小题,请考生检查题数。
可能用到的相对原子质量:H 1 C 12 O 16 Fe 56
第一部分 选择题 (共40分)
一、选择题(本题包括20小题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、不选、多选或涂改不清的,均不给分。
1.下列变化中,不属于化学变化的是
A.二氧化硫在空气中造成酸雨
B. 气球充入过量空气爆炸
C.铁钉在潮湿空气中生锈
D. 铜片在酒精灯上加热变黑
2.高锰酸钾与一定量水配成的溶液可用来消毒,该消毒液是
A.混合物 B.有机物
C.化合物 D.纯净物
3.下列原子属于金属元素的是
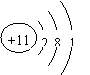 | |||
 | |||
A. B.
 | |||
 | |||
C. D.
4.葡萄糖(C6H12O6)是一种重要的营养物质,下列关于葡萄糖的说法,错误的是
A.葡萄糖是由碳、氢、氧三种元素组成
B.葡萄糖分子中含有6个碳原子和6个水分子
C.葡萄糖属于有机化合物
D.葡萄糖的相对分子质量为180
5.下列各组含氯物质中,氯元素化合价相同的一组是
A. Cl2 HCl B. NaCl HClO
C. ClO2 NaClO2 D. KClO3 Ca(ClO3)2
6.医疗生理盐水是质量分数为0.9%的氯化钠溶液,配制1000g这种生理盐水,所需氯化钠的质量为
A.0.09g B.0.9g C.9g D. 90g
7.向10mLpH为4的溶液中加入等体积的下列试剂,混合液的pH肯定增大的是
A.盐酸 B. 氢氧化钠溶液
C.pH为4的溶液 D. 稀硫酸
8.下列关于分子和原子的说法,正确的是
A.分子构成物质,原子也能直接构成物质
B.分子不停地运动,原子静止不动
C.在化学反应前后,分子和原子的种类保持不变
D.不同种类的原子,不能相互结合成分子
9.下列反应属于化合反应的是
A.电解水制备氢气
B.木炭与氧化铜混合加热得到金属铜
C.煅烧碳酸钙固体得到二氧化碳
D.硫在氧气中燃烧得到二氧化硫
10.牛奶中含钙量高,这里的“钙”通常指的是
A. 分子 B. 原子
C. 元素 D. 单质
|
|
A. B.
|
|
C. D.
12.下列各组气体中,仅用燃着的木条不能区分出来的是
A.一氧化碳和二氧化碳 B. 氧气和空气
C. 甲烷和空气 D. 二氧化碳和氮气
13.盛有饱和氢氧化钠溶液的烧杯在空气中放置一段较长时间,则该溶液中
A.氢氧化钠的质量减少
B.氢氧化钠的质量增大
C.氢氧化钠的质量分数增大
D.氢氧化钠的质量分数保持不变
14.根据组成元素的类别,对下列氧化物进行分类,其中一种与另外三种不属于同一类别,它是
A.MnO2 B.Cu2O C.P2O5 D.Fe3O4
15.下列说法不正确的是
A.化学反应在生成新物质的同时,还伴随着热量放出
B. 人类应更多地开发和利用太阳能、风能、地热能等新能源
C. 乙醇属于可再生能源
D. 人体活动所需能量与食物在体内的化学反应有关
16.下列各组物质,相互不能发生反应的是
A.氢氧化钠溶液和硫酸
B.氧化铁和盐酸
C.三氧化硫和氢氧化钠溶液
D.盐酸和二氧化碳
17.向结有水垢的热水瓶中加入稀盐酸,水垢溶解脱落;向所得溶液中加入过量Na2CO3溶液,又有白色沉淀出现,这种水垢可能含有
A.BaSO4 B.CaCO3
C.K2CO3 D.AgNO3
18.将金属Cu投入金属A的盐溶液中,观察到Cu的表面出现银白色物质;金属B投入稀硫酸中,观察到B的表面有气泡产生。下列关于金属A、B、Cu的活动性的叙述正确的是
A.B>Cu>A B.A>Cu>B
C.B>A>Cu D.A>B>Cu
19.据报道,某研究小组将二氧化碳与氢气按1:4比例在一定温度、压强下混合并以铑-镁为催化剂可生成X,其反应为:CO2+4H2==X+2H2O,则X为
A. CO B. CH4
C. H2 D. C
20.要除去硫酸镁溶液中混有的少量硫酸和硫酸铜,可加入下列物质中的
A.氢氧化钠 B.铁粉
C.氧化镁 D.镁粉
第二部分 非选择题 (共60分)
二、本题包括5小题,共34分
21.(7分)用化学用语表示下列物质或反应:
(1)硫酸钠: ;
(2)2个磷原子: ;
4个磷原子构成的白磷分子 ;
(3)镁条用砂纸打磨后放入氧气中,过一会儿,光亮的镁条变暗,反应的化学方程式是 ;
(4)饱和氯化钠溶液中,存在的微小粒子是 ;
22.(5分)下图是a、b两种固体物质的溶解度曲线。
 |
(1)图中a物质的溶解度曲线比b物质陡,说明 ;
(2)20℃时,100g水中最多能溶解的a物质的质量是 g,此时,要想在100g水中溶解更多的a物质,可采取的措施是 。
(3)40℃时,将40g a物质放入在100g水中,充分搅拌,所得溶液的质量是
g。
23.(8分)工业炼铁是把铁矿石和焦炭等原料一起加入高炉,在高温下通入空气进行一系列反应把铁还原出来。
(1)通入空气使固态的焦炭转化为具有还原性的气态物质,转化过程中涉及的反应的化学方程式是 。
(2)赤铁矿(主要成分为Fe2O3)在高炉里反应生成单质铁的化学方程式是: 。
(3)计算:
①Fe2O3的相对分子质量是: ;
②5000t含氧化铁84%的赤铁矿中,其氧化铁的质量是 t;
③上述赤铁矿理论上可炼得含铁98%的生铁 t。
24.(6分)生石灰是白色的块状物,在实际生产中,应用非常广泛。
(1)生石灰的主要成分为(填化学式) 。在食品包装中,常用生石灰作干燥剂,其干燥原理是(用化学方程式表示) ;在使用时,是用纸袋装着生石灰放入包装盒中,如果用塑料袋装生石灰就起不到干燥的作用,原因是 。
(2)在农村,生石灰也常用于畜禽栏舍的消毒。畜禽出栏后,将生石灰用水调成20%的石灰乳,涂刷墙面和地面。某农户误将生石灰直接撒在猪圈中消毒。一段时间后,发现猪的蹄部干燥开裂,有的甚至出现灼伤、溃疡。原因是
。
(3)上述用于消毒的浆状物要现配现用,如放置过久,就没有消毒作用了,其原因是(用化学方程式表示): 。
25.( 7分)某工厂的甲、乙、丙三个车间排出的污水中分别含有以下六种物质中的两种:KOH、HNO3、AgNO3、KCl、K2SO4、Ba(NO3)2。三个车间的污水经过滤后初步分析,情况如下:
| 车间 | 外观 | pH | 污水成分 | |
| 肯定含有 | 可能含有 | |||
| 甲 | 无色、透明 | >7 | ? | ? |
| 乙 | 无色、透明 | =7 | Ba(NO3)2 | ? |
| 丙 | 无色、透明 | <7 | ? | ? |
为了进一步确定各溶液的组成,进行如下实验:
 |
已知溶液中不可能同时存在Ag+和OH-,且两次混合均完全反应。根据以上信息回答:
(1)甲溶液中肯定含有的物质是(填化学式,下同) ,可能含有的另一种物质是 ,据此,沉淀X是 。
(2)根据(1)的判断,混合(Ⅱ)发生反应的化学方程式是 ;
(3)M溶液中溶质的化学式是 ,它是一种复合肥料,含有农作物所需的营养元素是(填元素符号) 。
三、本题包括4小题,共26 分。
26.(4分)将细口瓶中的液体倾倒到试管中时,应注意的事项是
(1)细口瓶的塞子应 在桌上;
(2)倾倒液体时,标签应 ,瓶口要挨着试管口,缓慢地倒。
27.
(10分)自然界中的水含有各种杂质,可以用
不同的方法进行净化。
(1)右图所示是用空饮料瓶、带导管的单孔
胶塞、蓬松棉、纱布、活性炭、小卵石、
石英沙等材料自制的一个简易净水器。
①根据上述净化材料的特性,B层最好放
置 ;
 ②该净水器不同位置的纱布所起的主要作用不同,其中第二层纱布的作用是:
②该净水器不同位置的纱布所起的主要作用不同,其中第二层纱布的作用是:
③你认为上述简易净水器(填“可以”或“不可以”)
将硬水变成软水。
(2)实验室为了配制溶液,常用如右图所示的装置制
取净化程度较高的蒸馏水。
①在连接好装置后,应先进行 的操作,再加入水和沸石进行蒸馏;
②在烧瓶中加入沸石的目的是 。
28.(6分)温室效应已引起全球广泛关注。某校研究小组的同学在“我与化学”活动中,为了研究CO2气体对空气温度的影响,进行了下列实验:
实验一,制取研究所需的CO2气体
实验室可用下列A、B装置制取CO2
(1)写出下列装置中仪器的名称:a ,b 。
(2)与A装置相比较,B装置的优点是便于在反应过程中
;
实验二、探究光照条件下CO2气体对空气温度是否有影响
步骤1:用5个规格相同的塑料矿泉水瓶分别收集1瓶空气、1瓶CO2以及3瓶CO2含量分别为10%、20%、30%的空气和CO2的混合气体,并用带温度计的胶塞塞紧瓶口;
2.把上述装有气体的矿泉水瓶放到电灯下照射,每隔1分钟记录一次温度,实验数据如下表:
|
CO2含量 | 起始 | 1 | 2 | 3 | 4 | 5 |
| 全部空气 | 23.0 | 23.3 | 23.9 | 24.6 | 25.0 | 25.5 |
| 10% | 23.0 | 23.5 | 24.2 | 25.0 | 26.0 | 27.0 |
| 20% | 23.0 | 24.0 | 24.5 | 25.5 | 26.5 | 27.5 |
| 30% | 23.0 | 24.5 | 25.0 | 26.2 | 27.5 | 29.0 |
| 100% | 23.0 | 30.0 | 33.0 | 35.6 | 37.0 | 39.5 |
回答下列问题:
(3)仔细阅读表中数据,该实验可以得出的结论是:
① ;
② 。
(4)根据上述数据推测,在相同条件下,当CO2气体含量为25%时,温度达到25.5℃所需要的时间范围为 min。
29.(6分)实验室有三瓶没有标签的液体,分别是氢氧化钠溶液、硫酸铜溶液和稀盐酸,不用其他试剂,设计实验进行鉴别,并完成实验报告。
| 实验步骤 | 实验现象与结论 |
化学参考答案
第一部分 选择题 (共40分)
一、选择题(本题包括20小题,每小题2分,共40分)
注意:每道选择题有四个选项,其中只有一项符合题意。请用铅笔在答题卡上作答。选错、不选、多选或涂改不清的,均不给分。
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | A | A | B | D | C | B | A | D | C |
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | C | D | A | C | A | D | B | A | B | D |
第二部分 非选择题 (共60分)
二、本题包括5小题,共34分
21.(7分)
(1)Na2SO4 (2)2P,P4;
(3)2Mg + O2 == 2MgO; (4)Na+、Cl-、H2O;
22.(5分)
(1)a物质的溶解度受温度的影响比b物质大 (2)10,加热
(3)130
|
|
|
3CO+Fe2O3====2Fe+3CO2。
(2)①160,②4200,③3000。
24.(6分)
(1)CaO,CaO+H2O=Ca(OH)2;水分子不易透过塑料被CaO吸收。
(2)①CaO可与猪蹄表面的水分反应而吸收水分,并且放出大量的热,可能导致灼伤;
②Ca(OH)2对皮肤具有腐蚀性。
(3)Ca(OH)2+CO2=CaCO3+H2O。
25.(7分)
(1)KOH,K2SO4(或KCl),AgCl(或BaSO4)
(2)K2SO4+Ba(NO3)2==BaSO4↓+2KNO3;HNO3+KOH==H2O+KNO3
或KCl+AgNO3==AgCl↓+KNO3;HNO3+KOH==H2O+KNO3
(3)KNO3,K、N。
三、本题包括4小题,共26分。
26.(4分)
(1)倒放 (2)朝向手心
27.(7分)
(1)①石英沙 ②将A层物质与B层物质隔离 ③不可以
(2)①检查装置的气密性; ②防止液体暴沸(或液体沸腾太剧烈)
28.(7分)
(1)试管,长颈漏斗
(2)添加反应液(或盐酸)。
(3)①在白炽灯光照条件下,CO2的存在对空气温度有影响;
②光照相同时间时,空气中CO2含量越高,气体的温度越高。
(4)2-3
29.(8分)
| 实验步骤 | 实验现象与结论 |
| 1、观察溶液颜色。 | 溶液为蓝色的是硫酸铜溶液,溶液为无色的是氢氧化钠溶液和稀盐酸 |
| 2、取任一无色溶液少量于试管中,再滴入硫酸铜溶液。 | 如果出现蓝色沉淀该溶液是氢氧化钠溶液,如果没有蓝色沉淀出现该溶液是稀盐酸 |
 时间
时间