2008年湖北省宜昌市初中毕业生学业考试
化 学 试 题
(考试形式:闭卷 试题共六大题28小题 卷面分数:100分 考试时限:90分钟)
我要注意:1.本卷共8页。其中试题6页,答题卷2页;请将答案填在答题卷相应的地方,交卷时只交答题卷。
2.答题中可能用到的数据和资料:
(1)相对原子质量:H~1 C~12 N~14 O~16 K~39 Ca~40
(2)碳酸钠的水溶液显碱性
(3)20℃时部分酸、碱、盐的溶解性:
| OH- | NO3- | Cl- | SO42- | CO32- | |
| H+ | - | 溶、挥 | 溶、挥 | 溶 | 溶、挥 |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Fe3+ | 不 | 溶 | 溶 | 溶 | — |
| Cu2+ | 不 | 溶 | 溶 | 溶 | 不 |
| Ag+ | — | 溶 | 不 | 微 | 不 |
一、我会选择(本题共16小题。每小题只有一个选项符合题意。1~12题,每小题2分;13~16题,每小题3分,共36分)
1.下列变化属于化学变化的是
A.冰棒融化 B.木材燃烧
C.湿衣服晾干 D.灯泡发光
2.空气中体积分数最高的气体是
A.氮气 B.氧气
C.二氧化碳 D.稀有气体
3.在家庭用的调味品中,与水充分混合后,不能形成溶液的是
A.食用油 B.食盐 C.味精 D.蔗糖
4.下列实验操作正确的是
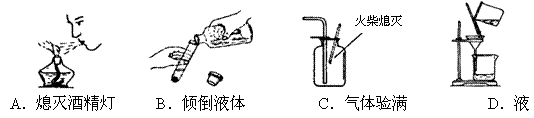
5.下列物质属于氧化物的是
A.O2 B.CH4 C.H2O D.KClO3
6.每年五、六月份,人们在桅子花树旁会闻到怡人的香味。这一现象说明
A.分子很小 B.分子分裂成原子
C.分子在不停地运动 D.分子之间有间隔
7.小京同学今天的午餐食谱是:主食——面包;配菜和副食——炸鸡腿、炸薯片、牛排、奶酪。小京午餐食谱缺乏的营养素是
A.糖类 B.脂肪 C.蛋白质 D.维生素
 8.下列有关汽水的说法正确的是
8.下列有关汽水的说法正确的是
A.汽水的pH为3~4,它显碱性
B.胃酸过多的人要多喝汽水
C.CO2易溶于水,所以用来制汽水
D.打开汽水盖时,有大量气泡冒出,说明气体的溶解度随压强
减小而减小
9.造成酸雨的元凶是
A.大量使用塑料购物袋 B.工业和生活污水任意排放
C.大量使用煤作燃料 D.农业生产任意使用农药和化肥
10.从水分子分解示意图中我们能获得许多信息,其中描述错误的是
 A.这是一个化合反应
A.这是一个化合反应
B.水分解时元素的种类不变
C.在化学变化中原子是最小的粒子
D.氢分子能保持氢气的化学性质
11.化学知识中有很多的“相等”,下列说法中错误的是
A.原子中质子数与中子数一定相等
B.溶液稀释前后,溶质的质量相等
C.在化合物里,元素正价总数和负价总数的绝对值相等
D.参加中和反应的氢离子个数与氢氧根离子个数相等
12.向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热,分反应后过滤。以下判断错误的是
A.滤纸上可能含有铜 B.滤液中可能含有硫酸亚铁
C.滤液中可能含有硫酸铜 D.滤纸上可能含有氧化铜
13.维生素是人体必需的重要营养素之一,它能促进人体生长发育,增强人体对疾病的抵抗能力。关于维生素C(C6H8O6)的说法错误的是
A.C6H8O6表示维生素C这种物质
B.维生素C是由C、H、O三种元素组成
C.维生素C是由C、H、O三种原子构成
D.1个维生素C分子中含有20个原子
14.在下列各化学反应中,不属于放热反应的是
A.镁带与盐酸反应 B.生石灰与水反应
C.酒精在空气中燃烧 D.碳和二氧化碳反应
15.两同学围绕蜂窝煤燃烧进行了如下探究,其中依据质量守恒定律解释的是
A.当煤燃烧正旺时将炉门关上,煤层上方发现蓝色火焰。解释:此时氧气不足而产生的CO在燃烧
B.煤燃烧完后煤灰质量比煤的质量轻。解释:煤燃烧后产生的二氧化碳等气体逸出
C.在煤炉上方放一壶水不能防止CO中毒。解释:CO难溶于水
D.将煤做成蜂窝状就更易燃烧。解释:蜂窝状的煤与空气接触面积增大
16.下列知识整理的内容不完全正确的一组是
| A | 食品保鲜的办法 | B | 灭火实例与原理 |
| 填充氮气——防止变质 放入生石灰——防止受潮 放入细铁粉——防止受潮和变质 | 油锅着火时用锅盖盖灭——隔绝空气 住宅失火时用水灭火——降低着火点 扑灭森林火灾时设置隔离带——隔离可燃物 | ||
| C | 日常物质的区别 | D | 化学中常见的“三” |
| 硬水和软水——加肥皂水并搅拌 羊毛和化纤——点燃后闻气味 氯化铵和磷矿粉——观察颜色 | 三种可燃性气体——H2、CO、CH4 三种可加热仪器——试管、烧杯、蒸发皿 三种构成的粒子——分子、原子、离子 |
二、我会填空(共5小题,化学方程式每空2分,其余每空1分,共15分)
17.(3分)用化学符号表示:
2个氮原子 17 ;3个五氧化二磷分子 18 ;正二价的镁元素 19 。
 18.(3分)北京奥运会游泳馆“水立方”内部材料主要由金属材料钢铁构成,外部材料聚氟乙烯属于 20 材料。为确保“水立方”的水质达到国际泳联最新卫生标准,泳池的水将采用“砂滤—臭氧—活性炭”净水工艺,其中活性炭净水是利用它的
21
性。“水立方”还设计了循环用水、收集应用雨水等系统,达到了 22 的目的,充分体现了绿色奥运的理念。
18.(3分)北京奥运会游泳馆“水立方”内部材料主要由金属材料钢铁构成,外部材料聚氟乙烯属于 20 材料。为确保“水立方”的水质达到国际泳联最新卫生标准,泳池的水将采用“砂滤—臭氧—活性炭”净水工艺,其中活性炭净水是利用它的
21
性。“水立方”还设计了循环用水、收集应用雨水等系统,达到了 22 的目的,充分体现了绿色奥运的理念。
19.(2分)有些物质有毒性,如CO、 23 等,有些物质有腐蚀性,如NaOH、
24 等,这些物质如果应用不慎会危及人体健康。有些物质如食盐虽无毒、无腐蚀性,但长期使用过多也不利于人体健康。
20.(4分)用10mL量筒取2mL氢氧化钠溶液滴入试管中,然后用滴管向试管中滴加硫酸铜溶液,有蓝色沉淀生成,其化学方程式是 25 。再用试管夹夹住试管,放在酒精灯火焰上加热,看到蓝色沉淀变成黑色固体。这一变化的化学方程式是 26
21.(3分)右图是A、B、C三种物质的溶解度曲线,据图回答:
![]()
 (1) t1℃时A、B、C三种物质的溶解度由大
(1) t1℃时A、B、C三种物质的溶解度由大
到小的顺序是 27 (填写序号,下同)。
(2) t1℃时30gA物质加入到50g水中不断搅拌,
形成的溶液质量是 28 g。
(3) 将t1℃时A、B、C三种物质饱和溶液的
温度升高到t2℃时,三种溶液的溶质质量分数
由大小关系是 29 。
三、我会说明(共2小题,化学方程式每空3分,其余每空1分,共12分)
22.(10分)实验室常用下列装置研究气体的制取和性质,根据所学知识回答下列问题。
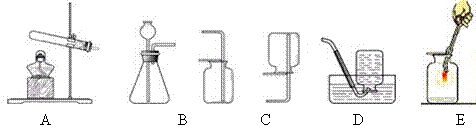

(1) 写出实验室制取氧气的一个化学方程式 30 。利用该反应制取氧气,发生装置应选 31 (填序号,下同)。
(2) 一氧化氮气体难溶于水,在空气中容易发生下列反应2NO+O2==2NO2,则收集一氧化氮气体时不能用的装置是(填序号) 32 。
(3) 按图F作细铁丝在氧气中燃烧的实验,我观察到的现象有 33 (只答一条),其相关的化学方程式是 34 。
(4) 实验室里将制得的二氧化碳气体通入澄清石灰水中,始终未出现浑浊现象,可能的原因是 35 。
23.(2分)自来水厂常用氯气消毒杀菌,化学方程式为Cl2+H2O![]() HCl+HClO。而HCl、HClO在水中会解离出H+、Cl-和ClO-,在野外也可以用漂白粉[Ca(ClO)2]对水进行消毒杀菌。
HCl+HClO。而HCl、HClO在水中会解离出H+、Cl-和ClO-,在野外也可以用漂白粉[Ca(ClO)2]对水进行消毒杀菌。
(1) HClO中氯元素的化合价是 36 。
(2) Ca(ClO)2在水中会解离出Ca2+和ClO-,我认为在水中起到消毒杀菌作用的离子是
____37 。
四、我会分析(共2小题,化学方程式每空3分,其余每空1分,共17分)
 24.(11分)碳与碳的化合物在工农业生产及日常生活中有广泛的用途。
24.(11分)碳与碳的化合物在工农业生产及日常生活中有广泛的用途。
(1)右图是碳原子结构示意图,碳原子的质子数是 38 ,碳元素在
元素周期表中位于第 39 周期。
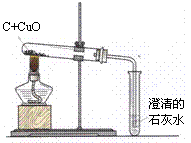 (2) 古代用墨书写或绘制的字画虽年久仍不变色,原因是墨中主要成分碳具有 40 性。右图是木炭还原氧化铜的实验,大试管中的反应体现了碳的还原性,其反应的化学方程式是 41 ,单质碳的还原性可以用于冶金工业。
(2) 古代用墨书写或绘制的字画虽年久仍不变色,原因是墨中主要成分碳具有 40 性。右图是木炭还原氧化铜的实验,大试管中的反应体现了碳的还原性,其反应的化学方程式是 41 ,单质碳的还原性可以用于冶金工业。
(3) 二氧化碳能参与光合作用完成大气中的“碳循环”,但是大气中二氧化碳的含量不断上升,会使全球变暖,从而导致 42 。蔬菜大棚用作气肥的二氧化碳,可用多种方法制得,例如可以用稀硫酸与碳酸氢铵(NH4HCO3)反应制得,反应后生成硫酸铵、水和二氧化碳,这一反应的化学方程式是 43 。
(4) 研究发现:物质的结构决定性质,物质的性质决定用途。如:一氧化碳也能还原氧化铜,也有还原性。从化学反应前后碳元素化合价的变化特点分析,一氧化碳和碳都具有还原性的原因是 44 。
![]()
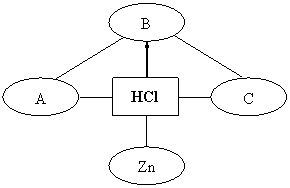 25.(6分)构建知识网络是一种重要的学习方法。下图是关于盐酸化学性质的知识网络,“——”表示相连的两种物质能发生反应,“ ”表示一种物质转化成另一种物质,A、C属于不同类别的化合物。完善这个知识网络:
25.(6分)构建知识网络是一种重要的学习方法。下图是关于盐酸化学性质的知识网络,“——”表示相连的两种物质能发生反应,“ ”表示一种物质转化成另一种物质,A、C属于不同类别的化合物。完善这个知识网络:
(1) 写出A、B、C的化学式:
A 45 ;B 46 ;C 47 。
(2) 根据自己得出的知识网络写出
一个复分解反应化学方程式:
48
五、我会探究(共1小题, 化学方程式每空3分,其余每空1分,共13分)
26.(13分)复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验。
探究1:研究常见物质组成


A、B、C都是研究物质组成的实验。从研究方法得知,A实验是利用可燃物消耗瓶内的 49 ,使瓶内压强减小来推测空气里氧气含量的。B实验是通过证明生成物的
50 来推断水的组成的。而C实验与 51 (填实验代号)实验的方法相同。
探究2:研究常见物质性质——氢氧化钠与硫酸是否刚好完全中和
(1) 探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量。
(2) 验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中, 52 | 53 | 证明研究结论正确 |
写出(2)出中涉及的化学方程式 54 。
探究3:研究常见物质制取——制取氢氧化钠溶液
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠。”他提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有 氢氧化钠 |
小妮认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是
55 。
小妮设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 56 | 57 | 无色溶液中确实 含有氢氧化钠 |
我认为:小欢和小妮的实验是为了证实小京结论的可靠性,小京的结论不可靠,原因
是 58 。显然小妮的实验可靠性比小欢的实验好,原因是 59 。
六、我会计算(共2小题,第27小题2分,第28小题5分,共7分)
27.(2分)化肥硝酸铵的化学式为(NH4NO3)。试求:
(1) 硝酸铵中N、H、O三种元素的质量比 60 ;
(2) 为了保证某一农作物获得3.5㎏氮元素,则需要 61 ㎏硝酸铵。
28.(5分)50g Ca(NO3)2溶液与50g K2CO3溶液混合后,恰好完全反应。经过滤、干燥、称量,得到5g沉淀。反应的化学方程式是:K2CO3+Ca(NO3)2==CaCO3↓+2KNO3。
请计算:
(1) 参加反应的K2CO3的质量。
(2) 过滤后所得溶液的溶质质量分数。
62
2008年湖北宜昌市初中毕业生学业考试化学试题
参考答案及评分说明
一、我会选择(共16小题。每小题只有一个选项符合题意。1~12题,每小题2分;13~16题,每小题3分,共36分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | B | A | A | D | C | C | D | D | C | A | A | B | C | D | B | B |
二、我会填空(共5小题。化学方程式每空2分,其余每空1分,共15分。书写化学方程式时,只要化学式有错误,该空不得分;若化学式均正确,配平错或反应条件错或生成物状态标注错共扣1分。下同)
17、17 2N;18 3P2O5;19 Mg
18、20 合成材料(或有机合成材料);21 吸附;22 节约用水(或节水)
19、23 SO2(或NO2或亚硝酸钠或甲醛或黄曲霉素等合理答案也可,写化学式也可)
24 浓硫酸 [或氢氧化钙或Ca(OH)2]
20、25 2NaOH + CuSO4
== Na2SO4 + Cu(OH)2↓;26 Cu(OH)2![]() CuO + H2O
CuO + H2O
21、27 B>C>A(或B、C、A或BCA);28 65;
29 B>C>A(或B、C、A或BCA)
三、我会说明(共2小题。化学方程式每空3分,其余每空1分,共12分)
22、30 2H2O2![]() 2H2O+O2↑(或2KClO3
2H2O+O2↑(或2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
或2KMnO4![]() K2MnO4+MnO2+O2↑);31 B(或A);32 B和C(或B、C)
K2MnO4+MnO2+O2↑);31 B(或A);32 B和C(或B、C)
33 剧烈燃烧(或火星四射或生成黑色固体或放出热量);34 3Fe+2O2![]() Fe3O4
Fe3O4
35 生成的二氧化碳中混有氯化氢气体(或盐酸浓度较高,挥发出了氯化氢气体或石灰水变质或二氧化碳的量很少)
23、36 +1;37 ClO-(或次氯酸根)
四、我会分析(共2小题,化学方程式每空3分,其余每空1分,共17分)
24、38 6;39 4(或四);
40 常温下的稳定(或常温下化学性质稳定或常温下化学性质不活泼);
41
C+2CuO![]() 2Cu+
CO2↑;42 温室效应
2Cu+
CO2↑;42 温室效应
43 H2SO4+2NH4HCO3==(NH4)2SO4+H2O+CO2↑
44 碳元素的化合价升高(或碳元素的化合价由低到高或反应后碳元素变成+4价)
25、45、46、47 NaOH、CuCl2、Na2CO3 NaOH、HNO3、Fe2O3
【说明:B物质对得1分,A与B、HCl全对得1分,C与B、HCl全对得1分;若B物质错则不得分。填物质名称不得分。本题属开放性答案,其它合理答案也可】
48 Na2CO3+2HCl==2NaCl+H2O+CO2↑[或NaOH+HCl==NaCl+H2O
或2NaOH+CuCl2==Cu(OH)2↓+2NaCl或Na2CO3+CuCl2==CuCO3↓+2NaCl等]
【说明:所写化学方程式要与45、46、47三空对应,只有得分的物质,该化学方程式才能得分,否则不给分】
五、我会探究(共1小题。化学方程式每空3分,其余每空1分,共13分)
26、49 氧气;50 元素种类(或组成或成分或氢气、氧气或H2、O2);51 B
52 加入锌粒(或加入氧化铜或加入氢氧化铜或加入碳酸钠等其它合理答案也可)
53 有气泡产生(或出现蓝色溶液或固体溶解,溶液变蓝或有气泡产生等)
54 Zn+H2SO4==ZnSO4+H2↑(或CuO+ H2SO4==CuSO4+H2O
或Cu(OH)2+ H2SO4== CuSO4+2H2O或Na2CO3+ H2SO4==Na2SO4+H2O+CO2↑)
【说明:52、53二空所写步骤、现象匹配,54空所写化学方程式与实验方案相关。其它合理答案也可】
55 碳酸钠溶液也能使无色酚酞试液变红(或碳酸钠溶液也显碱性)
56 取少量样品于试管中,加入足量的BaCl2溶液[或CaCl2溶液或Ba(NO3)2溶液或Ca(NO3)2溶液……];过滤,在滤液中滴加几滴无色酚酞溶液。(或过滤,在滤液中滴加硫酸铜溶液、硫酸镁溶液……)
57 生成白色沉淀,酚酞溶液变红[或产生蓝色沉淀、白色沉淀……]
【说明:56、57二空所写步骤、现象完整且匹配,其它合理答案也可】
58 没有证明有氢氧化钠生成(或生成的不一定是氢氧化钠)
【说明:55、58二空答案若雷同,只给一空分】
59 排除了干扰因素(或实验现象唯一或实验现象不同)(其它合理答案也可)
六、我会计算(共2小题。27题2分,28题5分,共7分)
27、60 28:4:48(或7:1:12);61 10
28、62 解:设K2CO3的质量为x,生成KNO3的质量为y
K2CO3 + Ca(NO3)2 == CaCO3↓ + 2KNO3
![]() 138 100 202
138 100 202
x 5g y …………………… 1分
(1) ![]() …………………………… 1分
…………………………… 1分
(2) ![]() …………………………… 1分
…………………………… 1分
溶液的质量=50g + 50g—5g = 95g ……………………………………… 1分
所得溶液的溶质质量分数为:![]() ………………… 1分
………………… 1分
答:K2CO3的质量为6.9g,溶液的溶质质量分数为10.6%
【说明:设、答为扣分内容,不单独给分。其它合理解答,也可分步给分】