2006年高要市初三化学模拟试题
注意事项:答题前,考生务必用黑色碳素墨水的签字笔,将自己的考生号、座位号和姓名填写在答题卡的密封线内。选择题用B型铅笔将答题卡Ⅰ卷对应题目的标号涂黑,全卷均答在答题卡上。
可能用到的相对原子质量:H-1; C-12;O-16;S-32 ;Zn-65
一、选择题(每题2分,共28分)
1. 2004年5月1日实施的新交通法加大了对“洒后驾车”的处罚力度。交警常用装有重络酸钾(K2Cr2O7)的仪器,检测司机是否洒后驾车。其原理是红色的重铬酸钾遇酒精后生成蓝绿色的物 质。下列说法不正确的是
A.该变化是化学变化 B.重铬酸钾中铬元素的化合价为+3价
C.分子是不断运动的 D.乙醇具有挥发性
2. 下列实验操作不正确的是
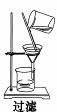 | 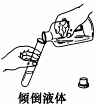 | 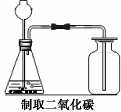 | |||||
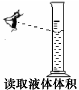 | |||||||
A B C D
3.分别将下列各组物质,同时加到足量水中,能得到无色透明溶液的是
A.HNO3、KOH、FeCl3 B.K2SO4、KCl、HCl
C.AgNO3、HCl、KCl D.Na2CO3、KCl、BaCl2
4、用一块棉布手帕浸泡在盛有质量分数约为 70 %酒精的溶液中,待均匀湿透后取出。将浸透的手帕展开,用镊子夹住两角,用火点燃,当手帕上的火焰熄灭后,手帕完好无损。对于这一现象,下面解释正确的是
A. 这是魔术,你所看到的是一种假象
B. 火焰的温度低于棉布的着火点
C. 手帕上的水汽化吸热,使手帕的温度低于棉布的着火点
D. 酒精燃烧后使棉布的着火点升高
5.下列各物质中的杂质(括号内为杂质),不能用稀盐酸除去的是
A.NaCl(Na2CO3) B.C粉(CuO) C.Cu粉(Mg粉) D. KNO3(KCl)
6. 据《说文解字》记载,我们的祖先在神农氏时代就开始利用海水晒盐。海水晒盐的原理是
A.日晒风吹使海水中的氯化钠蒸发 B.日晒风吹使溶液由饱和变为不饱和
C.日晒风吹使水分蒸发、晶体析出 D.日晒风吹使氯化钠的溶解度变小
7. 日常生活中的下列做法,可用物质的化学性质解释的是
①用汽油洗掉衣服上的油污 ②用纯碱除去面团因发酵产生的酸味
③用木炭粉除去冰箱内的异味
④家庭中熬骨汤时,加入少量食醋可以增加汤中的钙质
A.①② B.②④ C.①③④ D.②③④
8.下列叙述正确的是
A.物质的水溶液一定是无色透明的
B.饱和溶液是纯净物,不饱和溶液是混合物
C.当饱和溶液的温度升高时,其溶质的溶解度一定变大
D.饱和溶液不一定比不饱和溶液浓
9.据统计,我国仅20世纪90年代就发生火灾约89万起,给人民造成重大损失。应用
 化学知识能有效地预防和控制火灾。下面对图中灭火实例的灭火原理解释不正确的是
化学知识能有效地预防和控制火灾。下面对图中灭火实例的灭火原理解释不正确的是
| 灭火实例 | 灭火原理 | |
| A | 住宅失火时,消防队员用水灭火 | 降低可燃物的着火点 |
| B | 酒精在桌上着火时,用湿抹布盖灭 | 隔绝空气或氧气 |
| C | 炒菜油锅着火时,用锅盖盖熄 | 隔绝空气或氧气 |
| D | 扑灭森林火灾时,设置隔离带 | 可燃物与燃烧物隔离 |
10.小明从化学课知道蛋壳的主要成份是碳酸盐,决定制作一个“无壳鸡蛋”送给妈妈,他应从厨房中选择鸡蛋和下列物质的
A. 味精 B. 白酒 C. 酱油 D. 白醋
11.铝在人体内积累可使人慢性中毒,引起老年痴呆症。1989年世界卫生组织正式将铝确定为“食品污染源之一”而加以控制,铝在下列使用场合一般无须控制的是
A. 电线、电缆 B. 牙膏皮
C. 制造饮具和餐具 D. 糖果、香烟内包装
12.在温室大棚内生产蔬菜或花卉的过程中,常向棚内施放适量的二氧化碳,其主要目的是
A.使害虫窒息死亡,防止植物的病虫害
B.促进植物的光合作用,提高蔬菜等的产量和质量
C.产生温室效应,提高棚内温度
D.避免棚内发生火灾
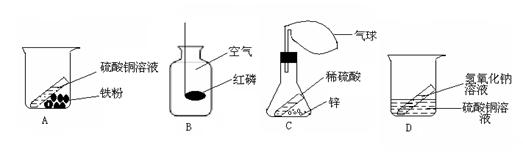 13.在探索质量守恒定律实验中,设计了如下图的实验装置,其中反应前后容器中物质的总质量不相等的是
13.在探索质量守恒定律实验中,设计了如下图的实验装置,其中反应前后容器中物质的总质量不相等的是
14.已知一种碳原子(质子数、中子数均为6)的质量为 a g,钠的相对原子质量为b,则一个钠原子的质量为( )
![]()
二、填空题(25分)
15.(7分)化学来自生活,用于生活。下表列出了生活中常用物质溶液的pH及一种主要成分(其他成分未列出)。试回答:
| 编号 | ① | ② | ③ | ④ | ⑤ |
| 名称 | 食醋 | 白酒 | 白糖水 | 石灰水 | 纯碱溶液 |
| 主要成分 | CH3COOH | C2H5OH | C12H22O11(蔗糖) | Ca(OH)2 | Na2CO3 |
| 溶液pH | 3 | 7 | 7 | 11 | 10 |
![]()
![]() (1)将上表①~⑤中的主要成分进行分类(填序号,下同)
(1)将上表①~⑤中的主要成分进行分类(填序号,下同)
![]()
![]() 属于酸的是______________;属于碱的是_____________;
属于酸的是______________;属于碱的是_____________;
属于盐的是______________;属于有机物的是_________。
![]() (2)当有人被蚊虫(体内含一种酸性物质)叮咬后,为减轻疼痛,可在伤处涂_________。
(2)当有人被蚊虫(体内含一种酸性物质)叮咬后,为减轻疼痛,可在伤处涂_________。
![]()
![]() (3)铝壶长时间煮水,内有一层水垢[主要含CaCO3和Mg(OH)2],可选用________采取少量多次的方法除去,不能采取大量一次的原因是__________。
(3)铝壶长时间煮水,内有一层水垢[主要含CaCO3和Mg(OH)2],可选用________采取少量多次的方法除去,不能采取大量一次的原因是__________。
16.(4分)如图为a、b两物质的溶解度曲线,请依图回答下列问题:
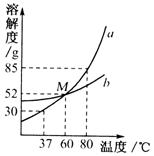
![]() (1)M点的含义为
(1)M点的含义为
(2)要想从b物质的溶液中获得较多b晶体,
![]() 最好用
法。
最好用
法。
(3)在80℃时,将15g a物质投入50g水中,
![]() 得到的溶液是否饱和?
,若不饱和,
得到的溶液是否饱和?
,若不饱和,
可用什么方法使其变为饱和溶液?请说出两种
具体的方法:
![]() ①
;
①
;
![]() ②
。
②
。
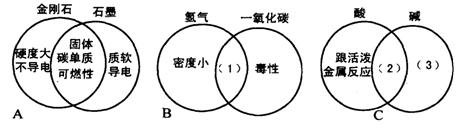 17.(6分)下图A是一种用于显示事物异同点的信息处理方法。两个圆分别代表金刚石和石墨的有关信息,两圆重叠的区域表示金刚石和石墨的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点)。请你在下图的空格内填写与图B、图C中(1)、(2)、(3)区域对应的适当内容(每处只要求填一点)。
17.(6分)下图A是一种用于显示事物异同点的信息处理方法。两个圆分别代表金刚石和石墨的有关信息,两圆重叠的区域表示金刚石和石墨的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点)。请你在下图的空格内填写与图B、图C中(1)、(2)、(3)区域对应的适当内容(每处只要求填一点)。
![]()
![]()
![]() (1)_______________ (2)______________ (3)_____________
(1)_______________ (2)______________ (3)_____________
![]() 18.(8分)化学与我们的生产密切相关,请试用所学过的化学知识解释下列现象或做法的原因(用化学方程式表示):
18.(8分)化学与我们的生产密切相关,请试用所学过的化学知识解释下列现象或做法的原因(用化学方程式表示):
![]() (1)人的胃液中含有少量盐酸,服用含少量细铁粉的补血药品,能治疗缺铁性贫血_____
(1)人的胃液中含有少量盐酸,服用含少量细铁粉的补血药品,能治疗缺铁性贫血_____
(2)食品包装袋中的干燥剂(主要成分是氧化钙)有防潮作用___________
![]() (3)用石灰浆粉刷墙壁,在一段时间内墙壁会“出汗”_______
(3)用石灰浆粉刷墙壁,在一段时间内墙壁会“出汗”_______
![]()
(4))胃痛时吃几块苏打饼干(含纯碱)可减轻胃痛,_______
三( 18分 )
19.(6分)完成下列各实验装置中所发生反应的化学方程式:


![]()
![]()
![]() (1)
(2) (3)
(1)
(2) (3)
(1) 。(2) 。(3) 。
20.(8分)A~D都是初中化学中的常见物质,C常温下是气态,且如图所示转化关系(反应条件、其他反应物及其他生成物均已略去):
写出下列物质的化学式: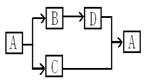
![]()
![]()
![]()
![]() A
;B ;C ;D
。
A
;B ;C ;D
。
21.(4分)李同学用实验探究Fe、Mg、Cu等三种金属活动性顺序时,有关反应记录如下:
![]()
![]()
![]()
![]() Cu与盐酸HCl不反应
Cu与盐酸HCl不反应
(1)从上述反应中,可获取的信息有:____________
![]()
![]() (2)李同学说,能从实验过程中发现镁比铁活泼,其依据是_________。如果补充一个实验(用化学方程式表示)________,也能说明镁比铁活泼。
(2)李同学说,能从实验过程中发现镁比铁活泼,其依据是_________。如果补充一个实验(用化学方程式表示)________,也能说明镁比铁活泼。
![]() (3)我们能用金属活动性顺序解释生活中的一些现象,如_______________。
(3)我们能用金属活动性顺序解释生活中的一些现象,如_______________。
四、实验题 (16分)
22.(7分)根据提供的仪器连接装置,只需写出使用仪器的编号。
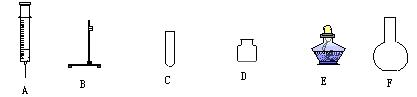
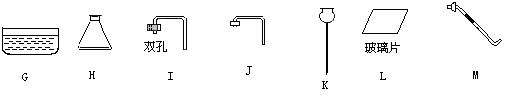
例:用排水法收集气体的装置:DMGL ;
![]()
![]() (1)写出出仪器名称:B
D
。
(1)写出出仪器名称:B
D
。
![]() (2)用排空气法收集气体的装置:
。
(2)用排空气法收集气体的装置:
。
![]() (3)实验室用高锰酸钾制取氧气的发生装置:
;实验室用过氧化氢和二氧化锰制取氧气的发生装置:
,其反应的化学反应方程式是________。
(3)实验室用高锰酸钾制取氧气的发生装置:
;实验室用过氧化氢和二氧化锰制取氧气的发生装置:
,其反应的化学反应方程式是________。
![]()
![]()
![]()
![]()
![]()
![]() 23.(9分)(1)实验室用石灰石与稀盐酸制取二氧化碳的发生装置可组合三套:
、
、
。 其反应的化学反应方程式是 。
23.(9分)(1)实验室用石灰石与稀盐酸制取二氧化碳的发生装置可组合三套:
、
、
。 其反应的化学反应方程式是 。
![]() (2)如何检验二氧化碳是否收集满了:
。
(2)如何检验二氧化碳是否收集满了:
。
五、计算题(13分)
| 盐 酸 体积:500mL |
![]() 24.实验室保存的一瓶浓盐酸,瓶上标签的部分内容如下图所示,请你根据标签上提供的数据解答下列问题。(计算结果精确到0.01)
24.实验室保存的一瓶浓盐酸,瓶上标签的部分内容如下图所示,请你根据标签上提供的数据解答下列问题。(计算结果精确到0.01)
(1) 瓶内浓盐酸的质量是__________。
![]() (2)用10mL浓盐酸可以配制溶质的质量分数为10%的盐酸溶液
(2)用10mL浓盐酸可以配制溶质的质量分数为10%的盐酸溶液
___________g
![]() 25. 把7g含杂质的锌片(杂质不与硫酸反应,也不溶于水)放在100g稀硫酸中 ,恰好完全反应。反应后得到的混合物总质量是106.8g。
25. 把7g含杂质的锌片(杂质不与硫酸反应,也不溶于水)放在100g稀硫酸中 ,恰好完全反应。反应后得到的混合物总质量是106.8g。
(1) ![]() 根据_______________定律,反应后生成的氢气质量是_______g。
根据_______________定律,反应后生成的氢气质量是_______g。
(2) 求原硫酸溶液的溶质质量分数。
2006年高要市初三化学模拟考试答案:
一、选择题(28分)1.B 2.A 3.B 4.C 5.D 6.C 7.B 8.D 9.A 10.D 11.A 12.B 13.B 14.A
二、填空题(25分)
15.(7分)(1)①、④、⑤、①②③ (2)④⑤ (3)① 以防除去水垢后CH3COOH腐蚀铝壶
16.(4分)(1) 60℃时a、b两物质的溶解度相等
(2)蒸发结晶 (3)不饱和,①再加入27.5g固体a ②降温至37℃
17. (6分)
(1)还原性,可燃性、双原子分子、气体、难溶于水等(叙述合理、正确均可)
(2)都是化合物、都能发生复分解反应、都能跟某些盐反应、都含有氢元素等
(3)与酸性氧化物反应、与酸反应、水溶液可使指示剂变色等
18.(8分)(每小题2分)略
三( 18分 )
19.(6分)每个化学方程式2分。所写化学方程式与实验装置中的反应不对应的不给分。答案略。
20.(8分)每空1分。只要答案合理均给分。
A.CaCO3 B.CaO C.CO2 D.Ca(OH)2或
A.H2O B.O2 C.H2 D.CuO等
21.(4分)(1)可获取的信息有:Mg、Fe均可与盐酸反应放出H2;Fe的金属活动性比Cu强;Cu不能与盐酸反应。
(2)Mg与HCl反应放出H2的速率比Fe大。![]() ;
;
(3)用Fe与CuSO4反应来冶铜。(每空格一分)
四、实验题 (16分)
![]() 22.(7分)(1)铁架台 集气瓶 (2)DJL (3)BCEM ;HIK(或BCJ、FAJ等,其它合理的答案均给分), 2H2O2
2H2O + O2↑
22.(7分)(1)铁架台 集气瓶 (2)DJL (3)BCEM ;HIK(或BCJ、FAJ等,其它合理的答案均给分), 2H2O2
2H2O + O2↑
23.(9分)(1)BCJ、HIK、FIK(或DIK)
CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ (化学方程式每一条2分,其余每空格一分)
(2)燃着的木条放在集气瓶的瓶口,木条熄灭了说明满了,否则不满。
用注射器缓缓注入稀盐酸,控制盐酸加入的速率从而控制产生气体的气流。
四、计算题(13分)
24、 (6分)(1)595g (2)44.03g (每题3分)
25. (7分)(1)质量守恒定律 (2分) 0.2 g (2分) (2)9.8%(3分)