《酸、碱、盐》知识点归纳
一、酸
1. 酸的5条通性
①酸和各种指示剂和pH试纸反应
| 酸的名称 | 石蕊试液 | 红色石 蕊试纸 | 蓝色石 蕊试纸 | 酚酞试液 | 白色酚 酞试纸 | pH试纸 |
| 盐酸 | ||||||
| 稀硫酸 | ||||||
| 碳酸 |
【浓硫酸具有脱水性(化学性质),所以试纸变成黑色】
②酸+活泼金属→盐+氢气
(注意:活泼金属是指( );酸是指( )
写出铁钉和盐酸反应的方程式
为什么实验室一般用锌粒,而不用铁或者是镁来制取氢气?
③酸+碱→盐+水
(注意:本反应是复分解反应【基本反应类型】,且是中和反应【属于复分解反应】)
| 举例 | 有关的化学方程式 | 简答 |
| 在烧碱溶液中滴加盐酸溶液 | 反应的基本类型: | |
| 在石灰水中滴加过量的硫酸溶液 | 如果在石灰水中预先滴加石蕊试液,可以看到颜色的变化是:
| |
| *在氢氧化铜中滴加硝酸溶液 | 可以看到的实验现象是:
| |
| *在氢氧化铁中滴加硝酸溶液 | 可以看到的实验现象是:
|
④酸+盐→新盐+新酸
| 举例 | 有关的化学方程式 | 简答 |
| 实验室制 取二氧化碳 | 反应的基本类型: | |
| 用氯化钡检验盐酸溶液和硫酸溶液 | 实验现象是:
| |
| 在硝酸银溶液中滴加盐酸 | 可以看到的实验现象是有白色沉淀,在滴加 沉淀不消失 | |
| 在碳酸钠溶液中滴加盐酸溶液 | 可以看到的实验现象是:
| |
| 在碳酸钡溶液中滴加硫酸溶液 | 可以看到的实验现象是:
|
⑤酸+碱性氧化物→盐+水
| 举例 | 有关的化学方程式 | 简答 |
| 用浓盐酸来 去除铁锈 | 实验现象: | |
| 用硫酸去 除氧化铁 | 反应前后铁元素的化合价 (变/不变) | |
| 在黑色氧化铜粉末中滴加硫酸 | 实验现象是 |
2.其他
①物理性质
| 名称 | 颜色 | ▲导电性 | 状态 | 挥发性 | 脱水性、吸水性 |
| 浓盐酸 | 无色 工业盐酸:黄 | 有 | 只有( )强调脱水性和吸水性 | ||
| 硫酸 | 无色 | ||||
| 浓硝酸 |
【浓硫酸具有吸水性所以可以作为许多气体干燥剂,但是浓硫酸不能干燥( )】
②用途
| 物质 | 用途 |
| 盐酸 | 制药、去除铁锈、制染料、味精、葡萄糖等 |
| 硫酸 | 去除铁锈、制化肥、农药和炸弹等 |
《酸、碱、盐》知识点归纳
二、碱
1.碱的4条通性
①酸和各种指示剂和pH试纸反应
| 碱的名称 | 石蕊试液 | 红色石 蕊试纸 | 蓝色石 蕊试纸 | 酚酞试液 | ▲白色酚 酞试纸 | pH试纸 |
| 氢氧化钠 | ||||||
| 氢氧化钙 | ||||||
| *氢氧化钾 |
②酸+碱→盐+水
(注意:本反应是复分解反应【基本反应类型】,且是中和反应【属于复分解反应】)
| 举例 | 有关的化学方程式 | 简答 |
| 在火碱溶液中滴加硫酸溶液 | 反应的基本类型: | |
| 在石灰水中滴加过量的盐酸溶液 | 如果在此石灰水中预先滴加酚酞试液,反应后,可以看到颜色的变化是: | |
| 在氢氧化铜中滴加硫酸溶液 | 可以看到的实验现象是:
| |
| *在氢氧化镁中滴加硝酸溶液 | 可以看到的实验现象是:
|
③碱+盐→新盐+新碱
| 举例 | 有关的化学方程式 | 简答 |
| 苏打溶液和石灰水反应 | 反应前后,溶液的pH值 (变大、变小、不变) | |
| 碳酸钾溶液和氢氧化钡溶液反应 | 在生成的白色沉淀中,再滴加硫酸溶液,可以看到 | |
| *硫酸铜溶液和氢氧化钾溶液反应 | 硫酸铜溶液是 色的。反应后,可以看到 | |
| 氯化铁溶液中滴加氢氧化钠溶液 | 实验现象是: | |
| *氯化镁溶液中滴加氢氧化钾溶液 | 在生成的白色沉淀中,再滴加硫酸溶液,可以看到 |
④碱+酸性氧化物→盐+水
| 举例 | 有关的化学方程式 | 简答 |
| 实验室用石灰水检验二氧化碳 | 实验现象是: | |
| 实验室用苛性钠吸收二氧化碳 | 反应后,得到的盐溶液的pH (<7/ =7/ <7) | |
| 工业上常用氢氧化钠吸收二氧化硫 | 二氧化硫是一种引起 的物质 |
2.其他
①物理性质
| 名称 | 颜色 | 潮解 | ▲导电性 | 密度 |
| 氢氧化钠 | 固体:白色 溶液:无色 | 固体:有 溶液:没有 | 导电 | 比水的密度大 |
| 氢氧化钙 | 无 | |||
| *氢氧化钾 |
【氢氧化钠能够潮解,所以可以作为许多气体干燥剂,但是它不能干燥酸性的气体,如:( 、 、 、 、 、 )等】
②用途
| 物质 | 用途 |
| 氢氧化钠 | 制皂、炼铝、造纸、精炼石油等 |
| 氢氧化钙 | 建筑、改良酸性土壤、配制波尔多液、制造漂粉精等 |
《酸、碱、盐》知识点归纳
三、几种重要的盐
| 物质 | 俗称 | 物理性质 | 化学性质 | ||
| 固体颜色 | 溶液颜色 | 溶解性 | |||
| 氯化钠NaCl | ① 氯化钠可以和硝酸银反应方程 ( ) ②电解饱和氯化钠溶液可以得到氢氧化钠、氢气和氯气 | ||||
| 碳酸钠 Na2CO3 | ① 石碱化学式: ② 碳酸钠溶液是( )性的,pH( )7 ③ 碳酸钠可以和酸反应 HCl+ Na2CO3→ 碳酸钠可以和石灰水(碱)反应 ( ) ④ 碳酸钠可以和氯化钙(盐)反应 ( ) | ||||
| 碳酸钠晶体 Na2CO3•10H2O | |||||
| 硫酸铜 CuSO4 | ① 无水硫酸铜检验水方程式 ( ) (实验现象: ) ② 硫酸铜晶体加热分解方程式 ( ) (反应基本类型: ) ③ 硫酸铜和铁反应方程式 ( ) (可用于去除硫酸亚铁中含有少量的硫酸铜) ④ 硫酸铜和碱反应 CuSO4+ Ba (OH)2→ (此化学方程式可用于除去硫酸铜) CuSO4+NaOH→ 硫酸铜和氯化钡(盐)反应 ( ) | ||||
| 硫酸铜晶体 CuSO4•5H2O | |||||
【注意:氯化钠的溶解度受温度影响( )大,因此要得到氯化钠晶体,可以采用(
)结晶的方法;硝酸钾的等物质的溶解度受温度影响( )大,因此可以采取(
)的方法】结晶
初中化学知识整理
1、 物质的颜色
| 物质 | 颜色 | 物质 | 颜色 | 物质 | 颜色 |
| 硫酸铜溶液 | 氯化铜溶液 | 硝酸铜溶液 | |||
| 硫酸铁溶液 | 氯化铁溶液 | 硝酸铁溶液 | |||
| ▲硫酸亚铁溶液 | 氧化镁 | 四氧化三铁 | |||
| 氧化铁 | 氧化铜 | 二氧化锰 | |||
| 氢氧化铁 | 氢氧化铜 | 氢氧化镁 | |||
| 硫酸铜粉末 | 硫磺 | 红磷 |
2、物质在空气中长期露置,请判断可能发生的变化(变大、不变、变小)
| 物质 | 质量 | ▲溶液密度 | 变化 | 溶液浓度 | 原因 |
| 浓盐酸 | 变 | 变 | ( )变化 | 变小 | 盐酸具有( )性,挥发出( )气体 |
| 浓硫酸 | 变 | 变 | 变小 | 浓硫酸具有( )性 | |
| 氢氧化钠(固体) | 变 | / | 化学变化 | / | ① 固体氢氧化钠能够( ),所以其表面会“出汗” ② 固体氢氧化钠还会和空气中的( )反应,方程式: |
| 生石灰 | 变 | / | / | ①生石灰会和空气中的( )反应,生成( ) ②熟石灰会继续和( )反应 | |
| 石灰水 | 溶液质量 变 | 变 | 变小 | 石灰水会和二氧化碳反应 | |
| 石碱 | 变 | / | / | 石碱会( ) | |
| 无水硫酸铜 | 变 | / | / | 无水硫酸铜会吸收空气中的水(颜色由( )色变成( )色) |
3、 检验气体
检验气体
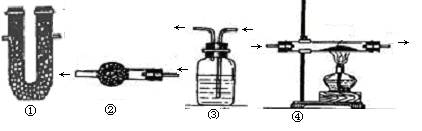
仪器名称:①U型管②干燥管③洗气瓶(“多功能瓶”)④硬质玻璃管
| 物质 | 选用试剂和装置 | 化学方程式 |
| 水蒸汽 | ①或者②中放无水硫酸铜 | |
| 氢气 | ④中放氧化铜+ ①或者②中放无水硫酸铜 | |
| 二氧化碳 | ③中石灰水 | |
| 一氧化碳 | ④中放氧化铜+③中石灰水 | |
| 氯化氢气体 | ③中硝酸银溶液 |
4、去除杂质(气体)

仪器名称:①U型管②干燥管③洗气瓶(“多功能瓶”)④硬质玻璃管
| 物质 | 选用试剂和装置 | 化学方程式 |
| 氧气 | ④中放铜粉或者用铜网 | |
| 水蒸汽 | ①或者②中放固体氢氧化钠或碱石灰或者③中浓硫酸(最常用) | |
| 氢气 | ④中放氧化铜 | |
| 二氧化碳 | ①或者②中放固体氢氧化钠或碱石灰//③中氢氧化钠溶液 | |
| 一氧化碳 | ④中放氧化铜 |
5、检验物质
| 被检验物质 | 选用的试剂 | 现象 | 有关的化学方程式 |
| 碳酸盐 | ①酸 | 气泡 | 例如:2HCl+ Na2CO3→2NaCl+ H2O +CO2↑ |
| ②氢氧化钙或氢氧化钡 | 白色沉淀 | 例如:Na2CO3+Ba(OH)2→BaCO3↓+2NaOH K2CO3+Ca(OH)2→CaCO3↓+2KOH | |
| ③可溶性的钡盐或者钙盐 | 例如:Na2CO3+BaCl2→BaCO3↓+2NaCl Na2CO3+CaCl2→CaCO3↓+2NaCl | ||
| 硫酸盐 | 钡盐 (再滴加稀酸) | 白色沉淀 (不消失) | 例如:Na2SO4+BaCl2→BaSO4↓+2NaCl |
| 盐酸盐 | 硝酸银 (再滴加稀酸) | 白色沉淀 (不消失) | 例如:AgNO3+NaCl→NaNO3+AgCl↓ |
| ▲铵盐 | 可溶性碱 | 刺激性 气味 | 例如:NH4Cl+NaOH→NaCl+NH3↑+ H2O |
6、物质的溶解性
① 可溶性碱:化学式( )
② 可溶性盐:
7、有关物质的酸碱性
一般而言,酸溶液是酸性的(pH<7);大多数的盐溶液是中性的(pH=7);碱溶液是碱性的(pH>7)。
【但是,在初中阶段学生还必须掌握①碳酸钠溶液②草木灰:主要成分是( )的水溶液是( )性的pH( )7,能够使酚酞试液变( )色,使紫色石蕊试液变( )色】
8、化肥
①能够被植物所吸收的营养元素(比如:N、P、K等)主要是以化合态存在于盐中或者有机物中
②尿素是含氮量最高的氮肥
|
④碳铵的施用:不能在受热受潮下使用,原因是NH4HCO3→NH3↑+H2O+CO2↑(氮元素流失)
9、几种物质的俗称
| 物质 | 化学式 | 俗称 | 物质 | 化学式 | 俗称 |
| 氯化钠 | NaCl | 碳酸钠 | Na2CO3 | 、 | |
| 氢氯酸 | HCl | 碳酸钠晶体 | 纯碱晶体、石碱 | ||
| 氢氧化钠 | NaOH | 、 、 | 硫酸铜 | CuSO4 | 无水硫酸铜 |
| 氢氧化钙 | Ca(OH)2 | 固体: 、 溶液: | 硫酸铜晶体 | CuSO4•5H2O | 、 |