九年级科学第一学期期中测试卷
班级 姓名 学号
亲爱的同学,这份试卷将再次记录你的自信、沉着、智慧和收获,请认真审题,看清要求,仔细答题,祝你成功!
本卷可能用到的相对原子质量:H—1 C—12 Na—23 S—32 O—16 Cl—35.5 Ca—40 K—39 Ag—108 N—14 Mg—24 Fe—56
一、选择题(本题24小题,共48分)
1、张大伯为了庄稼生长茂盛,茎杆粗壮,增强抗病虫害能力,需要施肥,下列物质属于钾肥的是( )
A.NH4HCO3 B.Ca(H2PO4)2 C.K2CO3 D.CO(NH2)2
2、某餐厅发生食物中毒现象,经调查原来是厨师以为盐就是食盐,因而误食了用毒工业用盐亚硝酸钠(NaNO2)。其实,盐是一大类物质,以下属于盐的是( )
A.纯碱 B.熟石灰 C.生石灰 D.干冰
3、我们学过的氢气、一氧化碳、碳三种物质的共同点是( )
A.都具有可燃性和还原性 B.都是单质
C.在一定条件下都能与二氧化碳起反应 D.燃烧时都生成二氧化碳
4、盛放在油罐车内的石油产品振荡时会产生静电,容易引起火灾或爆炸,所以油罐车尾部有一条拖地的铁链,这是利用了铁的什么性质( )
A.导热性 B.导电性 C.可燃性 D.延展性
5、一般在白蚂蚁的高发地区,白蚂蚁会蛀蚀木头,它分泌的蚁酸是一种酸,还能腐蚀很多建筑材料。下列建筑材料最不容易被白蚂蚁腐蚀的是 ( )
A.大理石 B.钢铁 C.陶瓷 D.铝合金
6、要除去氯化钠溶液中少量的碳酸钠,可加入适量的 ( )
A.石灰水 B.氯化钾溶液 C.硝酸 D.氯化钙溶液
7、小白同学为了区别氢氧化钠溶液和澄清石灰水,设计了如下图所示的四组实验方案,其中能达到目的的是( )
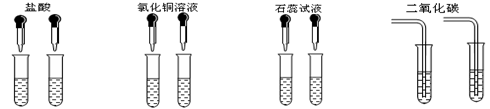 |
A B C D
8、纯碱是最重要的基础化工原料之一,被称为“化工之母”,其产量和消费量通常被作为衡量一个国家工业发展水平的标志之一。下列物质中不能与纯碱反应的是( )
A.稀硫酸 B.铁 C.石灰水 D.氯化钙
9、几年前,我国某集团花巨资购回在八国联军火烧圆明园时流失海外的国宝:铜铸的牛首、猴首和虎首,它们都是由含一定比例金、银、锡、锌的铜合金铸造的。铜合金属于( )
A.金属材料 B.无机非金属材料 C.合成材料 D.复合材料
![]() 10、“自主创新”是我国十一发展规划中提出的重大国策。经我国科学家的努力,已研制出具有自主知识产权的国产芯片—“龙芯一号”和“龙芯二号”,其芯片的核心部件是以高纯硅单质为原料制成的,用化学方法制备高纯硅的反应原理是: SiCl4
+ 2H2 Si
+ 4HCl,该反应属于( )
10、“自主创新”是我国十一发展规划中提出的重大国策。经我国科学家的努力,已研制出具有自主知识产权的国产芯片—“龙芯一号”和“龙芯二号”,其芯片的核心部件是以高纯硅单质为原料制成的,用化学方法制备高纯硅的反应原理是: SiCl4
+ 2H2 Si
+ 4HCl,该反应属于( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
11、学校实验室有四个药品橱分别存放了如下药品:
| 药品橱 | 甲 | 乙 | 丙 | 丁 |
| 药品 | 锌、铜 | 硫酸钠 | 氢氧化钠 | 盐酸 |
| 铁、镁 | 碳酸钠 | 氢氧化钾 | 稀硫酸 |
该实验室购进了两瓶无水氯化钙,应将它放在( )
A.甲橱 B.乙橱 C.丙橱 D.丁橱
12、在下列盐的水溶液中,若滴入氢氧化钠溶液产生蓝色沉淀;若滴入硝酸银溶液观察不到明显现象,则这种盐是( )
A.氯化铁 B.硝酸钾 C.硝酸铜 D.氯化铜
13、铁是人类生活中非常重要的一种材料,工业上可用如下化学反应制得铁:
![]()
|
A.Fe2O3 B.CO C.Fe D.CO2
14、某工厂排出的废水显酸性,且含有毒的Cu2+离子,加入适量的下列物质可以回收铜,且能降低溶液酸性的物质是( )
A.食盐 B.铁粉 C.石灰石 D.胆矾
15、下列各选项中,括号内物质是去除杂质所用的试剂(适量),其中错误的是( )
A.CuSO4中混有NaCl(AgNO3溶液) B.铜粉中混有铁粉(盐酸)
C.H2中混有CO2(NaOH溶液) D.氯化亚铁溶液中混有氯化铜(铁粉)
16、某气体的成分可能含有H2、CO、N2、CH4中的一种或两种。该气体在足量的氧气中充分燃烧后,将全部生成物依次通过浓硫酸和氢氧化钠溶液,发现浓硫酸和氢氧化钠溶液的质量都增加,则该气体的成分不可能是( )
A.CH4 B.CO和N2 C.H2 和CO D.CO和CH4
17、信达学校化学兴趣小组,为验证Fe、Ag、Cu三种金属活动性顺序,设计了如图所示的4种实验方案。其中不能达到目的的是 ( )
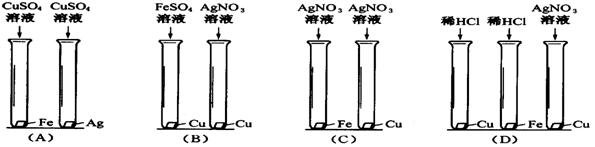 |
18、在相同条件下,H2S(氢硫酸)的酸性比H2SO3(亚硫酸)的酸性强,H2S(氢硫酸)是H2S(硫化氢)气体的水溶液,H2SO3(亚硫酸)是SO2与水反应后形成的溶液。在室温时,向饱和的H2SO3溶液中通入H2S气体,发生反应如下:2H2S+ H2SO3==3S↓+3 H2O。以下是向H2SO3溶液通入H2S的体积和溶液pH值关系图,正确的是( )
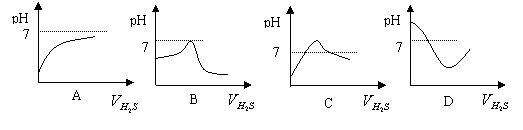 |
19、由石灰石和纯碱制烧碱,要经历下列几步反应:CaCO3====CaO+CO2,CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。在这些反应所属类型里,不包含 ( )
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
20、在已调平衡的托盘天平两边各放一个等质量的烧杯,向烧杯中各倒入质量相等、质量分数也相等的足量的稀硫酸,分别在左、右两盘的烧杯中同时放入等质量的金属粉末X、Y。观察到从反应开始后至反应结束托盘天平的指针始终偏向左边。则金属X、Y分别是 ( )
A.X :Al Y:Fe B.X :Zn Y:Fe
C.X :Zn Y:Al D.X :Fe Y:Zn
21、四位同学分别用下列四种方法检验NaOH溶液是否已变质含有Na2CO3,(1)加少量稀盐酸,无气泡放出,则一定不含Na2CO3(2)加少量澄清石灰水,有沉淀生成,则一定含有Na2CO3(3)加少量CaCl2溶液,有沉淀生成,则一定含有Na2CO3(4)加少量BaCl2溶液有沉淀生成,则一定含有Na2CO3,其中方法和结论都正确的是: ( )
A.(1)(2) B.(1)(2)(3) C.(2)(3)(4) D. (1)(2)(3)(4)
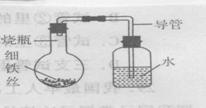 22、小刘同学将沾有清水的细铁丝放在右图的装置中,
22、小刘同学将沾有清水的细铁丝放在右图的装置中,
经过数小时后能观察到的现象是( )
A、铁丝不变,导管中水面上升 B、铁丝不变,导管中水面不变
C、铁丝生锈,导管中水面上升 D、铁丝生锈,导管中水面不变
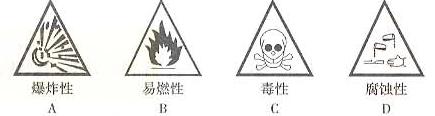
23、下列是一些常用的危险图标,装运浓硫酸的箱子应贴的图标是( )
24、以下对科学事实的归纳和总结,你认为正确的是 ( )
A、置换反应不一定要在溶液中发生 B、碱能跟一切非金属氧化物起反应
C、酸能跟所有盐起反应 D、酸跟活泼金属反应一定生成盐和氢气
二、简答题(每空2分,共20分)
25、小芳同学想要验证Fe、Cu、Ag三种金属的金属活动性顺序,他选择了Cu、Ag 和FeSO4溶液,结果实验得不到他想要的结果,你能在他原来的方案上改动一种试剂,帮他完成实验吗?________________________________________________。
26、“珍爱生命,拒绝毒品”是每个公民的责任,但是在某些娱乐场所,还有人服用俗称摇头丸的毒品。该毒品能使人手舞足蹈,呈癫狂状态,严重危害人的身心健康和社会稳定,有一种“摇头丸”的化学式为C12H xO2N,相对分子质量为209,试回答下列问题:
(1)该物质属于 (填“有机化合物”或“无机化合物”)
(2)该物质的一个分子中,含氢原子 个。
(3)该物质中碳元素与氧元素的质量比为 。(最简整数比)
27、商店门牌上装潢的鎏金大字,不少是由黄铜做的。黄铜是铜和锌的合金,它可用来制造机器、电子零件及日常用品。由于外形很象黄金,所以常被不法分子用来冒充黄金进行诈骗活动。为了鉴别黄铜和黄金,你想到用哪种方法呢?(写出一种方法即可)________________________
28、现有含铁的质量分数为50%的赤铁矿1000吨,可制得 含铁96%的生铁_____________吨(保留一位小数)。
29、有三种白色粉末分别是碳酸钙、碳酸钠和无水硫酸铜,要将它们一次区分开来,最简单的方法就是用_____________。
 30、某初中学生在帮助老师准备实验时,发现了一瓶失去标签的黑色粉末和一瓶标签破损(如图38)的无色液体。询问老师得知,该实验室的黑色粉末只有氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉五种可能。为了鉴定这两种试剂,该同学将黑色粉末与无色液体混合,发现立即产生气泡。
30、某初中学生在帮助老师准备实验时,发现了一瓶失去标签的黑色粉末和一瓶标签破损(如图38)的无色液体。询问老师得知,该实验室的黑色粉末只有氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉五种可能。为了鉴定这两种试剂,该同学将黑色粉末与无色液体混合,发现立即产生气泡。
(1)请你根据上述信息,作出关于黑色粉末和无色液体可能成分的猜测:
| 黑色粉末 | 无色液体 | |
| 猜测 |
(2)做出上述猜测的理论依据是(化学方程式)
三:分析题:(每空2分,共20分)
31、某同学对一种无色溶液进行鉴定实验,试根据他实验报告中的步骤和现象,填写相应的实验结论。(该溶液只含一种溶质)
| 实验步骤 | 实验现象 | 结 论 |
| a. 取该溶液少许,向其中加几滴紫色石蕊试液 | 溶液变红色 | 该溶液一定显 性 |
| b. 再取该溶液少许,向其中加入硝酸银溶液,再加入足量的稀硝酸 | 有白色沉淀生成,该沉淀不溶于稀硝酸 | 白色沉淀为 说明该溶液为 |
32、氯化铁是一种良好的净水剂,化学上可以用多种方法来制取。请写出四种用铁的化合物通过一步化学反应制取氯化铁的三个化学方程式:
① ②
③
(注:碳酸铁不要作为反应物)
33、我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。他以食盐、水、氨气、二氧化碳为原料,先制得碳酸氢钠和氯化铵,进而生产出纯碱。右表是几种物质在不同温度时的溶解度:
| 0℃ | 20℃ | 40℃ | 60℃ | |
| NaHC03 | 6.9 | 9.6 | 2.7 | 6.4 |
| NaCl | 35.7 | 35.8 | 6.6 | 37.3 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 |
(3)“侯氏制碱法”制NaHC03的方程式是NaCI+C02+NH3+H20=NaHC03+NH4Cl,该反应能进行的原因是碳酸氢钠的溶解度很小,在溶液中析出沉淀,进而生产出纯碱属于________(填酸、碱、盐),它的浓溶液与澄清石灰水反应的化学方程式为______________________________________。
34、食品的包装袋内常放入一小包干燥剂,其主要成分为生石灰,干燥袋上都有“请勿食用”字样。(1)“请勿食用”是因为干燥剂食用后,对人体有 作用。
(2)写出干燥剂的主要成分吸水过程中发生反应的化学方程式: 。
四、分析、计算题(本题共2小题,35小题6分,36小题 6分,共12分)
 35、精盐(NaCl)和纯碱(Na2CO3)是两种常见之物。
35、精盐(NaCl)和纯碱(Na2CO3)是两种常见之物。
(1)用化学方法区别这两种固体,可以选择下列哪一种物质?
答: A.白酒 B.米醋 C.纯净水 D.酱油
(2)王清华同学不慎在精盐中混入了少量纯碱,他想重新得到精盐,设计了以下两个实验方案:
 |
你认为合理的实验方案是
并说明另一方案不合理的理由
(3)假设(2)中固体混合物有53克,加入足量的稀盐酸充分反应后,生成4.4克二氧化碳气体,求该固体混合物中氯化钠的质量分数。
36.甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸反应,所得数据如下:
|
| 甲 | 乙 | 丙 | |||
| 取用金属混合物的质量(/g) | 10 | 10 | 20 |
| |
| 取用稀硫酸的质量(/g) | 100 | 120 | 100 |
| |
| 反应后过滤得到干燥固体的质量(/g) | 2 | 2 | 12 |
| |
计算:(1)金属混合物中铁的质量分数。
(2)甲 制得的硫酸亚铁的质量。
(3)该硫酸中溶质的质量分数。
科学答题卷 姓名 学号
一、选择题(本题有24小题,每小题2分,共48分。)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
| 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
|
|
|
|
|
|
|
|
|
|
|
|
|
二、简答题(每空2分,共20分)
25、________________________________________________
26、
(1) (2) (3)
27、________ ________________ 28、_____________29、_____________。
30、(1)
(2)(化学方程式)
三:分析题:(每空2分,共20分)
31、(1) (2) (3)
32、① ②
③ ④
(注:碳酸铁不要作为反应物)
33、__________________________________, ________ ______________________________________。
四、分析计算题(本题有2小题,共12分)
34、(1)
(2)
(3)
35、(5)
(6)
(7)
答案 姓名 学号
二、选择题(本题有24小题,每小题2分,共48分。)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| c | A | A | B | C | D | D | B | A | C | B | A |
| 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| A | B | A | B | C | B | C | C | C | C | A | A |
二、简答题(每空2分,共20分)
25、Ag改为AgNO3
26、
(1)有机化合物(2)19(3) 9:2
27、有稀盐酸检测,放出气体为黄铜 28、520。8 29、水
30、(1)铁 硫酸
(2)(化学方程式)略
三:分析题:(每空2分,共20分)
31、(1)酸 (2)氯化银 (3)盐酸
32、略
(注:碳酸铁不要作为反应物)
33、碳酸氢钠的溶解度很小,在溶液中析出沉淀。
四、分析计算题(本题有2小题,共12分)
34、(1) B
(2)方案一, 引入一种新的杂质硫酸钠
(3)80%
35、(5)无影响,稀释后溶质的质量不会减少。
(6)先向醋酸溶液里,滴加几滴无色酚酞,当最后加入一滴氢氧化钠时,溶液变为红色,说明恰好反应完全。
(7)5% 符合