初三科学上学期月考卷
石莉蔷
本卷可能用到:(1)相对原子质量H—1 C—12 O—16 Na—23
Cl—35.5 K—39 Ca—40 Cu—64 Zn—65 S —32
一、选择题(本大题共30小题,第1~10小题,每小题3分,第11~30小题,每小题2分,共70分。请选出一个符合题意的选项,不选、多选、错选均不给分)
1.下列各类食物中蛋白质含量最丰富的是( )




2.下列能由酸与金属直接反应制得的物质是( )
A.FeCl3 B.AlCl3 C.AgCl D.Cu Cl2
3.我省盛产茶叶,“太平猴魁”“黄山毛峰”等绿茶享誉海内外.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列关于单宁酸的说法不正确的是( )
A.由碳氢氧三种元素组成 B.一个分子含76个碳原子
C.碳氢氧原子个数比为76:52:46 D.一个分子中含23个氧分子
4.下列物质露置在空气中一段时间后质量增加且变质的是( )
A.浓硫酸 B.大理石 C.烧碱 D.浓盐酸
5.我们生活中常用到的下列物质属于有机合成材料的是 ( )
A.棉花 B.塑料 C.羊毛 D.天然橡胶
6.下列选项中物质的名称、俗名、化学式不完全一致的是( )
A.碳酸钠、纯碱、Na2CO3 B.氢氧化钠、石灰石、Ca(OH)2
C.氧化钙、生石灰、CaO D.氢氧化钠、烧碱、NaOH
7.我们常见的一些食物的近似pH范围如下:
| 食物 | 橘子汁 | 四川泡菜 | 牛奶 | 鸡蛋清 |
| 近似pH范围 | 3.0~4.0 | 3.2~3.6 | 6.3~6.6 | 7.6~8.0 |
则下列说法中,不正确的是 ( )
A. 鸡蛋清显碱性 B. 胃酸过多的人应少吃四川泡菜
C. 橘子汁不能使无色酚酞试液变红 D. 牛奶比鸡蛋清的碱性强
8.只用一种试剂就能方便地区分稀盐酸、蒸馏水、澄清的石灰水的是( )
A、酚酞溶液 B、石蕊溶液 C、二氧化碳 D、火碱溶液
9.把50g10%的氢氧化钠溶液稀释为4%的溶液,需要加入的水的质量为( )
A.50g B.75g C.100g D.150g
10.有A、B、C三种溶液,它们之间相互反应的现象如下:( )
A+B→有气体生成 A+C→无明显现象 B+C→有白色沉淀生成,则A、B、C 三种溶液可能是下列各组中的 ( )
A.HCl、NaOH和Na2CO3溶液 B.NaCl、Na2CO3和Ca(OH)2溶液
C.HCl、Na2CO3和CaCl2溶液 D.H2SO4、HCl和BaCl2溶液
11. 下列各组物质中,能在同一溶液里大量共存的是( )
A.Na2SO4 Ba(OH)2 HCl B.CuSO4 H2SO4 HNO3
C.FeCl3 NaOH Ca(OH)2 D.K2SO4 NaOH BaCl2
12. 下列供热方式,最有利于环境保护的是 ( )
A.用煤做燃料供热 B.用石油做燃料供热
C.用天然气或煤气做燃料供热 D.用太阳能供热
13.下列能正确表示加水稀释pH=10的NaOH溶液的是 ( )
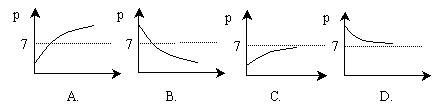
14.根据你的生活经验和所学化学知识判断,下列说法不正确的是 ( )
A.维生素、糖、蛋白质等都是对人类生命活动有重要意义的营养素
B.大多数有机物难溶于水,易溶于汽油、酒精、苯等有机溶剂
C.绝大多数有机物不易导电
D.有机物的熔点低,受热易分解,都能燃烧
15.下列实验操作正确的是 ( )
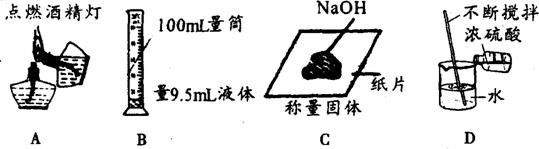
16.向一定量的Ba(OH)2溶液中逐滴加入稀H2SO4,下列图像中V表示加入稀H2SO4的体积,其中正确的是( )
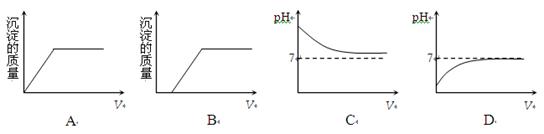
17.下列各组气体中均混有水蒸气,其中可以用固体氢氧化钠干燥的是 ( )
A.CO、H2、HCl B.SO2、CO2、HCl
C.H2、O2、N2 D.SO2、H2、CO
18.随着化学工业的发展,能源的种类也变得多样化起来。最近吉林市的小英家就使用上了天然气做饭,天然气的主要成分是 ( )
A.CO B.CO2 C.H2 D.CH4
19.下列物质中,溶于水不能放出大量热的是( )
A、生石灰 B、 NaOH 固体 C、浓硫酸 D、氢氧化钙
20.2007年第二期的《化学世界》杂志上报道了浙江大学化学工程研究所以丁铵(二正丁基二硫代磷酸铵)和氯化锌为原材料合成二正丁基二硫代磷酸锌(ZBPD)的文章,该反应的原理可以用下式表示。该反应属于( )
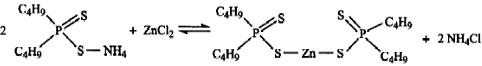
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
21.欲除去括号内的少量杂质,选用试剂不正确的是 ( )
A.NaOH溶液(Na2CO3)选用稀盐酸 B.C(CuO)选用稀硫酸
C.NaCl溶液[Ba(OH)2]选用硫酸铜溶液 D.MnO2(KCl)选用水
22.对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )




A B C D
23.明明到医院检查完身体后,医生建议他多吃水果和蔬菜,请你判断医生让他主要补充 ( )
A.蛋白质 B.糖类 C.油脂 D.维生素
24.5克食盐加入到100克水中并充分搅拌,所得溶液的质量分数( )
A.=5% B.<5% C.>5% D.不能确定
25.鱼胆弄破后,会使鱼肉粘上一种叫胆汁酸(一种酸)的难溶于水物质,使鱼肉变苦,要消除这种苦味,可用下列的何种溶液冲洗最适宜( )
A. 食盐水 B. 醋酸 C. 纯碱溶液 D. 氢氧化钠溶液
26.溶液在稀释前后保持不变的是 ( )
A.溶质的质量分数 B.溶质的质量
 C.溶液的质量 D.溶剂的质量
C.溶液的质量 D.溶剂的质量
27.现有一种物质分子的模型如右图,则下列说法正确的是 ( )
A.该物质不是有机物 B.该物质的化学式为 C2H6O
C.该物质不是可燃物 D.大量饮用该物质对人体有益
28.下列是关于粗盐提纯实验的几种说法,其中正确的 ( )
A.为加快过滤速度,应用玻璃不断搅拌过滤器中的液体
B.如果经两次过滤,滤液仍浑浊,则应检查实验装置并分析原因
C.蒸发滤液时,要用玻璃棒不断搅拌,用酒精灯持续加热,直到蒸干为止
D.蒸发完毕后,待其冷却,由于食盐无毒,可用手指将食盐转移到纸上称量
29.为完全中和某盐酸溶液,需a克质量分数为4%的NaOH溶液。如果改用a克质量分数为4%的KOH溶液,反应后溶液的PH值为……………( )
A、大于7 B、小于7 C、等于7 D、无法判断
30.从100 mL溶质的质量分数为 10%的硫酸溶液中倒出 20 mL,剩下的溶液中溶质的质量分数( )
A.8% B.10% C.12.5% D.80%
二、简答题(本大题共8小题,每空2分,共50分)
31.用Na、H、O、S四种元素中的若干种,写出下列物质的化学式:
(1)一种酸 ;(2)一种盐 ;(3)一种碱 ;
32.纯碱(Na2CO3)是厨房中常用的物质,以下是有关纯碱性质的描述:①是白色粉末状物质,②易溶于水,③不小心掉入食醋中会有大量气泡产生。其中,属于物理性质的是 ,属于化学性质的是 。(填序号)
33.用化学反应方程式说明下列事实:
(1)电镀厂常用稀硫酸除去铁锈: ;
(2)锅炉中的水垢(主要成分为CaCO3)可用稀盐酸清除: ;
(3)医药用的氢氧化铝乳剂可用来治疗胃酸(盐酸)过多: 。
34.在我国推广使用“清洁燃料”的过程中,2005年5月16日上海交通大学宣布:我国首台使用二甲醚为燃料的城市客车问世,这将有效地解决公交车冒黑烟的问题。
(1)已知二甲醚的化学式为C2H6O,二甲醚的式量 ;
![]() (2)二甲醚在空气中完全燃烧生成二氧化碳和水,完成有关反应的化学方程式:
(2)二甲醚在空气中完全燃烧生成二氧化碳和水,完成有关反应的化学方程式:
C2H6O + 3O2 ;
(3)从上述反应可见,二甲醚和天然气一样属于 能源。
35.某些植物的花汁可作酸碱指示剂。取三种花汁用稀酸溶液或稀碱溶液检验,颜色如下:
| 花种类 | 花汁在酒精(中性)中颜色 | 花汁在稀酸中颜色 | 花汁在稀碱中颜色 |
| 玫瑰花 | 粉红 | 粉红 | 绿 |
| 万寿菊花 | 黄 | 黄 | 黄 |
| 大红花 | 粉红 | 橙 | 绿 |
试回答下列问题:
(1)为试验生活中的食盐水、肥皂水、汽水、石灰水四种物质的酸碱性,我选择 花汁,不选用其他花汁的原因是 。
(2)取所选花汁少许分别滴入上述四种物质,请将所显颜色填入下表中:
| 试验物质 | 食盐水 | 肥皂水 | 汽水 |
| 所显颜色 |
|
|
|
36.(6分)味精是烹制菜肴时常用的调味品,其主要成分是谷氨酸钠,谷氨酸钠有鲜味,易溶于水。小靖发现某品牌味精包装上标注:“谷氨酸钠含量≥80%,NaCl≤20%。”他想测定此味精中NaCl的含量(谷氨酸钠的存在不影响NaCl的性质)。
(1) 下面是他所做实验的有关步骤,请补全实验步骤②。
① 称取该味精样品5.0g,并溶于蒸馏水;
② 加入过量的___________溶液; ③ 过滤;
④ 用蒸馏水反复洗涤沉淀多次;
⑤ 将沉淀烘干、称量,测得固体质量为2.87g。
(2) 根据上述实验步骤回答下列有关问题:
① 过滤操作所需要的仪器除烧杯、铁架台(带铁圈)、玻璃棒外,还需要_________________________________________________。
② 检验沉淀是否洗净的方法是_________________________。
③ 此样品中NaCl的质量分数为___________,是否符合其包装上标注的标准?_________________________________。
37.在煤气中加入的少量有特殊气味的乙硫醇(C2H5SH)也可以燃烧,其反应的化学方程式为2C2H5SH+9O2 ![]() 4CO2+2X+6H2O,则x的化学式是
4CO2+2X+6H2O,则x的化学式是
38.为了除去氯化钠样品中的碳酸钠杂质,兴趣小组最初设计了如下的方案并进行实验。


(1)写出沉淀A的化学式 。
(2)加入CaCl2溶液后,分离除去沉淀A的实验操作方法是 。
(3)同学在实验过程中,又发现了新的问题:此方案很容易引入新的杂质,请写出固体物质B的成分 (用化学式表示)。
三、分析计算题(本大题共3大题,每小题10)
39.将25 g石灰石(主要成份是 CaCO3)放入73 g稀盐酸中(石灰石中的杂质不跟盐酸反应,也不溶于水)恰好完全反应,生成8.8 g二氧化碳气体。
试求:(1)石灰石中碳酸钙的质量分数;
(2)稀盐酸中溶质的质量分数;
(3)反应后溶液中溶质的质量分数。
 40.实验室中浓硫酸的商标如右图所示。请根据有关信息计算:
40.实验室中浓硫酸的商标如右图所示。请根据有关信息计算:
(1)该试剂瓶中硫酸溶液的质量是
(2)欲配制100g溶质质量分数为19.6%的稀硫酸,需这种浓硫酸多少克?
(3)取足量的稀硫酸与6.5 g锌充分反应,可制得氢气多少克?
41.某石化厂有一种石油产品含有质量分数为4.9%的残余硫酸,过去他们都是用NaOH溶液来清洗这些硫酸。请计算:
(1)若要清洗100kg的这种石油产品,需要多少千克的NaOH?
| 名 称 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 6.00 | 24.00 |
(2)改石化厂进行了技术改造,采用Ca(OH)2中和这些残余硫酸。每处理100kg这种产品,可以节约多少经费?NaOH和Ca(OH)2的市场价格如下表:
44. (6分)(1) AgNO3溶液
(2) 漏斗
(3) 取少量最后一次洗涤后的液体,加入稀盐酸或NaCl溶液,若无白色沉淀生成,证明沉淀已洗净
(4) 23.4﹪ , 不符合
(5) 使用时应避免酸性较强和碱性较强条件下使用, 避免在温度过高条件下使用