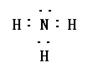高中毕业班化学质量检查试卷Ⅰ
化 学 试 题
本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分108分,考试时间60分钟。
相对原子质量:H 1 C 12 N 14 O 16 C1 35.5 Mg 24 A1 27
第Ⅰ卷
一、选择题(本题包括8小题,每小题只有一个选项符合题意)
6.下列应用与胶体性质无关的是 ( )
A.血液透析 B.盐酸除锈 C.明矾净水 D.电泳提纯
7.下列说法正确的是 ( )
A.1LO2的质量一定比1LC12的质量小 B.1.8gH2O所含电子数为0.1NA
C.等质量的NO2和N2O4所含原子数一定相等
D.等体积、等物质的量浓度的强酸溶液中所含的H+离子数一定相等
8.某c(H+)=1×10-2mol・L-1的溶液中含有大量NO3-、SO42-,该溶液中还可能大量存在的离子是 ( )
A.NH4+ B.I- C.Ba2+ D.C6H5O-
9.通过置换反应不可能生成 ( )
A.Fe3O4 B.F2 C.A12O3 D.C
|
|
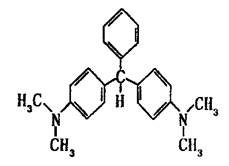
于无色孔雀石绿的叙述中,正确的是( )
|
|
C.与苯胺 互为同系物
D.在一定条件下,1mol无色孔雀石绿可以和9mol氢气发生加成反应
11.在定条件下,氨气与氟气发生反应:4NH3+3F2 NF3+3NH4F,其中NF3分子构型与NH3相似。下列有关说法错误的是 ( )
A.NF3是极性分子
B.NF3既是氧化产物,又是还原产物
C.NH4F中既含有离子键又含有共价键
D.上述反应中,反应物和生成物均属于分子晶体
|
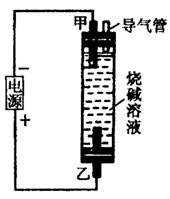
溶液中产生的白色沉淀能保持较长时间不变
色。下列说法错误的是 ( )
A.烧碱溶液注入容器前,需预先煮沸
B.甲电极上有氢气冒出
C.只能用铁作甲电极和乙电极
D.可用食盐水代替烧碱溶液
13.在二氧化碳的水溶液中存在着如下平衡
![]() CO2(g) CO2(aq)
CO2(g) CO2(aq)
![]() CO2(aq)+H2O H2CO3(aq)
CO2(aq)+H2O H2CO3(aq)
![]() H2CO3(aq) H+(aq)+HCO3-(aq)
H2CO3(aq) H+(aq)+HCO3-(aq)
![]() HCO3- (aq) H+(aq)+CO32-(aq)
HCO3- (aq) H+(aq)+CO32-(aq)
下列有关说法正确的是 ( )
A.水中溶解的二氧化碳的浓度,夏天时比冬天的高
B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高
C.气压升高,水中c(HCO3-)增大
D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×10-14
2007年明珠学校高中毕业班质量检查Ⅰ
第Ⅱ卷
26.(16分)铝镁合金已成为轮船制造、化工生产等行业的重要材料。研究性学习小组的三位同学,为测定某含镁3%―5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列三种不同实验方案进行探究。填写下列空白。
![]() [探究一]
[探究一]
实验方案:铝镁合金 测定剩余固体质量
实验中发生反应的化学方程式是 。
实验步骤:
(1)称取5.4g铝镁合金粉末样品,投入VmL 2.0mol・、L-1NaOH溶液中,充分反应, NaOH溶液的体积V≥ 。
|
(填“偏高”或“偏低”)。
![]() [探究二]
[探究二]
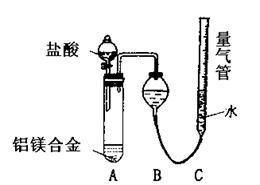
实验方案:铝镁合金 测定生成气体的体积
实验装置:
问题讨论:
(1)某同学提出该实验装置不够完善,应在
A、B之间添加一个干燥、除酸雾的装置。你
的意见是: (填“需要”或“不需要”)
(2)为使测定结果尽可能精确,实验中应注意的问题是(写出两点):
①
。
② 。
|
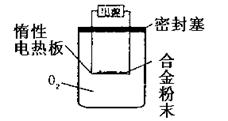
实验方案:称量xg铝镁合金粉末,放在如右图
所示装置的惰性电热板上,通电使其充分灼烧。
问题讨论:
(1)欲计算Mg的质量分数,该实验
中还需测定的数据是 。
(2)若用空气代替O2进行实验,对测定结果是否有影响? (填“是”或“否”。)
[实验拓展]参照探究一、探究二实验方案,请你另设计一个实验方案,测定该铝镁合金中镁的质量分数。
27.(16分)知周期元素A、B、C、D的原子序数依次增大,它们的原子核外电子层数之和
为7。B的化合物种类繁多,数目庞大。A与D能形成原子个数比为1:1和2:1的化合物。
(1)只由A、B、D组成的化合物中,相对分子质量最小的是 ,写出该化合物的一种用途 。人类六大营养素中,只由A、B、D三种元素组成的有 (填其中一种营养素的名称)。
(2)只由A、C组成的一种常见气态化合物,其电子式为 ,工业
|
(3)只由A、C、D组成的盐,发生水解反应的离子方程式为 。
|
是 ;乙为天然蛋白质水解的相对分子质量最小的产
物,其结构简式为 。
|
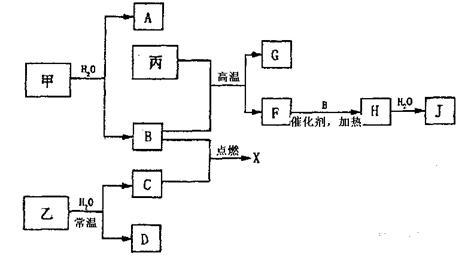
(1)若B与C反应的产物X为两种物质组成的混合物,该反应能放出大量热,常用于
焊接与切割金属,该反应的化学方程式为 。若B与C的反应产
物X是纯净物,反应也能放出大量热,则C是 。
(2)实验室检验F时,常用的试剂为 ,在检验过程中观察到的实验现象是 。
(3)J的工业生产过程中,F→H的反应在 (填工业设备名称)
进行,已知丙与B反应生成1molF时放出426.5kJ的热量,则丙与B反应的热化学方程式
为 。由丙制取1molJ时,需要
消耗 molB。
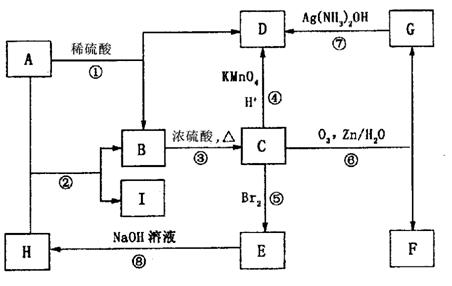
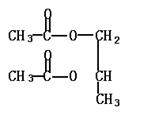
29.(14分)烯烃R―CH=CH2(―R为烷基)在不同条件下可以被氧化成不同产物:
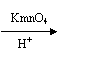 |
R―CH=CH2 R―COOH+CO2
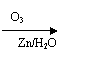 |
R―CH=CH2 R―CHO+HCHO
|
(1)A的结构简式是 ;D所含官能团的名称为 。
(2)反应⑦的化学方程式为 。
|
| |
(3)A的同分异构体中,含有H―C―O―结构的酯有 种。
(4)反应②是酯交换反应(酯+醇→新酯+新醇),反应中A和H的物质的量之比为2:1,
该反应的化学方程式是 。
(5)①―⑧反应中,属于取代反应的是 (填序号)。
参考答案
评分说明:
1.计算题只有最后答案而无演算过程的,不得分;只写出一般公式,但未能与度题所给的具体条件联系的,不得分。
2.化学方程式、离子方程式未配平的,都不得分。
第Ⅰ卷
6.B 7.C 8.A 9.B
|
26.(16分)
[探究一]2A1+2NaOH+2H2O 2NaA1O2+3H2↑ (3分)
(1)97(2分) (2)偏高(1分)
[探究二](1)不需要(1分)
(2)检查装置的气密性;合金完全溶解(或加入足量盐酸,或调整量气管C的高度,使C中液面与B液面相平等合理答案)(各1分,共2分)
[探究三](1)灼烧后固体的质量 (2分)
![]()
![]() (2)是(2分)
(2)是(2分)
[实验拓展]铝镁合金 溶液 测量固体质量
(或铝镁合金 溶液 测定固体质量等合理答案) (3分)
| |
(1)HCHO(或H―C―H、甲醛)(1分)
作消毒剂(或作防腐剂、作化工原料等合理答案)(1分)
|
(2) (1分)

N2+3H2 2NH3(3分) C (2分)
![]() (3)NH4++H2O NH3・H2O+H+(或其它合理答案) (3分)
(3)NH4++H2O NH3・H2O+H+(或其它合理答案) (3分)
(4)NH4++HCO3-+2OH- NH2・H2O+H2O+CO32- (3分)
| |
H2N―CH2―C―OH (1分)
![]() 28.(14分)
28.(14分)
(1)2C2H2+5O2 4CO2+2H2O (3分) H2 (2分)
(2)品红溶液 (1分) 品红溶液褪色,加热后,溶液又变成红色 (2分)
(3)接触室(1分)
4FeS2(s)+1102(g) 2Fe2O3(s)+8SO2(g); △H=-3412kJ・mol-1
(或其它合理答案)(3分)
![]() (3分)
(3分)
| |
(1)CH3―C―O―CH2―CH2―CH3 (2分)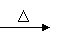 羧基 (1分)
羧基 (1分)
|
(3)4(2分)
| |
| |
| |
CH3 (5)①②⑧(3分)