选择题训练(41)
一、选择题(每小题只有一个正确答案,每小题4分,8小题共32分)
1、相同温度、相同物质的量浓度的四种溶液,①CH3COONa ②NaHSO4③NaCl ④C6H5ONa,按pH由大到小的顺序排列,正确的是:
A.④>①>③>② B.①>④>③>② C.①>②>③>④ D.④>③>①>②
2、用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A、 加热 B、不用稀硫酸而用浓硫酸;
B、 C、滴加少量CuSO4溶液; D、不用铁片而用铁粉
3、某温度下,甲、乙两个烧杯中各盛有100g相同浓度的KCl溶液,现将甲杯蒸发35g水,析出晶体5g;乙烧杯蒸发45g水,析出晶体10g。则原溶液需蒸发多少克水才恰好达到饱和?
A、10g B、15g C、20g D、25g
4、在一定条件下,将m体积NO和n体积O2同时通入倒立于水中且盛满水的容器中内,充分反应后,容器内残留m/2体积的气体,该气体与空气接触后变为红棕色。则m的n比值为
A、3:2 B、2:3 C、8:3 D、3:8
5、在pH值都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子浓度分别为A摩/升与B摩/升,则A和B关系为
A、A>B B、A=10-4 B C、B=10-4 A D、A=B
6、下列离子方程式中正确的是
A、向硝酸银溶液中加入过量氨水:Ag+ + 2NH3・H2O = [Ag(NH4)2]+ + 2H2O
B、苯酚钠溶液中充入少量CO2: C6H5O- + CO2 + H2O →C6H5O- + HCO3-
C、0.5L0.4mol/LFeBr2溶液中标况下的Cl24.48L:2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl-
D、铝粉溶于浓氢氧化钡溶液: 2Al + 4OH- = 2AlO2- + 2H2↑
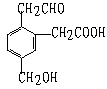 7、某有机物的结构式为它在一定条件下右能发生的反应有①加成
②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
7、某有机物的结构式为它在一定条件下右能发生的反应有①加成
②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
A、②③④ B、①③⑤⑥ C、①③④⑤ D、②③④⑤⑥
8、用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为
A、3 B、4 C、5 D、6
二、选择题(每小题4分,10小题共40分,每小题有一个或两个正确选项。)
9、“不粘锅”的内层其实是在金属的内壁涂了一层聚四氟乙烯,故而不粘食物。以下对聚四氟乙烯的叙述错误的是:
A、它在没有水加热时容易燃烧 B、其中的C-F键非常稳定
C、它的单体含有C=C双键 D、分子内支链多且互相缠绕
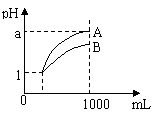 10、pH=1的两种酸溶液A、B各1
mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是
10、pH=1的两种酸溶液A、B各1
mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是
A、A、B两种酸溶液的物质的量浓度一定相等
B、稀释后,A酸溶液的酸性比B酸溶液强;
C、若a = 4,则A是强酸,B是弱酸;
D、若1< a < 4,则A、B都是弱酸。
11、下列溶液一定呈中性的是
A、[H+]=1×10-7mol/L的溶液; B、[NH4+]=[Cl-]的NH4Cl和氨水的混合溶液
C、pH=14-pOH的溶液; D、[H+]=[OH-]=1×10-6mol/L的溶液
![]() 12.某温度下,在容积固定的密闭容器中发生可逆反应:A(g) +
2B(g) 2Q(g)。平衡时,各物质的浓度比为c(A):c(B):c(Q)=1:1:2,保持温度不变,以1:1:2的体积比再充入A、B、Q,则下列叙述正确的是
12.某温度下,在容积固定的密闭容器中发生可逆反应:A(g) +
2B(g) 2Q(g)。平衡时,各物质的浓度比为c(A):c(B):c(Q)=1:1:2,保持温度不变,以1:1:2的体积比再充入A、B、Q,则下列叙述正确的是
A、刚充入时反应速率V正减少,V逆增大;
B、达到新的平衡时,反应混合物中A、B的物质的量分数增加;
C、达到新的平衡时,c(A):c(B):c(Q)仍为1:1:2;
D、达到新的平衡过程中,体系压强先增大,后逐渐减少。
13.C8H18经多步裂化,最后完全转化为C4H8、C3H6、C2H4、C2H6、CH4五种气体的混合物。该混合物的平均相对分子质量可能是
A、28 B、30 C、38 D、40
14、下列说法中正确的是
A、1mol稀硫酸和1mol稀Ba(OH)2溶液完全中和所放出的热量为中和热。
B、中和反应都是放热反应,盐类水解反应都是吸热反应。
C、在101kPa时,1mol碳燃烧所放出的热量一定是碳的燃烧热。
D、碳与二氧化碳的反应既是吸热反应,也是化合反应。
15、下列说法正确的是(NA为阿伏加德罗常数)
A、通常状况时,28g氮气所含原子数目为NA;
B、常温常压下,1mol二氧化氮完全被碱吸收消耗NA个氢氧根离子;
C、在常温常压下;11.2L氯气所含有的原子数目为NA;
D、标况下,22.4L一氯甲烷和二氯甲烷的混合物所含分子数为NA。
16、0.8mol锌跟稀硝酸反应,消耗2molHNO3,则还原产物可能是
A、NO B、NO2 C、N2O D、NH4NO3
17、下列各组溶液中,不用任何其他试剂就能鉴别的是
A、Na2SO4 H2SO4 AlCl3 BaCl2 B、HCl NaOH K2SO4 NaHSO4
C、NaAlO2 KHCO3 NaCl NaHSO4 D、NaOH FeCl3 MgCl2 K2SO4
18、在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是
A、将pH=4的盐酸和醋酸稀释成pH=5的溶液,醋酸所需加入的水量多
B、盐酸和醋酸都可用相应的钠盐与浓酸酸反应制取
C、相同pH值的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH值变化大
D、相同pH值的盐酸和醋酸分别跟锌反应时,产生氢气的起始速度相等