08届高考化学调研测试题
可能用到的相对原子质量:H-1 He—4 C—12 N-14 O—16 Na—23
Cl-35.5 K—39 Cu-64 Br-80 I-127
第一部分 (选择题 共70分)
一、 选择题(本题包括10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1.材料是人类赖以生存的重要物质基础,而化学是材料科学发展的基础。下列有关材料的说法中正确是
A.生活中的玻璃、陶瓷、水泥属于无机硅酸盐材料,其生产原料都需要使用石灰石
B.合金材料钢铁里的铁和碳在潮湿的空气中因构成许多原电池而易发生电化学腐蚀
C.居室装修材料如化纤地毯、三合板、花岗岩等均会释放出污染空气的甲醛气体
D.造成“白色污染”的聚氯乙烯塑料在日常生活中可用来进行食品包装
2.下列现象或应用不能用胶体知识解释的是
A.肾功能衰竭等疾病引起的血液中毒,可利用血液透析进行治疗
B.向牛油和氢氧化钠溶液共煮后的溶液中加入食盐后有固体析出
C.水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
D.氯化铝溶液中加入碳酸钠溶液会出现白色沉淀
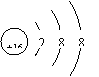 3.下列化学用语表达正确的是
3.下列化学用语表达正确的是
A.硫原子的结构示意图:
B.CaCl2的电子式:![]()
C.乙烯的结构简式:CH2CH2
D.碳酸氢钠溶于水的电离方程式:NaHCO3==Na++HCO3-
4.简单原子的原子结构可用下图形象地表示:
![]()
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的是
A.①②③互为同素异形体 B.①②③互为同位素
C.①②③是三种化学性质不同的粒子 D.①②③具有相同的质量数
5.下列实验方案能达到目的的是
A.除去NaCl固体中混有的MgCl2:加入KOH试剂后过滤
B.实验室获取少量纯净的水:蒸馏自来水
C.己烷中混有少量己烯:加溴水后分液
D.提取碘水中的碘:加入适量乙醇,振荡、静置、分液
6.下列各溶液中,各离子可能大量共存的有
A.含有大量Ba2+的溶液中:HCO3-、Fe3+、Ag+、SO42-、SCN-
B.由水电离的c(OH-)=10-14mol·L-1 的溶液中:CH3COO-、 C6H5O-、Na+、K+
C.滴加无色酚酞试液后仍无色的溶液中:Na+、CO32-、K+、ClO-、AlO2-
D.加入铝粉后产生氢气的溶液中:NH4+、Na+、NO3-、Cl-、S2-
7.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是
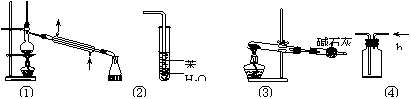
A.装置①常用于分离互不相溶液混合物
B.装置②可用于吸收HCl气体,并防倒吸
C.以NH4HCO3为原料,装置③可用于实验室制备少量NH3
D.装置④b口进气可收集CO2、NO等气体
8.下列各组物质的性质比较,正确的是
A.酸性:HClO4>H3PO4>H2SO4 B.氢化物稳定性:H2S>HF>H2O
C.碱性:NaOH>Mg(OH)2>Ca(OH)2 D.氧化性:F2 > Cl2 > Br2 > I2
9.已知下列几种烷烃的燃烧热数据如下:
| 烷烃 | 甲烷 | 乙烷 | 丙烷 | 丁烷 |
| 燃烧热/(kJ/mol-1) | 890 | 1560 | 2220 | 2880 |
据此判断,表示戊烷燃烧的热化学方程式正确的是
A.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(l);△H = - 3540 kJ/mol
B.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(g);△H = - 3540 kJ/mol
C.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(g);△H = + 3540 kJ/mol
D.C5H12(l) + 8O2(g) = 5CO2(g) + 6H2O(l);△H = + 3540 kJ/mol
10.海水淡化可采用膜分离技术。如右下图所示,对淡化膜右侧的海水加压,水分子可以透过淡化膜进入左侧淡水池,而海水中其它各种离子不能通过淡化膜,从而得到淡水。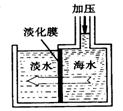 对加压后右侧海水成分变化分析正确的是
对加压后右侧海水成分变化分析正确的是
A.溶质质量增加 B.溶剂质量减少
C.溶液质量不变 D.溶质质量分数减少
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
11.第ⅡA的铍在一定条件下可形成化合物Na2BeO2。下列有关铍及其化合物的叙述正确的是
A.氧化铍不能溶于盐酸 B.氢氧化铍易溶于水
C.单质铍可溶于氢氧化钠溶液生成氢气 D.Na2BeO2溶液呈碱性
12.在蒸发皿中加热蒸干并灼热(低于400℃)下列物质的溶液,可以得到该物质固体的是
A.氯化铝 B.碳酸钠 C.碳酸镁 D.高锰酸钾
13.下列说法正确的是
A.把100mL3mol·L-1的H2SO4跟100mLH2O混合,硫酸的物质的量浓度改变为1.5mol·L-1
B.把100g20%的NaCl溶液跟100gH2O混合后,NaCl溶液的质量分数是10%
C.把200mL3mol·L-1的BaCl2溶液跟100mL3mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3mol·L-1
D.把100mL20%的NaOH溶液跟100mLH2O混合后,NaOH溶液的质量分数是10%
14.常温下,0.1 mol·L-1某一元酸(HA)溶液中![]() =1×10-8,下列叙述正确的是
=1×10-8,下列叙述正确的是
A.溶液中水电离出的c(H+)=10-10 mol·L-1
B.溶液中c(H+)+c(A-)=0.1 mol·L-1
C.与0.05 mol·L-1 NaOH溶液等体积混合后所得溶液中离子浓度大小关系为
c(A-)>c(Na+)>c(OH-)>c(H+)
D.上述溶液中加入一定量CH3COONa晶体或加水稀释,溶液的c(OH-)均增大
15.某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
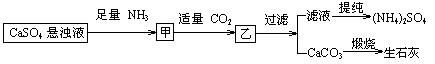
下列推断不合理的是
A.往甲中通CO2有利于(NH4)2SO4生成
B.生成1mol(NH4)2SO4至少消耗2 NH3
C.CO2可被循环使用
D.直接蒸干滤液能得到纯净的(NH4)2SO4
16.下列离子方程式书写正确的是:
A.将Ba(OH)2溶液不断加入KAl(SO4)2溶液中反应至沉淀物质的量最大:
3Ba2+ + 6OH– + 2Al3+ + 3SO42–== 3BaSO4↓+ 2Al(OH)3↓
B.向硝酸银溶液中加入过量氨水:Ag+ + 2NH3·H2O = [Ag(NH3)2]+ + 2H2O
C.CuSO4溶液跟Ba(OH)2溶液混合:Ba2+ + SO42– == BaSO4↓
D.氢氧化铁溶于氢碘酸中:Fe(OH)3 + 3H+ = Fe3+ + 3H2O
17.pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000mL,其pH值与溶液体积的关系如图,下列说法正确的是
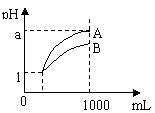 A.A、B两种酸溶液的物质的量浓度一定相等
A.A、B两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液强;
C.若a = 4,则A是强酸,B是弱酸;
D.若1< a < 4,则A、B都是弱酸。
 18.目前人们正在研究一种高能电池——钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na + xS Na2Sx,以下说法正确的是:
18.目前人们正在研究一种高能电池——钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na + xS Na2Sx,以下说法正确的是:
A.放电时钠作正极,硫作负极;
B.充电时钠极与外电源的正极相连,硫与外电源的负极相连
C.充电时,阳极发生的反应为:Sx2- - 2e = x S
D.放电时钠极发生氧化反应
19、在一定条件下密闭容器中的反应:2A(g)+B(g)![]() 2C(g),△H<0到达平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是
2C(g),△H<0到达平衡后,改变一个条件x,下列量y的变化一定符合图中曲线的是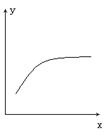
| x | y | |
| A | 再加入A | B的转化率 |
| B | 再加入C | A的体积分数 |
| C | 缩小体积 | A的转化率 |
| D | 升高温度 | 混合气体的平均摩尔质量 |
20、混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是
A.向CuSO4溶液中加入适量铁粉
B.等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液
C.等物质的量的NaHCO3与Na2O2固体;
D.在NaBr溶液中充入过量氯气;
第二部分 (非选择题共80分)
三、(本题包括3小题,共28分)
21.硝酸钾是一种用途广泛的化工原料,工业中利用温度对溶解度的影响,常用硝酸钠与氯化钾按一定比例混合结晶得到。
请填写下表中的空格,并回答相关问题。
| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 称量、溶解 | 称取20 g硝酸钠和 17 g氯化钾,溶解在 35 Ml 蒸馏水 |
| ② | 蒸发 | 加热蒸发,当 停止加热 |
| ③ | 过滤 | 在承接滤液的烧杯应预先加2mL的蒸馏水,趁热过滤, |
| ④ | ||
| ⑤ | 减压过滤得到粗产品 | |
| ⑥ | 重结晶 得到产品 |
(1)在步骤③中趁热过滤的目的是: ,在热过滤中,承接滤液的烧
杯应预先加2mL的蒸馏水,其作用是: 。
(2) 步骤③、④两次过滤后都应该用少量蒸馏水洗涤晶体,步骤③应用 水、步骤④ 水(填“冷、热”)
(3)实验中得到的粗产品和产品在成分上有明显的区别,请用实验加以区分(简述实验过程)
22、(10分)化学研究小组,通过网上查找资料发现,Cl2的制取有下列不同方案:
![]() 方案:加热条件下二氧化锰与浓盐酸反应制得Cl2
方案:加热条件下二氧化锰与浓盐酸反应制得Cl2
![]() 方案:浓盐酸与氯酸钾固体反应制得Cl2
方案:浓盐酸与氯酸钾固体反应制得Cl2
![]() 方案:电解饱和食盐水法制得Cl2
方案:电解饱和食盐水法制得Cl2
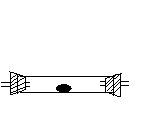
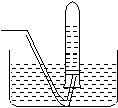
现实验室有供选择的如下几种仪器来制取Cl2
 | |||||||
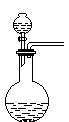 | |||||||
 | |||||||
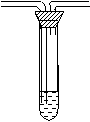 | |||||||

A B C D E
(1)用上述仪器不能实现的方案为 。不考虑固定装置的仪器,可行但缺仪器的方案是 ,所缺的仪器是 。
(2)若按b方案制Cl2时发生化学方程为_______________________,要制取并收集纯净的Cl2(允许含有少量水蒸气或空气),须使用到的上述仪器中的(按气流从左到右的流向顺序列出)___ (填A、B、C……)。
(3)若要设计联合实验探究氯气的漂白原理,从制备装置中产生氯气后应连接的装置是(画出装置图并注明所使用的试剂或用品)
23.实验探究题(18分)
Ⅰ.某校化学实验兴趣小组在“探究卤素单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入1~2滴溴水,振荡后溶液呈黄色。
(1)提出问题:![]() 、
、![]() 谁的氧化性更强?
谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:![]() >
>![]() ,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含_▲_(填化学式,下同)所致。
,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含_▲_(填化学式,下同)所致。
②乙同学认为氧化性:![]() >
> ![]() ,故上述实验现象是发生化学反应所致,则溶液呈黄色是含_▲_所致。
,故上述实验现象是发生化学反应所致,则溶液呈黄色是含_▲_所致。
(3)设计实验并验证:
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a. 酚酞试液 b. 四氯化碳 c. 无水酒精 d. 硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
(4)应用与拓展:
①在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为_▲_。
②在100![]() 溶液中通入
溶液中通入![]() (标准状况),溶液中有1/3的Br-被氧化成单质
(标准状况),溶液中有1/3的Br-被氧化成单质![]() ,则原
,则原![]() 溶液中
溶液中![]() 的物质的量浓度为_▲_。
的物质的量浓度为_▲_。
四、(本题包括3小题,共30分)
24.(10分)黄铜是一种铜锌合金,除含铜和锌外,还含有少量铅、铁等杂质。为了测定黄铜中铜的百分含量,实验共分为五步完成:①用2︰1的浓硝酸在加热条件下溶解黄铜屑,使Cu、Zn、Pb、Fe转化成Cu2+、Zn2+、Pb2+、Fe3+进人溶液;②用2︰1的氨水中和溶液中过量的硝酸(用弱酸调pH值确保各种金属阳离子不沉淀),并移入250mL锥形瓶中;③称取黄铜屑0.1g放入小烧杯中;④加入掩蔽剂NH4HF2溶液,使Fe3+变成不参与反应的[FeF6]3-离子,然后再加入过量KI溶液;⑤用浓度为0.06mol/L的Na2S2O3溶液滴定至溶液呈浅黄色时,加入0.2%的淀粉溶液作指示剂继续滴定至终点。滴定反应方程式为:2Na2S2O3+I2=2NaI+Na2S4O6。重复滴定3次,平均耗用Na2S2O3溶液为15.80mL。
(1)用编号填出实验步骤的正确操作顺序为
(2)根据已知事实写出测定含铜量过程中加入KI溶液后发生反应的离子方程式:
(3)根据已知数据写出计算含铜量的数学式(无需化简)
(4)如果不加NH4HF2会使测定结果 (填偏高、偏低、无影响),原因是
(5)溶液中Pb2+、Zn2+不影响实验结果的原因是
25.(12分)MnO2和锌是制造干电池的主要原料。某地有软锰矿和闪锌矿两座矿山,它们的主要成份为:
软锰矿:MnO2含量≥65% Al2O3含量为4%
闪锌矿:ZnS含量≥80% FeS、 CuS、 CdS含量各为2%
电解法生产MnO2传统的工艺主要流程为:软锰矿加煤还原焙烧;用硫酸浸出焙烧料;浸出液经净化后再进行电解,MnO2在电解池的阳极析出。
电解锌的传统生产工艺为:闪锌矿高温氧化脱硫再用热还原法还原得粗锌:
2ZnS+O2![]() 2ZnO+2SO2 2C+O2
2ZnO+2SO2 2C+O2![]() 2CO ZnO+CO
2CO ZnO+CO![]() Zn(g)+CO2
Zn(g)+CO2
将用热还原法制得的粗锌溶于硫酸,再电解ZnSO4溶液可生产纯度为99.95%的锌。
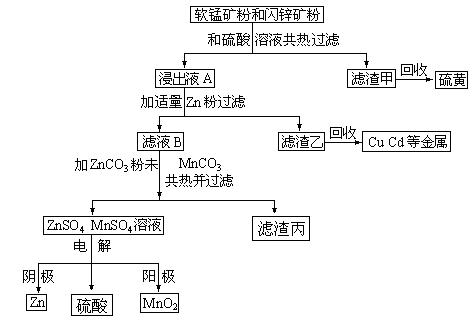
现在生产MnO2和锌的新工艺主要是通过电解获得MnO2和锌,副产品是硫、金属铜和镉。简化流程杠图如下:
试回答下列问题:
(1)Zn的原子序数为30,它在元素周期表中的位置是 ;软锰矿、闪锌矿粉未与硫酸溶液共热时析出硫的反应为氧化-还原反应,例如:MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O,据此写出MnO2在酸性溶液中分别FeS发生氧化-还原反应的化学方程式 ;软锰矿中Al2O3溶于硫酸的离子方程式 ;由滤渣甲回收硫黄的实验方法是 ;
(2)用离子方程式表示浸出液A与适量Zn粉作用得到滤液B与滤渣乙的过程
(3)滤渣丙的化学成分是 ;
(4)用铁和铂电极电解MnSO4和ZnSO4的混合溶液可以得到Zn和MnO2,电解时,铁做
极,铁极发生的电极反应为 。
(5)试从环境保护和能量消耗的角度评价90年代新工艺相比较有哪些优点
。
26.(10分)红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基本化工原料,在印染工业、电镀工业和皮革工业中作助剂,在化学工业和制药工业中也用作氧化剂,应用领域十分广泛。
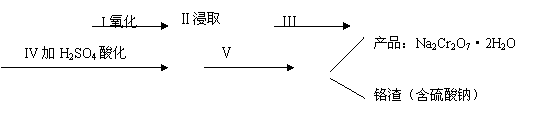
(1)实验室中红矾钠可用铬铁矿(主要成分:FeO·Cr2O3)利用以下过程来制取。
 |
![]() 铬铁矿等原料
Na2CrO4溶液
铬铁矿等原料
Na2CrO4溶液
①步骤I中反应的化学方程式为:
![]() △H<0
△H<0
该反应的化学平衡常数的表达式为 。
②图1、图2表示该反应在t1时达到平衡、在t2时因改变某个条件而发生变化的曲线:
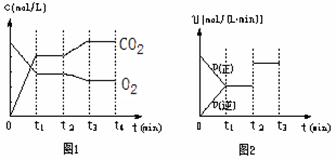 由图1判断,反应进行至t2 min时,曲线发生变化的原因是
由图1判断,反应进行至t2 min时,曲线发生变化的原因是
(用文字表达)。由图2判断,t2 min到t3 min 的曲线变化的原因可能是 (填编号)
a.升高温度 b.加了催化剂
c.将原料粉碎 d.缩小容器体积
(2)步骤Ⅱ中所得溶液显碱性,其中除含有Na2CrO4外还含有铝、硅元素的化合物,它们的化学式可能是 、 。
①步骤Ⅲ需将溶液的pH调至7~8并煮沸,其目的是 。
②步骤Ⅳ中发生反应的离子方程式为: 。
五、(本题包括1小题,共8分)
27.尼泊金酸的结构简式为: ![]()
(1)尼泊金酸的分子式为____________。
(2)尼泊金酸不具有的性质是_________(选填序号)。
a. 可溶于水 b. 通常状况下呈固态 c. 发生消去反应 d. 遇FeCl3溶液显紫色
(3)1 mol尼泊金酸与下列物质反应时,最多可消耗__________(选填序号)。
a. 4 mol H2 b. 2 mol NaHCO3 c. 2 mol Br2 d. 2 mol Na2CO3
(4)将尼泊金酸与足量NaOH溶液混合后反应,生成的有机物结构简式为_________________。
(5)尼泊金酸有多种同分异构体,写出以下含有苯环的同分异构体的结构简式:
ⅰ酯类___________________________;ⅱ醛类___________________________。
六、(本题为分叉题,共10分,分为A、B两题,考生可任选一题。若两题均做,一律按A题计分)
28(A)(10分)下表为长式周期表的一部分,其中的编号代表对应的元素。
| ① | |||||||||||||||||
| ② | ③ | ||||||||||||||||
| ④ | ⑤ | ⑥ | ⑦ | ||||||||||||||
| ⑧ | ⑨ | ⑩ |
请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的常见化合物的晶体类型是________________。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的孤对电子数为 ;该元素与元素①形成的分子X的空间构形为
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式: 。
(5) 1183 K以下⑨元素形成的晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的原子间距离相同。
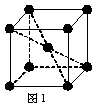
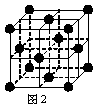
在1183 K以下的晶体中,与⑨原子等距离且最近的⑨原子数为______个,在1183 K以上的晶体中,与⑨原子等距离且最近的⑨原子数为________, 转变温度前后两者的密度比(1183 K以下与1183 K以上之比)___________。(用根号表示)
28、(B)(10分)(一)已知:HCN的结构为H—C≡N,R—CN RCOOH,
![]() R—Cl+CN- R—CN+Cl-
R—Cl+CN- R—CN+Cl-
![]() (R为烃基)。玉米芯、甘蔗渣等废物水解发酵后可制得糠醛
, 它是重要的化工原料,它在一定条件下可发生以下变化:
(R为烃基)。玉米芯、甘蔗渣等废物水解发酵后可制得糠醛
, 它是重要的化工原料,它在一定条件下可发生以下变化:
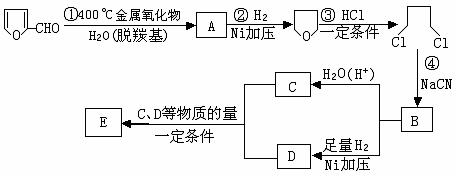
(1)写出反应类型:② ,④ 。
(2)写出反应③的化学方程式: ;
写出能证明糠醛中含有醛基的一个化学反应方程式 。
(3)若E为环状化合物,则其结构简式 。
(二)相对分子质量不超过100的有机物A, 既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。 A完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现A的氢谱如下:
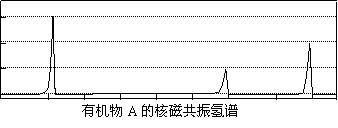 |
试写出A与甲醇反应生成有机物B的化学反应方程式:
。
[参考答案]
一.选择题,每小题3分,共30分
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 答案 | B | D | D | B | B | B | C | D | A | B |
二、选择题(本题包括10小题,每小题4分,共40分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分)
| 题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 答案 | AD | B | B | D | D | AB | C | CD | AC | BD |
第二部分 (非选择题共80分)
三、(本题包括3小题,共30分)
21.(8分)
(1)(2分)避免溶液冷却时硝酸钾晶体析出。防止降温时氯化钠溶液达饱和而析出。
(2)热、冷(每空1分)
(3)(4分) 取少量样品置于干净的试管中,加入少量蒸馏水溶解,加硝酸酸化后加入硝酸银溶液观察是否有白色沉淀生成。有则样品是粗产品,无则产品及格。
22、(12分)
(1)c(1分), a(1分), 酒精灯(1分) (2)方程式略(2分)。EBC(或ED:排饱和食盐水法)(2分)
(3)图略(流程:干燥---通入干的红布条-----通入显的红布条-----通氢氧化钠溶液)(4分,装置2分,试剂2分)
23.(10分)
(2)、①Br2 ②Fe3+ (3)、 d 溶液呈血红色, b CCl4层呈无色。(以上每空1分,共6分),(4)、2Fe2++Br2=2Fe3++2Br- (2分) 5、1.2mol/L(2分)
四、(本题包括3小题,共32分)
24.(20分)
(1)③①②④⑤ (2分)
(2)2Cu2++4I-=2CuI↓+I2 (2分)
(3)![]() (2分)
(2分)
(4)偏高 (1分); Fe3+可氧化I-生成I2,使I2的量增加,消耗Na2S2O3的量增多。 (1分)
(5)Pb2+、Zn2+的氧化性比Cu2+的氧化性弱,不能氧化I-。 (2分)
25.(12分)
(1)四周期ⅡB族;MnO2+2FeS+6H2SO4=Fe2(SO4)3+3MnSO4+2S¯+6H2O ,
Al2O3+6H+=2Al3++3H2O ,
加热(每空1分)
(2)Zn+Cu2+=Cu+Zn2+ Zn+Cd2+=Cd+Zn2+ Zn+2Fe3+=2Fe2++Zn2+ (3分)
(3)Fe(OH)3,Al(OH)3; (2分,漏写1分)
(4)阴极(1分);Zn2++2e-=Zn(1分)
(5)从环境保护角度评价:无SO2对大气的污染;从能量消耗角度评价:无高温焙烧热污染,不需要高温焙烧节约燃料。(2分)
26.(10分)
(1)①![]() (2分)
(2分)
②t2 时对平衡体系降温 (2分) b(1分)
(2)NaA1O2[或NaA1(OH)4]、Na2SiO3(各1分,共2分)
①除去A1O2、SiO32-等杂质(1分)
②2CrO42-+2H+=Cr2O72-+H2O(2分)
五、(本题包括1小题,共8分)
27.(8分)
(1)C7H6O3(1分);(2)c(1分);
(3)c.d(2分);
(4)
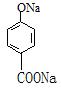 (2分);
(2分);
(5) ⅰ: (邻,间等)(1分);ⅱ:
(邻,间等)(1分);ⅱ: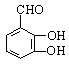 (1分)。
(1分)。
六、(本题为分叉题,共10分,分为A、B两题,考生可任选一题。若两题均做,一律按A题计分)
28(A)(10分)
(1)⑨ (1分) (2)苯 (1分) 分子晶体 (1分)(3) 1 (1分)三角锥形 (1分)(4) Be(OH)2+2NaOH=Na2BeO2+2H2O (1分)(5)8 (1分)12 (1分) ![]() (2分)
(2分)
28(B)(10分)
(一)⑴加成反应 取代反应(各1分,共2分)
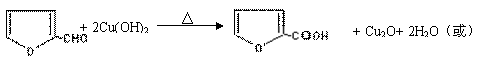 ⑵
⑵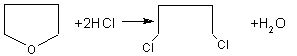 (2分)
(2分)

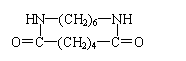 |
⑶ (2分)
![]()
![]() (二)CH2=C(CH3)COOH+CH3OH
CH2=C(CH3)COOCH3+H2O(2分)
(二)CH2=C(CH3)COOH+CH3OH
CH2=C(CH3)COOCH3+H2O(2分)