第一学期化学选修1化学与生活
第一章关注营养平衡
单元检测题
第Ⅰ卷
一.选择题 (每小题只有一个选项符合题意)
1. 在一定条件下,纤维素与浓H2SO4和浓HNO3的混合酸反应生成硝酸纤维,这个反应的类型属于( )
A.硝化 B.磺化 C.酯化 D.氧化
2.下列有机反应中,不属于还原反应的是( )
A.葡萄糖→六元醇 B.丙醛→1-丙醇
C.正丙醇→正丙醛 D.植物油→硬化油
3.下列各组物质中,互为同分异构体的是( )
A.淀粉和纤维素 B.苯甲醇与邻甲苯酚
C.葡萄糖与麦芽糖 D.乙醇与乙醚
4.环氧乙烷(![]() )、丙酮、丁醛、葡萄糖的混合物,碳元素的质量分数为66%,则氧元素的质量分数为( )
)、丙酮、丁醛、葡萄糖的混合物,碳元素的质量分数为66%,则氧元素的质量分数为( )
A.33% B.27% C.30% D.23%
5.下列物质是以蛋白质为原料制成的是
A.胶棉 B.人造丝 C.阿胶 D.人造棉
6.下列叙述中,正确的是 ( )
①能发生酯化反应的酸一定是羧酸 ②油脂水解后得到的醇是丙三醇 ③天然蛋白质水解的最后产物是多种α—氨基酸 ④淀粉、纤维素、油脂都是高分子化合物 ⑤蛋白质溶液中加入K2SO4溶液后,蛋白质从溶液中析出,这种变化叫变性
A. ③ B. ③④ C.②③ D.①⑤
7.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣服的汗渍、血迹及人体排放的蛋白质油渍遇到它,皆能水解而除去,下列衣料中不能用加酶洗衣粉洗涤的是 ( )
①棉织品 ②毛织品 ③晴纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥锦纶织品
A. ①②③ B. ②④ C. ③④⑤ D.③⑤⑥
8.葡萄糖的分子式为C6H12O6,通过缩合反应把10个葡萄糖分子连接起来所形成的链状化合物的化学式为 ( )
A.C60H120O60 B. C60H100O52 C.C60H102O51 D. C60H112O51
二.选择题 (每小题有一个或二个选项符合题意)
9.用石灰水保存鲜蛋是一种化学保鲜法。石灰水能保存鲜蛋的原理是 ( )
①石灰具有强碱性,杀菌能力强 ②石灰水能与鲜蛋呼出的CO2反应,生成碳酸钙薄膜,起保护作用 ③石灰水是电解质溶液,能使蛋白质凝聚 ④石灰水能渗入蛋内中和酸性物质
A. ①② B. ③④ C. ②④ D. ①③
10.生物体内氧化所产生的代谢水的质量,不同的物质有所不同,最高者每氧化1g该物质可产生1.07ml水。骆驼体内储存有大量该物质,故30多天不喝水也能照常活动,该物质是 ( )
A.蛋白质 B.脂肪 C.葡萄糖 D.肝糖元
11.下列反应既是加成反应又可看作还原反应的是 ( )
A.乙烯水化 B.油脂氢化 C.乙醛转化为乙醇 D.乙醛转化为乙酸
12.有一种二肽的化学式是C8H14N2O5 ,水解后得到丙氨酸和另一氨基酸X,X的化学式是 ( )
A.C5H7N2O5 B.C5H9N2O5 C.C5H11NO5 D.C5H7NO4
13.下列物质属于油脂的是( ).
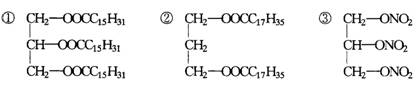
④润滑油 ⑤花生油 ⑥石蜡
A.①② B.④⑤ C.①⑤ D.①③
14.下列物质不属于同系物的是( ).
A.乙酸异戊酯、异戊酸异戊酯 B.硬脂酸、油酸
C.乙二醇、丙三醇 D.甲酸、硬脂酸
15.下列各实验现象能用同一原理解释的是 ( )
A.苯酚、乙烯都能使溴水褪色
B.稀硫酸中加入铜粉不反应,再加入硝酸钠或硝酸铁后,铜粉溶解
C.葡萄糖和福尔马林与新制的氢氧化铜悬浊液共热,都产生红色沉淀
D.将SO2通入氯化钡溶液至饱和,再加入足量硝酸或苛性钠溶液,都产生白色沉淀
16.下列操作不能达到实验目的的是 ( )
A.提纯蛋白质可以在蛋白质溶液中加饱和(NH4)2SO4溶液,蛋白质析出,然后把沉淀溶于蒸馏水中
B.制溴苯时采用三溴化铁作催化剂
C.石蜡和氧化铝混合加热,生成的气体能使酸性高锰酸钾溶液褪色,证明生成的气体中含有不饱和烃
D.淀粉溶液中加入硫酸加热水解,冷却,加银氨溶液做银镜反应
17.1998年江西曾发生误食工业用猪油的中毒事件,调查原因是工业品包装中混入有机锡等,下列有关叙述正确的是 ( )
A.猪油是天然有机高分子化合物
B.猪油是高级脂肪酸甘油酯
C.猪油发生皂化反应,反应液使蓝色石蕊试纸变红
D.猪油皂化反应完全后,反应液静置分为两层
18.人类在地球上的活动致使一年内产生的CO2(主要是煤和石油的利用)约达200亿吨,若植物将这些CO2全部转化为淀粉,那么最终由此而生成的淀粉最接近( )
A.1200亿吨 B.120亿吨 C.200亿吨 D.400亿吨
第Ⅱ卷
三.实验题
19.下列有机实验操作或叙述中正确的是 (填写代号)。
A.用银氨溶液检验某病人是否患糖尿病
B.乙酸乙酯中的少量乙酸可用饱和碳酸钠溶液除去
C.蔗糖水解时应用浓硫酸作催化剂
D.在鸡蛋白溶液中滴入浓硝酸,微热会产生黄色物质
E.在植物油中滴入溴水,溴水会褪色
F.用盐析法分离油脂皂化反应的产物
G.在酒精中加新制生石灰后蒸馏制无水酒精
H.制酚醛树脂时,应将温度计插入水浴中
20.某学生进行蔗糖水解实验,并检验水解产物中是否含有葡萄糖。该生拟定如下操作:
A.取一只试管制取Cu(OH)2沉淀备用;B.再加入3ml~5mlH2SO4;C.再加入3ml~5mlNaOH溶液;D.加入NaOH溶液中和其中的硫酸;E.加入稀硫酸中和其中的氢氧化钠;F.把氢氧化铜沉淀加入溶液中;G.加热煮沸几分钟;H.加热至沸,观察之;I.取一支试管加入少量蔗糖溶液。
⑴从上述操作中选择必要的若干步,按实验正确顺序填入下列空格中:
A—( )—( )—( )—( )—( )—( )
⑵写出蔗糖水解的化学方程式 。
⑶写出用氢氧化铜检验葡萄糖的化学方程式 。
四.填空题
21. 柴杉醇是一种新型抗癌药,其分子式C47H51NO14,它是由如下的A酸和B醇生成的一种酯。
![]()
B.R—OH(R是一个含C、H、O的基团)
(1)A可在无机酸的催化下水解,其反应方程式是:____________________________。
⑵ A水解所得的氨基酸不是天然蛋白质的水解产物,因为 。
(3)写出R-OH的分子式_____________________________。
22. 甘油的用途很广,大量用来制造硝化甘油,硝化甘油是甘油与浓硝酸发生酯化反应(在浓硫酸条件下)生成的三硝酸甘油酯.硝化甘油是制备炸药的原料,在医疗上又是心脏病的急救药.试写出以油脂(主要成分是硬脂酸甘油酯)、氨气、空气、水和氢氧化钠为原料制取硝化甘油的化学方程式.
_______________,_______________,_______________,_______________,_______________.
三.计算题
23.某高级脂肪酸![]() 0.2mol完全燃烧,生成二氧化碳和水共6.8mol;同量的
0.2mol完全燃烧,生成二氧化碳和水共6.8mol;同量的![]() 与64g溴完全加成.求该高级脂肪酸分子中m和n的值.
与64g溴完全加成.求该高级脂肪酸分子中m和n的值.
24.参考下列①~③项内容,回答问题:
①皂化值,是使1g油脂皂化所需要的KOH的毫克数.
②碘值,是使100g油脂与碘加成时消耗单质碘的克数.
③几种油脂的皂化值、碘值列表如下:
| 花生油 | 亚麻仁油 | 牛油 | 黄油 | 硬化大豆油 | 大豆油 | |
| 皂化值 | 190 | 180 | 192 | 226 | 193 | 193 |
| 碘值 | 90 | 182 | 38 | 38 | 5 | 126 |
(1)甘油酯![]() (相对分子质量为884)形成的油.用KOH皂化时,其皂化值为________,反应的化学方程式:_______________________.
(相对分子质量为884)形成的油.用KOH皂化时,其皂化值为________,反应的化学方程式:_______________________.
(2)填空回答:
①亚麻仁油比花生油所含的________________;
②黄油比牛油________________;
③硬化大豆油的碘值小的原因是________________.
(3)为使碘值为180的100g鱼油硬化,所需的氢气的体积在标准状况下为多少升?
(4)用下列结构式所代表的酯,若皂化值为430,求n为多少?并完成下列反应方程式.
![]() →( )+( )
→( )+( )
参考答案:
一.选择题
1.C 2.C 3.B 4.D 5.C 6.C 7.B 8.C
二.选择题
9.A 10. B 11. BC 12. D 13. C 14.BC 15. BC 16.D
17.B 18. B
三.实验题
19.B 、 D 、 E 、 F 、 G 20.⑴ I B G D F H ,⑵、⑶ 略。
四.填空题
21.(1)![]() +C6H5-COOH 。 ⑵氨基不在α位
。
+C6H5-COOH 。 ⑵氨基不在α位
。
(3)C31H38O11。
22.![]()
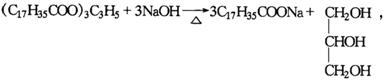
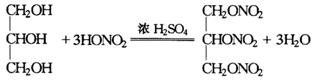
五.计算题
23.解:![]() 为0.4mol,与0.2mol
为0.4mol,与0.2mol![]() 完全加成,说明该酸分子中有两个碳碳双键,则n与m的关系是:n=2m+1-4=2m-3……①
完全加成,说明该酸分子中有两个碳碳双键,则n与m的关系是:n=2m+1-4=2m-3……①
该高级脂肪酸的分子式是![]() ,1mol该酸完全燃烧后生成(m+1)mol
,1mol该酸完全燃烧后生成(m+1)mol ![]() 和
和![]() .已知0.2mol
.已知0.2mol![]() 完全燃烧生成
完全燃烧生成![]() 和
和![]() 共6.8mol,则可列式:1∶〔(m+1)+
共6.8mol,则可列式:1∶〔(m+1)+![]() 〕=0.2∶6.8 即2m+n=65……②
〕=0.2∶6.8 即2m+n=65……②
综合关系式①、②计算可得:m=17,n=31
24.(1)190,![]()
(2)①不饱和脂肪酸(酸根)多;②低级脂肪酸(酸根)多;③不饱和键少
(3)![]()