高考化学无机部分选择题强化训练(五)
命题:毕长明 2006-11-29 时间:40分钟
请务必将选择题答案填在题后的表格中
一、选择题(本题共有8个小题,每题只有一个答案)
1.2006年9月28日,中国科学家研制的“人造太阳”成功地进行了一次放电。所谓“人造太阳”是指受控核聚变。从1 L海水中提取出来的氘(![]() )受控核聚变成氦(
)受控核聚变成氦(![]() )时产生的能量相当于300 L汽油燃烧放出的能量。因此这种技术对解决能源问题有着十分广阔的发展前景。下列有关说法正确的是
)时产生的能量相当于300 L汽油燃烧放出的能量。因此这种技术对解决能源问题有着十分广阔的发展前景。下列有关说法正确的是
A.氘(![]() )受控核聚变成氦(
)受控核聚变成氦(![]() )是一种化学变化
)是一种化学变化
B.![]() 和
和![]() 互为同位素
互为同位素
C.符号![]() 中的“2”与符号
中的“2”与符号![]() 中的“2”意义不同
中的“2”意义不同
D.![]() 2和
2和![]() 2的物理性质、化学性质都存在着很大的差异
2的物理性质、化学性质都存在着很大的差异
2.正确掌握化学用语是学好化学的基础。下列有关表述中正确的一组是
A.C2H4和C4H8两物质中碳的质量分数相同,它们一定是同系物
B.16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体
C.S2-的结构示意图为:![]() ,NH4Cl的电子式为:
,NH4Cl的电子式为: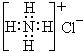
D.SiH4、CH4、NH4+的空间构型均为正四面体型;CO2、C2H2均为直线型
3.最新研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,可以得到的正确结论是
![]() A.羰基硫属于非极性分子
A.羰基硫属于非极性分子
B.羰基硫的电子式为:
C.羰基硫沸点比CO2低
D.羰基硫分子中三个原子不在同一直线上
4.下列各选项所述的两个量,前者一定大于后者的是
①F![]() 和Br
和Br![]() 的沸点 ②纯水在25℃和80℃时的pH
的沸点 ②纯水在25℃和80℃时的pH
③同温下分别在100 g水中最多能溶解的无水CuSO![]() 和CuSO
和CuSO![]() · 5H
· 5H![]() O的质量
O的质量
④25℃时,等体积且pH都等于5的盐酸和AlCl![]() 溶液中,已电离的水分子数
溶液中,已电离的水分子数
⑤在NH![]() +NO—→ N
+NO—→ N![]() +H
+H![]() O(未配平)反应中,被氧化和被还原的N 原子数
O(未配平)反应中,被氧化和被还原的N 原子数
⑥耐火材料MgO和CaO的熔点 ⑦H![]() 和H
和H![]() 的离子半径
的离子半径
A.①②④ B.②③⑤ C.②⑥⑦ D.⑤⑥⑦
5.从下列事实所列出的相应结论正确的是
| 实 验 事 实 | 结 论 | |
| A | Cl2的水溶液可以导电 | Cl2是电解质 |
| B | SO2通入硝酸钡溶液出现白色沉淀 | BaSO3不溶于强酸 |
| C | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->H3AlO3 |
| D | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
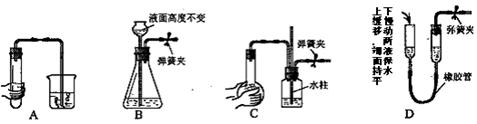 6.下列各图所示装置,肯定不符合气密性要求的是
6.下列各图所示装置,肯定不符合气密性要求的是
7.甲、乙都是短周期元素,其中甲元素原子的最外层电子数是次外层电子数的2倍,乙元素原子K层
和M层电子数之和与L层的电子数相同。下列判断不正确的是
A.乙元素的族序数比甲元素的族序数大
B.乙元素最高价含氧酸酸性比甲元素最高价含氧酸酸性强
C.乙元素的原子序数比甲元素的原子序数大
D.含乙元素的化合物数目比含甲元素的化合物数目多
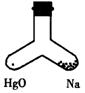 8.在右图支管中,一管装入2.3g金属钠,一管装入HgO,同时加热两部分,Na完全燃烧 ,若加热后容器里空气成分基本未变,则HgO质量可能是
8.在右图支管中,一管装入2.3g金属钠,一管装入HgO,同时加热两部分,Na完全燃烧 ,若加热后容器里空气成分基本未变,则HgO质量可能是
A.21.7g B.24g
C.43.4g D.10.85g
二、选择题(本题包括8小题,每小题1~2个答案)
9.阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中不正确的是
A.将162.5g FeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数小于6.02×1023
B.在含196g H2SO4的浓硫酸溶液中加入足量的锌粉使其充分反应,则反应结束时,转移电子数约为4×6.02×1023个
C.在石墨晶体中,平均0.3 mol碳碳共价键所含有的碳原子数约为0.2×6.02×1023
D.1mol C10H22分子中共价键总数约为31×6.02×1023
10.为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性。 ②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。 ③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀。 ④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀。根据实验以下推测正确的是
A.一定有SO32-离子 B.一定有CO32-离子
C.不能确定C1-离子是否存在 D.不能确定HCO3-离子是否存在
11.下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是
| (I) | (II) | |
| A | 少量CO2通入Ba(OH)2溶液 | 过量CO2通入少量Ba(OH)2溶液 |
| B | 少量浓氨水滴入Al2(SO4)3溶液 | 少量Al2(SO4)3溶液滴入浓氨水 |
| C | 0.1mol Cl2通入含0.2mol FeBr2的溶液 | 0.3 molCl2通入0.2molFeBr2溶液中 |
| D | 过量BaCl2溶液与少量Na2SO4溶液相混合 | 少量Ba(NO3)2溶液与过量MgSO4溶液相混合 |
12.下列表格中的各种情况,可以用下面的图象曲线表示的是
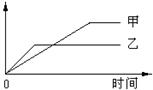
| 反应 | 纵坐标 | 甲 | 乙 | |
| A | 等质量钾、钠分别与足量水反应 | H 2质量 | 钠 | 钾 |
| B | 相同质量氨,在同一容器中 2NH3 | 氨气的转化率 | 500℃ | 400℃ |
| C | 在体积可变的恒压容器中,体积比1:3的N2、H2,N2+3H2 | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
| D | 2molSO2与lmolO2,在相同温度下2SO2+O2 | SO3物质的量 | 10个大气压 | 2个大气压 |
13.四种主族元素的离子aXm+、bYn+、cZn-、dRm-(a、b、c、d为元素的原子序数),
它们具有相同的电子层结构,若m>n,则下列关系能够成立的是
A. 原子序数:a>b>c>d B. a-b=n-m
C.元素非金属性:Z<R D.最高价氧化物对应水化物的碱性:X>Y
14.将多磷酸钠溶液通过氢型阳离子交换柱,进行Na+与H+的交换,得到多磷
酸,其结构为:
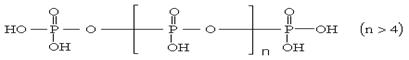
交换后的溶液用0.1mol·L-1的NaOH溶液滴定。在消耗NaOH溶液42.00mL和50.00mL时各有一个滴定终点。则下列判断正确的是
A.两端的__OH上的氢难电离 B.中间链上的__OH上的氢难电离
C.所有的__OH上的氢电离能力都一样 D.无法判断哪一部分__OH上的氢难易电离
15.恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g) + 2B(g) ![]() 2C(g) + xD(s) 的化学平衡状态,相关数据如下:
2C(g) + xD(s) 的化学平衡状态,相关数据如下:
M:3molA 2molB; 2min达到平衡,生成D1.2mol,测得从反应开始到平衡C的速率0.3mol·L-1·min-1
N:2molC ymolD; 达到平衡时c(A)=0.6mol·L-1。
下列推断的结论中不正确的是
A.x=2 B.平衡时M中c(A)﹤0.6mol·L-1
C.y﹥0.8 D.y﹤0.8
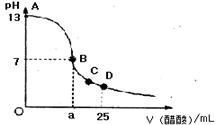 16.在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示,有关粒子浓度关系比较正确的
16.在25mL0.1mol/LNaOH溶液中逐滴加入0.2mol/L醋酸溶液,曲线如下图所示,有关粒子浓度关系比较正确的
A.在A、B间任一点,溶液中一定都有
c(Na+)>c(CH3COO—)>c(OH—)>c(H+)
B.在B点,a>12.5,且有
c(Na+)==c(CH3COO—)=c(OH—)==c(H+)
C.在C点:c(CH3COO—)>c(Na+)>c(H+)>c(OH—)
D.在D点:c(CH3COO—)十c(CH3COOH)==2c(Na+)
请将以上答案填入以下空格内
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 答案 | C | D | B | C | C | D | D | A |
| 题号 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 |
| 答案 | B | BC | BD | A | A | A | BD | CD |