高考化学学业水平测试模拟试卷
本试卷分为第I卷和第II卷两部分。试卷1至6页。共100分。考试时间75分钟。
注意事项:
1. 答卷前,考生务必将本人的学校、班级、姓名、学号、考试号填在第II卷的密封线外和机读卡上。
2. 将第I卷答案用2B铅笔填涂在机读卡上,在试卷上答题无效。第II卷直接在试卷上作答。
3. 考试结束,请将机读卡和第II卷交给监考人员。
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 Al-27 S-32 Cl-35.5 Fe-56 Cu-64
第I卷(选择题,共69分)
一、本大题共17题,每题3分,共51分。在每题的四个选项中,只有一个选项是符合要求的。
1.下列各组物质中互为同素异形体的是
A.11H和12H B.CH3COOH和CH3OCH3
C. O2和O3 D.H2O和H2O2
2.将少量下列物质分别加入足量的水中,充分搅拌后能形成溶液的是
A.粉笔灰 B.冰块
C.食盐 D.色拉油
3.下列化学用语错误的是
A.NaCl的电子式![]() B.甲烷的结构式
B.甲烷的结构式 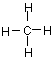
C.Mg原子结构示意图 ![]() D.乙烯的结构简式CH2=CH2
D.乙烯的结构简式CH2=CH2
4.下列化学反应属于吸热反应的是
A.碘的升华 B.生石灰溶于水
C.镁与稀盐酸反应 D.氢氧化钙与氯化铵晶体混合
5.下列各组离子在溶液中可大量共存的是
A.NH4+,SO42-,K+,OH- B.H+,Ba2+,NO3-,SO42-
C.K+,Cl-,CO32-,Na+ D.Ca2+,NO3-,Na+,CO32-
6.用NA表示阿佛加德罗常数,下列说法正确的是
A.22.4L O2的物质的量约为1mol
B.标准状况下,11.2L H2O的物质的量约为1 mol
C.1 L 1mol/L的NaOH溶液中Na+的物质的量为1 mol
D.0.1mol铁与足量的盐酸完全反应,铁失去的电子数为0.1NA
7.下列过程涉及化学变化的是
A.升华 B.分馏
C.盐析 D.变性
8.下列仪器常用于物质分离的是
A.量筒 B.天平
C.分液漏斗 D.容量瓶
9.硅在自然界最主要的存在形式是 ①硅 ②二氧化硅 ③硅酸盐
A.①② B.①③
C.②③ D.①②③
10.下列过程合乎实际并用于工业生产的是
A.钠在氯气中燃烧制氯化钠 B.氯化铵与氢氧化钙共热制氨气
C.浓盐酸与二氧化锰共热制氯气 D.氯气与石灰乳反应制漂白粉
11.下列化学变化不能一步实现的是
A.Na→Na2O B.Al→Al(OH)3
C.N2→NO D.SO2→SO3
12.铁是一种应用广泛的金属。下列有关铁的说法错误的是
A.铁与盐酸反应生成氯化铁与氢气 B.常温下,铁在浓硫酸中会发生钝化
C.铁在氧气中燃烧生成四氧化三铁 D.铁是一种银白色金属
13.1868年,俄国化学家门捷列夫制作出了第一张元素周期表,提示了化学元素间的内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是
A.元素周期表有七个周期 B.元素周期表有18个族
C.IA族的元素全部是金属元素 D.短周期是指第一、二、三、四周期
14.下列物质中熔点最高的是
A. 干冰 B.氯化钠
C.金刚石 D.汞
15.下列说法正确的是
A.医疗上常用碳酸钡作X射线透视肠胃的内服药剂,即钡餐
B.人体补碘,所有的食品都应加碘
C.由于近几十年来温室效应加剧,加速了古建筑的风化
D.硅的提纯与应用,促进了半导体元件与集成芯片的发展
16.下列关于糖的说法错误的是
A.淀粉是一种天然高分子化合物 B.糖都能水解
C.纤维素没有甜味 D.糖类是人体内能量的主要来源之一
17.下列关于油脂的叙述错误的是
A.油脂由C、H、O三种元素组成 B.油脂在碱性条件下不能发生水解反应
C.天然油脂的主要成份是高级脂肪酸甘油酯
D.工业上可以用油脂制造肥皂和油漆等化工产品
二、本大题包括“(一)化学与生活”和“(二)有机化学基础”两个模块各6题,每题3分,每个模块18分。每位考生只需选择其中一个模块作答,若两个模块均作答,则以第一个模块计算成绩。在每题的四个选项中,只有一个选项是符合要求的。
(一)化学与生活
18.下列所述情况可能引起污染的是
①含磷洗衣粉的大量使用 ②农业生产中农药的使用不当 ③工业废气的任意排放
A.①② B.①③
C.②③ D.①②③
19.下列关于生产、生活中的化学知识的叙述正确的是
A.用食醋可以帮助我们除去热水瓶的水垢(主要成分是CaCO3和Mg(OH)2)
B.“白色污染”主要是指由石灰造成的环境污染
C.铁只有在酸性条件下才能发生腐蚀
D.蛋白质只含C、H、O、N四种元素
20.磷酸钙陶瓷是一种新型无机非金属材料,它可以用于制造人造骨骼,这是利用了该材料的
A.机械功能 B.热功能 C.生物特性 D.光学特性
21.为了减少汽车尾气对大气造成的污染,目前市场上推出了使用乙醇汽油(在汽油中加入适量乙醇)的汽车。下列叙述错误的是
A.汽车使用乙醇汽油可以减少有害气体的排放 B.乙醇汽油是一种化合物
C.乙醇充分燃烧生成CO2和H2O D.用粮食发酵可制得乙醇
22.下列关于物质的使用合理的是
A.亚硝酸钠是常用的防腐剂
B.婴儿食品应添加着色剂,以增加婴儿对食物的兴趣
C.维生素C可防治坏血病,因而我们需要大量补充维生素C
D.药物可以帮助我们战胜疾病,但我们仍需合理用药
23.下列关于硅酸盐材料的说法错误的是
A.生活中常见的硅酸盐材料有玻璃、水泥、陶瓷
B.普通玻璃的主要成份是SiO2
C.陶瓷的主要原料是黏土
D.硅酸盐水泥以石灰石和黏土原料
 (二)有机化学基础
(二)有机化学基础
18.某有机物的结构式为它在一定条件下右能发生的反应有
①加成 ②水解 ③酯化 ④氧化 ⑤中和 ⑥消去
A.②③④ B.①③⑤⑥
C.①③④⑤ D.②③④⑤⑥
19.用式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为
A.3 B.4
C、.5 D.6
20.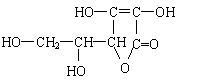 维生素C的结构简式为 ,有关它的叙述错误的是
维生素C的结构简式为 ,有关它的叙述错误的是
A、.是一个环状的酯类化合物 B.易起氧化及加成反应
C、.可以溶解于水 D.在碱性溶液中能稳定地存在
21.某有机化合物X,经过下列变化后可在一定条件下得到乙酸乙酯.则有机物X是
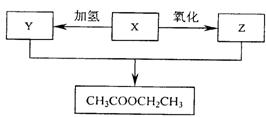
A.C2H5OH B.C2H4
C.CH3CHO D.CH3COOH
22.符合下列分子式的有机物没有同分异构现象的是
A.CH4 B.C12H22011
C.C4H10 D.C4H9
23.某有机物的结构式如图所示,其名称正确的是:
A.5-乙基-2-已烯 B.2-甲基庚烯
C.3-甲基-5-庚烯 D.5-甲基-2-庚烯
第Ⅱ卷(非选择题,共31分)
三、本大题包括“(一)化学与生活”和“(二)有机化学基础”两个模块各2题,每个模块12分。每位考生只需选择其中一个模块作答,若两个模块均作答,则以第一个模块计算成绩。
(一)化学与生活
24.(6分)“民以食为天”,人类生命活动所需的各种营养素主要来自于食物。
| 主食 | 米饭 |
| 副食 | 烧豆腐、红烧鱼 |
| 饮料 | 牛奶 |
| 你的补充 |
上表是小明制定的食谱,在食谱中,主食含有的营养素主要有 , 。小明制定的食谱中还缺乏的一种营养素是 。
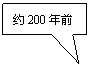
25. (6分)金属是一种重要的材料,人类的生活和生产都离不开金属,从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限:
 | |||||
 | |||||
 | |||||
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
(1)每年世界上钢铁的产量很高,但钢铁的腐蚀也给人类带来了巨大的损失,铁在潮湿的空气中锈蚀主要属于 腐蚀。铝的活动性比铁强,但铝在空气中却比铁表现出良好的抗腐蚀性,其原因是 。
(2)除金属材料外,人类还研发了许多种材料,如:塑料、合成橡胶、合成纤维等,它们属于 材料。
(二)有机化学基础
24. (3分)某芳香族化合物A的分子式为C7H6O2,溶于NaHCO3水溶液,将此溶液加热,能用石蕊试纸检验出有酸性气体产生。
(1) 写出化合物A的结构简式: ;
(2)根据题意写出化学反应方程式 。
25.(9分)为扩大现有资源的使用效率,在一些油品中加入降凝剂J,以降低其凝固点,扩大燃料油品的使用范围。J是一种高分子聚合物,它的合成路线可以设计如下,其中A的氧化产物不发生银镜反应:
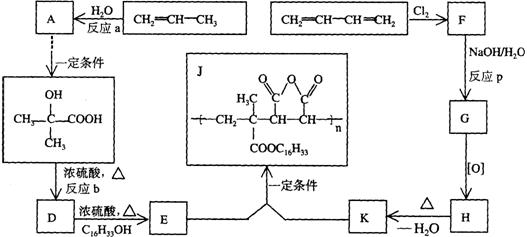
试写出:
(l)反应类型;a 、b 、P
(2)结构简式;F 、H
(3)化学方程式:D→E
E+K→J
四、本大题共3题,共19分。
26.(6分)氯气是一种重要的化工原料,在生产和生活中应用十分广泛。
已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O ,所以在实验室可用高锰酸钾固体和浓盐酸制氯气。
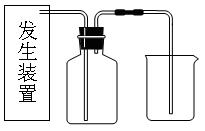
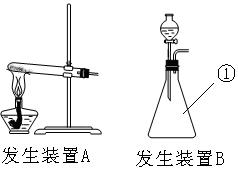
(1)请为该实验选择合适的发生装置 。(填A或B)
(2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,氧化剂是 。
(3)当集气瓶中收集满氯气时,可以观察到气体呈 色。
(4)工业上常用电解饱和食盐水制取氯气,试写出该反应的化学方程式:
。
(5)写出仪器①的名称 。
27.(4分)已知A是黑色固体,C和F是无色气体,D是红棕色气体。
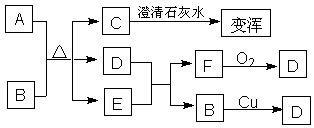
(1)写出C和D的化学式 、 。
(2)写出A和B反应的化学方程式: 。
28.(5分)有A、B、C、D短四种周期元素,它们的原子序数依次增大。A是自然界中相对原子质量最小的元素,B是自然界中含量最高的元素,D则是自然界中含量最高的金属元素,C与A同主族、与D同周期。
(1)写出A和D的元素符号 、 。
(2)A2B属于 化合物。(填离子或共价)
(3)比较C和D的原子半径 C D。(填“>”、“=”或“〈”)
(4)比较C和D的金属性C D。(填“>”、“=”或“〈”)
(5)将2.7克D单质溶于200 mL 1 mol・L-1的NaOH溶液中,计算生成的气体在标准状况下的体积为多少升?
参考答案及评分标准
参考答案
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | C | C | C | D | C | C | D | C | C |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | |
| 答案 | D | B | A | A | C | D | B | B |
《化学与生活》
| 题号 | 18 | 19 | 20 | 21 | 22 | 23 |
| 答案 | D | A | C | B | D | B |
《有机化学基础》
| 题号 | 18 | 19 | 20 | 21 | 22 | 23 |
| 答案 | C | D | D | C | A | D |
《化学与生活》
24.糖类 (2分) 水(2分) 维生素 (2分)
25.(1)电化学腐蚀(2分)铝表面形成了一层致密的氧化膜(2分)有机高分子材料(2分)
《有机化学基础》
24. (1) ![]() -COOH (1分) (2)
-COOH (1分) (2) ![]() -COOH + NaHCO3 →
-COOH + NaHCO3 →![]() -COONa + H2O +CO2↑ (2分)
-COONa + H2O +CO2↑ (2分)
25. (1)加成 (1分)消去 (1分)水解(或取代)(1分)
(2)![]()
![]() (2分)
(2分)
(3)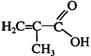 +C16H33OH
+C16H33OH ![]()
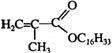 +H2O(2分)
+H2O(2分)
n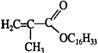 +n
+n 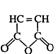
![]()
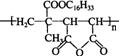 (2分)
(2分)
三.
26.(1)
B 1分 (2) KMnO4 1分 (3) 黄绿 1分
(4)
2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ 2分
(5)
锥形瓶 1分 。
2NaOH+H2↑+Cl2↑ 2分
(5)
锥形瓶 1分 。
27.(1)CO2 1分 NO2 1分
(2)C+4HNO3(浓)![]() CO2↑+4NO2↑+2H2O 2分
CO2↑+4NO2↑+2H2O 2分
28.(1) H 1分 、 Al 1分 (2)共价1分 (3) > 2分 (4) > 2分
(5) 3.36 L(2分)