专题复习:高三综合科化学实验
一:考试要求
1、 化学实验常用仪器的主要用途和使用方法
2、 化学实验基本操作
3、 常见气体实验室制法(包括所用试剂、仪器、反应原理和收集方法)
4、 常见物质(包括气体物质、无机离子)的分离、提纯、和鉴别
5、 化学实验的基本方法①根据实验现象,观察、记录、分析或处理数据,得出正确结论。②根据实验试题要求,设计基本实验方案。③能绘制和识别典型的实验仪器装置图。
二、最基本操作:
| 使用仪器 | 操作方法 | 注意事项 | |
| 药品的取用 | 药匙、纸槽、镊子、胶头滴管 |
固体 送入:依试管大小长短分别用药匙后端小匙、大匙、纸槽送入 | ① 用过的药匙应擦净备用 ② 若为块状物或密度较大颗粒应轻滑至管底 |
|
液体 量小:胶头滴管 | ① 试剂瓶盖仰放在桌面 ② 标签应对着掌心 ③ 瓶口紧贴仪器口 | ||
| 试剂的称量 | (称固体) 托盘天平 | ① 游码移到左端刻度尺零处,调节 天平零点 ② 称量物放左盘,砝码放右盘 ③ 称量完毕后,应将砝码放放砝码盒中,游码移回零处 | ① 称量物(特别是易潮解、易腐蚀)不能直接放在托盘上 ② 1g以下使用游码 |
| (量液体)量筒、移液管、滴定管 | 精确度要求不高用量筒 精确度要求较高用移液管或滴定管 | 读数时应平视,使液体凹液面最低点刻度和视线在同一水平线上 | |
| 加热 | 试管、铁架台、试管夹、酒精灯 | 加热盛液体试管:用试管夹夹在距管口1/3处,试管口向上倾斜45° | 管口不得对着别人和自已 |
| 加热盛固体试管:用铁架台和铁夹固定在距管口1/3处,管口稍向下倾斜 | 先均匀加热,再固定加热 | ||
| 蒸发皿、坩埚、坩埚钳 | 置于铁圈或三角架上,用酒精灯外焰直接加热 | 移取时要用坩埚钳 | |
| 烧杯、石棉网、烧瓶、锥形瓶 | 用铁架台和铁夹固定或置于三角架上,垫石棉网加热 | 给烧瓶加热有时要加沸石或碎瓷片 | |
| 溶解 | 烧杯、烧瓶、玻棒、导管、漏斗 | 固体溶解:用粉碎、搅拌、振荡和加热等方法来加速溶解。溶解度较小的气体,将导管插入水底部,极易溶于水的气体,将导管口置于液面上或倒置一漏斗,漏斗边缘刚好浸没在液面下 | 严禁用量筒、容量瓶等量器来溶解药品 |
三、基本操作
1、试纸的使用
试纸的种类很多。常用的有红色石蕊试纸、蓝色石蕊试纸、pH试纸、淀粉碘化钾试纸等。(l)在使用试纸检验溶液的性质时,一般先把一小块试纸放在表面皿或玻璃片上,用沾有待测溶液的玻璃棒点试纸的中部,观察颜色的变化,判断溶液的性质。(2)在使用试纸检验气体的性质时,一般先用蒸馏水把试纸润湿。粘在玻璃棒的一端,用玻璃棒把试纸放到盛有待测气体的试管口(注意不要接触),观察试纸的颜色变化情况来判断气体的性质。 注意:使用pH试纸不能用蒸馏水润湿。
2、溶液的配制(配制一定物质的量浓度的溶液)
计算:算出固体溶质的质量或液体溶质的体积。
称量:用托盘天平称取固体溶质质量或用量简量取所需液体溶质的体积。
溶解:将固体或液体溶质倒入烧杯中,加入适量的蒸馏水,用玻璃棒搅拌溶解,冷却到室温后,用玻璃棒将溶液引流注入容量瓶里。
洗涤(转移):用适量蒸馏水将烧杯及玻璃棒洗涤2-3次,将洗涤液注入容量瓶。振荡,使溶液混合均匀。
定容:继续往容量瓶中小心地加水,直到液面接近刻度2-3m处,改用胶头滴管加水,使溶液凹面恰好与刻度相切。把容量瓶盖紧,再振荡摇匀。
3.过滤 过滤是除去溶液里混有不溶于溶剂的杂质的方法。
过滤时应注意:
①一贴:将滤纸折叠好放入漏斗,加少量蒸馏水润湿,使滤纸紧贴漏斗内壁。
②二低:滤纸边缘应略低于漏斗边缘,加入漏斗中液体的液面应略低于滤纸的边缘。
③三靠:向漏斗中倾倒液体时,烧杯的夹嘴应与玻璃棒接触;玻璃棒的底端应和过滤器有三层滤纸处轻轻接触;漏斗颈的末端应与接受器的内壁相接触,例如用过滤法除去粗食盐中少量的泥沙。
4.蒸发和结晶 蒸发是将溶液浓缩、溶剂气化或溶质以晶体析出的方法。结晶是溶质从溶液中析出晶体的过程,可以用来分离和提纯几种可溶性固体的混合物。结晶的原理是根据混合物中各成分在某种溶剂里的溶解度的不同,通过蒸发减少溶剂或降低温度使溶解度变小,从而使晶体析出。加热蒸发皿使溶液蒸发时、要用玻璃棒不断搅动溶液,防止由于局部温度过高,造成液滴飞溅。当蒸发皿中出现较多的固体时,即停止加热,例如用结晶的方法分离NaCl和KNO3混合物。
5.蒸馏 蒸馏是提纯或分离沸点不同的液体混合物的方法。用蒸馏原理进行多种混合液体的分离,叫分馏。
6.分液和萃取 分液是把两种互不相溶、密度也不相同的液体分离开的方法。萃取是利用溶质在互不相溶的溶剂里的溶解度不同,用一种溶剂把溶质从它与另一种溶剂所组成的溶液中提取出来的方法。
7、中和滴定 ①准备过程:检查滴定管是否漏水;用水洗涤玻璃仪器;用少量标准液或待测液润洗装标准液的滴定管或装待测液的滴定管;装液体(在锥形瓶中放一定量待测液),排气泡、调零点并记录初始读数。当然也可以用待测液滴定标准液。
②滴定过程:
姿态:左手控制活塞或小球,右手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化。
滴速:逐滴滴入,当接近终点时,应一滴一摇。
终点:最后一滴刚好使指示剂颜色发生明显改变时即为滴定终点。记录读数
③数据处理及误差分析(略)
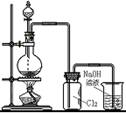
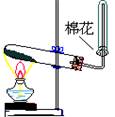
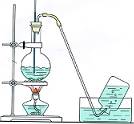
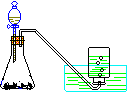
8.气体的制取(氯气 氨气 乙烯 乙炔)含实验原理、实验装置、气体干燥、气体收集
| 气体 | 氯 气 | 氨 气 | 乙 烯 | 乙 炔 |
| 原料 | ||||
| 实验 原理 | ||||
| 实验 装置 及类型 |
|
|
|
|
| 气体收集 | ||||
| 气体检验 |
9.离子的检验(Cl-、 SO42- 、NH4+)方法
| 离 子 | Cl- | SO42- | NH4+ |
| 检验 方法 |
四:练 习
1、下列操作中:(1)取用药品(2)溶解(3)过滤(4)蒸发。其中要使用到玻璃棒是( )
A、(1) B、(1)、(2) C、(1)、(2)、(3)、(4) D、(2)、(3)、(4)
2、下列仪器中不能受热的是 ( )
A、试管 B、烧杯 C、蒸发皿 D、量筒
3、在进行过滤操作时,除了使用铁架台、烧杯、玻璃棒外,还需要的仪器是( )
A、 洒精灯 B、托盘天平 C、蒸发皿 D、漏斗
4、下列有关使用托盘天平的叙述,不正确的是( )
A.称量前先调节托盘天平的零点 B.称量时左盘放被称量物,右盘放砝码
C.潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量,其他固体药品可直接放在天平托盘上称量
D.用托盘天平可以准确称量至0.1g
5、下列仪器中:①启普发生器②分液漏斗③滴定管④容量瓶⑤洗气瓶⑥胶头滴管,在使用前需要检验是否漏水的是( )
A.①②⑥ B.③④ C.①②③④ D.④⑤⑥
6、下列化学实验基本操作中,正确的是( )
A、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的量筒中并搅拌
B、用量筒量取液体时,视线与量筒内液体保持水平
C、用滴管滴加液体时,为防止液滴飞溅,滴管紧贴试管内壁
D、用用托盘天平称量物质时,称量物放在左盘,砝码放在右盘
7、用pH试纸测定某无色溶液的pH值时,规范的操作是( )
A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B.将溶液倒在pH试纸上,跟标准比色卡比较
C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较
D.在试管内放少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
8、实验室里需用480mL 0.1mol・L-1的硫酸铜溶液,现用容量瓶进行配制,以下操作正确的是( )。
A.称取7.68g硫酸铜,配成480mL溶液 C.称取8.0g硫酸铜,加入500mL水
B.称取12.0g胆矾配成500mL溶液 D.称取12.5g胆矾配成500mL溶液
9、用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中正确的是( )
A、酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B、锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液
C、滴定时,没有逐出滴定管下口的气泡
D、滴定时,眼睛应注视滴定管内液体液面的变化
10、下列各组物质可按溶解、过滤、蒸发的操作顺序,将它们分离的是( )
A、氧化铜和炭粉 B、食盐和泥沙 C、水和酒精 D、氯化银和硫酸钡
二、简答题
11、常见的分离方法的选择:
(1)固体与固体的混和物:①杂质易分解、易升华时,用 法,如碳酸钠中混有NaHCO3;②一种易溶,一种难溶,用 法,如NaCl中混有泥砂;③二者均易溶,但其溶解度随温度的影响不同,用 法,如NaCl中混有KNO3。
(2)液体与液体的混和物:①沸点相差较大时,用 法,如石油的分馏;②互不混溶时,用 法,如苯与水的混和物的分离;③在溶剂中的溶解度不同时,用 法,如用CCl4萃取碘水中的碘。
12、根据下列实验装置图回答(装置用代号表示)
①实验室制氧气时,应选用的发生装置是 ;制氢气时应选用的发生装置是 ,制二氧化碳时应选用的发生装置是 ,检验二氧化碳气体可选用D装置,
其装置中盛放的试剂一般是 。
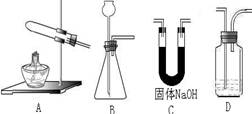 ②用锌粒和浓盐酸反应制氢气,将制成的气体通入硝酸银,有白色沉淀,说明氢气中含有(写化学式) ,反应方程式为 ,若要制出纯净的氢气,除发生装置外还应选用的一种装置是 ;该装置中药品的作用是 。13
②用锌粒和浓盐酸反应制氢气,将制成的气体通入硝酸银,有白色沉淀,说明氢气中含有(写化学式) ,反应方程式为 ,若要制出纯净的氢气,除发生装置外还应选用的一种装置是 ;该装置中药品的作用是 。13
实验室常用氯酸钾与二氧化锰混合加热制氧气,反应的化学方程式 。
参考答案:1-10:DDDCC DCDBB 11:加热 过滤 结晶 蒸馏 分液 萃取
12:①A B B,澄清石灰水 ②HCl HCl+AgNO3==AgCl↓+HNO3 C 除去H2中的HCl和水 2KClO3==2KCl+3O2↑