第三章 有机化合物
第四讲 基本营养物质
复习重点:糖类、油脂和蛋白质组成的特点;糖类、油脂和蛋白质的主要性质。
复习难点:葡萄糖与弱氧化剂氢氧化铜的反应;油脂的水解反应。
知识梳理
一、糖类
从结构上看,它一般是__________________的物质。 糖的分类: __糖 __糖 __糖。
1、 葡萄糖: 白色晶体 溶于水 不及蔗糖甜(葡萄汁 甜味水果 蜂蜜),分子式: ____ (180) 最简式: ___ (30)符合此简式的有 甲醛、乙酸、甲酸甲酯等。结构简式: _____________ 或_____________。
化学性质:
①还原性:银镜反应:________________;
与新制Cu(OH):浊液反应:________________;
②加成反应:能与H2加成生成己六醇________________;
③酯化反应:________________;
④发酵反应:________________;
⑤生理氧化:1 mol葡萄糖完全氧化生成液态水时,放出约2804 kJ的热量,是维持人体生命活动所需要的能量,其反应热化学方程式为:________________。
2、双糖―蔗糖
低聚糖: 糖类水解后生成几个分子单糖的糖.双糖、三糖等. 其中最重要的是双糖(蔗糖和麦芽糖)。蔗糖与麦芽糖的比较:
| 蔗糖 | 麦芽糖 | |
| 分子式 | C12H22011 | |
| 结构差异 | 不含醛基 | 含醛基 |
| 来源 | 在植物体内由葡萄糖、果糖缩合生成。
(果糖) (葡萄糖) | 淀粉水解糖化而成。
淀粉 (麦芽糖) |
| 性质差异 | ①不显还原性,不发生银镜反应 | ①有还原性能发生银镜反应 |
| ②可水解,生成一分子果糖和一分子葡萄糖 | ②可水解,生成二分子葡萄糖 | |
| ③有甜味 | ③有甜味,但不如蔗糖甜 | |
3、淀粉:
定义:多糖是由很多个单糖分子按照一定方式,通过在分子间脱去水分子而成的多聚体。因此多糖也称为多聚糖。一般不溶于水,没有甜味,没有还原性。淀粉与纤维素的比较:
|
| 淀粉 | 纤维素 |
| 分子组成 | (C6H1005) | (C6H1005)(与淀粉分子式中的n是不同的值) |
| 结构特点 | 几百个到几千个葡萄糖单元构成的高分子化合物,有直链及支链结构 | 几千个葡萄糖单元构成的高分子化合物,与淀粉 不是同分异构体。分子的一个结构单元含三个醇羟基 |
| 物理性质 | 白色粉末状物质。不溶于冷水,在热水里淀粉颗粒会膨胀破裂,有一部分淀粉会溶解在水里,另一部分悬浮在水里,形成胶状淀粉糊 | 白色、无臭、无昧的物质,不溶于水,也不溶于一般有机溶剂 |
| 化学性质 | 1.不与银氨溶液发生银镜反应。不显还原性,是一种非还原性糖; 2.在稀酸作用下发生水解,最终产物是葡萄糖: 在人体内也水解为葡萄糖: 3.淀粉遇碘后变蓝色 | 1.不与银氨溶液发生银镜反应,不显还原性,是一种非还原性糖; 2.在酸作用下水解,最终产物是葡萄糖,但比淀粉水解困难(需水浴加热,用70%的H2S04催化): 3.与硝酸发生酯化反应
|
二、油脂
1.油脂的组成与结构
油脂属于 类。是 和 生成的 。包括: 。脂肪:由 的高级脂肪酸甘油酯组成;油:由 的高级脂肪酸甘油酯组成,油脂的结构可表示为:______________。R1、R2、R3代表烃基,R1、R2、R3相同的油脂为 甘酯,不相同的为 甘油酯。
2.油脂的性质(1)物理性质:密度比水 , 溶于水,易溶于有机溶剂。
(2)化学性质 :①油脂的氢化(硬化 、 ),反应方程式为:,
![]()
|
![]()
![]()
![]() C17H33一COOCH +3 H2 C17H35―COOCH
C17H33一COOCH +3 H2 C17H35―COOCH
![]() C17H33― COOCH2
C17H35―COOCH2
C17H33― COOCH2
C17H35―COOCH2
②油脂的水解:油脂在酸性条件下水解不完全,在碱性条件下可完全水解。如:
![]() C17H35― COOCH2
H+
C17H35― COOCH2
H+
![]() C17H35― COOCH + 3H2O
C17H35― COOCH + 3H2O ![]()
C17H35― COOCH2
![]()
![]() C17H35― COOCH2
C17H35― COOCH2
![]()
![]() C17H35― COOCH + 3NaOH
C17H35― COOCH + 3NaOH
C17H35― COOCH2
(皂化反应)
注意:工业上利用皂化反应制肥皂。肥皂的主要成分是高级脂肪黢钠。油脂水解后,为使肥皂和甘油充分分离,采用盐析的方法,即加入食盐细粒,使肥皂析出。
三、蛋白质
1.氨基酸(1)结构:氨基酸是一种含氮有机物,分子中含有羧基(一COOH),也含有氨基(-NH2),天然氨基酸都是 。
(2)性质
①两性
![]()
![]()
![]() R-CHCOOH+HCl
R-CHCOOH
R-CHCOOH+HCl
R-CHCOOH
NH2 NH2C1
![]()
![]()
![]() R―CHCOOH +NaOH R- CHCOONa +H2O
R―CHCOOH +NaOH R- CHCOONa +H2O
NH2 NH2
②缩合反应
![]()
2.蛋白质
(1)定义:蛋白质是由不同的氨基酸(天然蛋白质所含的都是α一氨基酸)经缩聚后形成的高分子化合物。
(2)结构特点:与氨基酸相似,分子中存在着氨基(NH2)和羧基(-COOH),是两性物质,蛋白质溶液是胶体。
(3)化学性质①两性:与氨基酸相似。②水解:最后得到多种氨基酸
![]()
③盐析:提纯蛋白质
少量Na2SO4、(NH4)SO4可促进蛋白质的溶解,浓的上述无机盐溶液可降低蛋白质的溶解度,盐析是可逆的。
④蛋白质的变性 :蛋白质在 、 、 、 、 、 、 等的作用下发生变性,蛋白质的变性是不可逆的。
⑤颜色反应:某些具有苯环结构的蛋白质遇浓HNO3变性,产生黄色不溶物。
⑥灼烧气味:灼烧蛋白质产生烧焦羽毛的气味。
(4)蛋白质的鉴别①颜色反应。 ②灼烧,闻气味。如鉴别毛料和棉料、毛纤等。
疑难点拨
一、比较蛋白质的盐析、变性与胶体的凝聚
|
| 盐 析 | 变 性 | 胶体凝聚 |
| 概 念 | 蛋白质溶液中加浓无机盐溶液,使蛋白质析出 | 蛋白质在某些条件作用下凝聚,丧失生理活性 | 胶体中加入强电解质,不同电荷的胶体或加热而使之凝聚成大颗粒 |
| 对 象 | 高分子等(如蛋白质等) | 高分子(如蛋白质) | 带电的胶粒 |
| 变化条件 | 浓无机盐溶液 | 受热、紫外线、强酸、强碱、重金属盐,某些有机物等 | 强电解质,不同电荷的胶体,加热 |
| 变化实质 | 物理变化(溶解度降低) | 化学变化 | 物理变化 |
| 变化过程 | 可逆 | 不可逆 | 不可逆 |
| 用 途 | 分离,提纯 | 杀菌,消毒等 | 鉴别,分离等 |
二、酯和油脂的比较
| 酯 | 油脂 | ||
| 油 | 脂 | ||
| 组成 | 有机酸或无机酸与醇类反应的生成物 | 高级不饱和脂肪酸甘油酯 | 高级饱和脂肪酸的甘油酯 |
| 状态 | 常温下呈液态或固态 | 常温下呈液态 | 常温下呈固态 |
| 存在 | 花草或动植物体内 | 油料作物的籽粒中 | 动物脂肪中 |
| 实例 | CH3COOC2H5 | (C17H33C00)2C3H5 | (C17H35COO)3C3H5 |
| 联系 | 油和脂统称油脂,均属于酯类,含相同的酯基 | ||
三、蛋白质盐析和变性的比较
| 盐 析 | 变 性 | |
| 变化条件 | 浓的(钾、钠、铵)盐 | 受热、紫外线、酸、碱、重金属盐、甲醛 |
| 反应类别 | 物理变化 | 化学变化 |
| 变化过程 | 可逆 | 不可逆 |
| 用途 | 分离、提纯蛋白质 | 杀菌、消毒 |
四、硝基化合物与硝酸的无机酯的区别
| 硝基化合物 | 硝酸的无机酯 | |
| 定义 | 硝基-N02直接与烃基碳相连接的化合物 | -N02通过氧原子与烃基相连,即 R-0-N02 |
| 实例 | CH3CH2-N02硝酸乙烷 C6H5-N02硝基苯 | CH3CH2-0-N02 硝酸乙酯 |
五、淀粉、纤维素水解实验的注意问题
(1)淀粉、纤维素水解都用H2SO4做催化剂,但淀粉用 20%H2SO4,纤维素用90%H2SO4,均需微热;(2)检验产物时,必须用NaOH溶液中和过量的酸,才能用银氨溶液或新制Cu(OH)2,进行检验。
(3)淀粉是否发生水解的判断:利用淀粉遇碘变蓝的反应和其水解最终产物葡萄糖能发生银镜反应来判断淀粉是否发生水解和水解进行程度。如淀粉没有水解,则不能发生银镜反应;如淀粉已完全水解,则遇碘不能变蓝色;如既能发生银镜反应,又能遇碘变蓝色,则说明淀粉仅部分水解。
典例剖析
【例1】下列物质中,在一定条件下既能发生银镜反应,又能发生水解反应的是( )
A、甲酸甲酯 B、蔗糖 C、葡萄糖 D、麦芽糖
解析:蔗糖不显还原性;蔗糖发生水解反应能生成葡萄糖和果糖,其产生物能发生银镜反应。甲酸甲酯、麦芽糖均能水能,且分子中均含有醛基。故能发生银镜反应。答案: A、D
【例2】将蔗糖与稀H2SO4共煮后,向溶液中加入新制Cu(OH)2,加热至沸腾一直未见红色沉淀产生,其原因是________________。
解析:水解反应中稀H2SO4是催化剂,性质不变,加入的Cu(OH)2被H2SO4溶解生成CuSO4,无法发生Cu(OH)2与醛基的反应。答案:未加NaOH溶液中和酸,酸溶解了Cu(OH)2。
【例3】下列关于油脂的叙述不正确的是( )
A、油脂属于酯类 B、油脂没有固定的熔、沸点
C、油脂是高级脂肪酸甘油酯 D、油脂都不能使溴水褪色
解析:从油脂的定义、结构特点来分析,油脂是高级脂肪酸甘油酯,所以A、C正确。油脂为混合物,没有固定的熔、沸点,所以B也正确。油酸甘油酯与溴加成为使溴水褪色,所以D不正确答案:D。
【例4】低聚糖中的乳糖是一种二糖,棉子糖是一种三糖。乳糖水解生成互为同分异构体的葡萄糖和半乳糖;棉子糖水解可生成蔗糖和半乳糖。推断乳糖的分子式为: 。若棉子糖发生水解的最终产物都是单糖,该糖水解的化学方程式为: 。
解析: 已知乳糖是二糖。水解后生成的半乳糖和葡萄糖互为同分异构体,即二者的分子式均为C6H12O6联系所学蔗糖水解的反应,蔗糖也是二糖。可将它的分子视为一个葡萄糖分子和一个果糖分子脱一分子水时的缩合产物。由此推断乳糖脱去一分子时的聚合产物,其分子式应为C12 H22O11。进一步推理,一个三糖分子应是由一分子二糖一分单糖脱一分子水的缩合产物。根据题给棉子糖水解生成蔗糖和半孔糖的反应,可知棉子糖的分子式为:
![]() C12H22O11+C6H1206一H20
C18H32016
C12H22O11+C6H1206一H20
C18H32016
(蔗糖) (半乳糖) (棉子糖)
再由题意,棉子糖水解的最终产物都是单糖。可知蔗糖又继续水解成为葡萄糖和果糖,所以棉子糖水解的化学方程式为:
![]() C18H32016+2H2O C6H1206 + C6H1206 + C6H1206
C18H32016+2H2O C6H1206 + C6H1206 + C6H1206
(棉子糖) (半乳糖) (葡萄糖) (果糖)
答案:C12 H22O11 、
![]() C18H32016+2H2O
C6H1206 + C6H1206 + C6H1206
C18H32016+2H2O
C6H1206 + C6H1206 + C6H1206
(棉子糖) (半乳糖) (葡萄糖) (果糖)
【例5】某同学为了检验淀粉的水解情况,设计了如下三个实验方案:
方案甲:淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 溶液变蓝,结论:淀粉未水解;
溶液变蓝,结论:淀粉未水解;
方案乙:淀粉溶液![]() 水解液
水解液![]() ,无银镜生成;
,无银镜生成;
结论:淀粉未水解;
方案丙:淀粉溶液![]() 水解液
水解液![]() 中和液
中和液![]() 红色沉淀
红色沉淀
结论:淀粉已完全水解。
根据以上操作、现象判断结论是否正确,不正确的请说明原因。
解析:淀粉水解程度的判断,应注意检验产物中是否生成葡萄糖,同时还要确定淀粉是否还存在,另外应特别注意,检验葡萄糖前要中和水解液的酸性。
答案:(1)甲不正确。原因是未检测葡萄糖。(2)乙不正确。原因是未中和水解液的酸性,不能检测出葡萄糖是否存在。(3)丙不正确。原因是证明淀粉发生了水解,是否完全水解还需加I2检验淀粉是否存在,如不变蓝,则水解完全。
【例6】 (2002・春・京皖)在某些酶的催化下,人体内葡萄糖的代谢有如下过程:
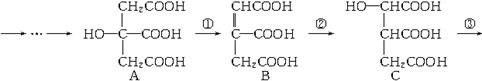 |
葡萄糖
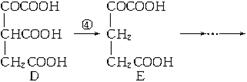
请填空:
(1)过程①是________反应,过程②是________反应。过程③是________反应(填写反应类型的名称)。
(2)过程④的另一种生成物是________(填写化学式)。
(3)上述物质________和________互为同分异构体(填写字母代号)。
解析:(1)小题是考查有机反应的基本类型,要求对有机反应的基本概念非常熟悉,根据概念进行判断: ①是消去反应,②是加成反应,③是氧化反应。根据质量守恒可以知道,④的另一种产物应该是CO2;其中,A和C互为同分异构体。答案:(1)①消去;②加成;③氧化。(2)CO2 (3)A、C。
【例7】 (2002・全国高考题)L一多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下:
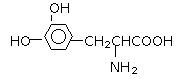
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果。下列关于L-多巴酸碱性的叙述正确的是( )
A.既没有酸性,又没有碱性 B.既具有酸性,又具有碱性
C.只有酸性,没有碱性 D.只有碱性,没有酸性
解析:从L-多巴的结构式可知,分子中含有羧基、酚羟基可推知化合物具有酸性,含有氨基可推知化合物具有碱性。答案:B。
知能训练
一、选择题
1. (2003年上海,1)下列物质一定不是天然高分子的是 ( )
A.橡胶 B.蛋白质 C.尼龙 D.纤维素
2. (2003年上海,2)上海环保部门为了使城市生活垃圾得到合理利用,近年来逐步实施了生
活垃圾分类投放的办法。其中塑料袋、废纸、旧橡胶制品等属于…( )
A.无机物 B.有机物 C.盐类 D.非金属单质
3.生命起源的研究是世界性科技领城的一大课题。科学家认为生命起源的第一层次是产生了
与硝基化合物可能是同分异构体的物质,这类物质是 ( )
A.醇 B.羟酸 C.氨基酸 D.糖
4.下列说法中不正确的是 ( )
A.胶体都可产生电泳现象 B.糖类可看作是烃的衍生物
C.淀粉和纤维素都是混合物 D.不只是蛋白质才具有盐析的性质
5.科学报道,常吃盐腌莱者比不吃者得胃癌的相对危险性高5~6倍,这是因为在无氧条件下
发酵时( )
A.硝酸盐被还原成为亚硝酸盐 B.蛋白质被分解为亚硝胺类
C.纤维素分解为葡萄糖 D.Na+和C1-离子浓度增加
6.(2000年汕头普通高校招生模拟二) 面粉的生产车间必须严禁吸烟,主要的目的是( )
A.避免烟尘杂入面粉 B.保护工人健康
C.防止污染环境 D.防止发生爆炸
7.变质的粮食中所含的较强的致癌物质是( )
A・硫化物 B.黄曲霉素 C.铅化合物 D.亚硝酸盐
8.衬衣领口因汁渍而产生的黄斑的主要成分是 ( )
A.食盐 B.淀粉 C.碱类 D.蛋白质
9.区别植物油和矿物油的正确方法是 ( )
A.加酸性高锰酸钾溶液,振荡 B.加NaOH溶液・煮沸
C.加新制Cu(OH):悬浊液,煮沸 D.加溴水,振荡
10.食品店里出售的冰淇淋是硬化油,它是以多种植物油为原料来制取的,制作过程发
生的反应是 ( )
A.水解 B.加聚 C.加成 D.氧化
11.用石灰水保存鲜蛋是一种化学保鲜法。石灰水能保存鲜蛋的原理是( )
①石灰水具有强碱性,杀菌能力强 ② Ca(OH)2能与鲜蛋呼出的C02反应,生成CaCO3薄膜,起保护作用③石灰水是电解质溶液,能使蛋白质凝聚 ④石灰水能渗入蛋内中和酸性物质
A.①② B.③④ C.②④ D.①③
12.下列实验不能获得成功的是 ( )
A.用浓溴水除去苯中混有的苯酚杂质
B.淀粉与稀H2S04充分反应后,加入适量新制Cu(OH)2溶液,加热产生红色沉淀
C.只用一种试剂鉴别Na2S溶液、NaCl溶液、Na2SiO3溶液、Na2C03溶液
D.用饱和Na2CO3溶液除去乙酸乙酯中混有的乙酸杂质
13.不属于糖类化合物,但和葡萄糖中碳、氢、氧的质量分数均相同,且能发生银镜反应的物
质是 ( )
A.乙醛 B.甲醛 C.甲酸甲酯 D.乙酸
14.实验室区别下列物质,选用的试剂正确的是 ( )
A.苯和乙烷(发烟H2S04) B.植物油与矿物油(氢氧化钠溶液)
C.乙醛和丙醛(溴水) D.Na2CO3和NaHC03(石灰水)
15.分子量为300以下的某一元脂肪酸1.0g可与2.7g碘完全加成,也可被0.2gKOH所中和,由此推测该脂肪酸的准确分子量为 ( )
A.282 B.280 C.278 D.无法确定
16.“喷水溶液法”是最近日本科学家研制出的一种使沙漠变绿洲的新技术,它是先在
沙漠中喷洒一定量的聚丙烯酸酯水溶液,水溶液中的高分子与沙土粒子结合,在地表下30~50cm处形成一个厚0.5cm的隔水层,即能阻止地下的盐分上升,又有拦截、蓄积雨水的作用.下列对聚丙烯酸酯不正确的说法是 ( )
A.单体的结构式为CH2=CH―COOR B.在一定条件下能发生加成反应
C.在一定条件下能发生水解反应 D.没有固定的溶沸点
17.把2g甲醛气体溶于6g冰醋酸中,再加入4g果糖得混合物甲;另取5g甲酸甲酯和9g葡萄
糖相混合,得混合液乙;然后将甲和乙两种混合液再按7:4的质量比混合得丙,则丙中碳元素的质量分数是 ( )
A.20% B.35% C.40% D.55%
18.1924年,中国药物学家陈克恢检验并证实了麻黄素有平喘作用,于是从中药麻黄中提取麻
黄素作为平喘药一度风靡世界。将10g麻黄素完全燃烧,可得26.67gCO2,8.18gH2O,同时测得麻黄素中含氮8.48%。据此,判断麻黄素的分子式为 ( )
A.C2H3NO B.C10H15N203 C.C10H15NO D.C20H30N20
二、填空题
19.为了进行Ⅰ项实验,从Ⅱ项中选出一种试剂,从Ⅲ项中选出一种合适的操作方法:
| I实验 | Ⅱ试剂 | Ⅲ操作 | 答案 | |
| (1)除去苯中的苯酚 | A.CaO | a.分馏 | (1) | |
| (2)除去工业酒精中的水 | B.Na2C03溶液 | b.蒸馏 | (2) | |
| (3)除去乙酸乙酯中的乙酸 | C.NaCl | C.过滤 | (3) | |
| (4)除去肥皂中的甘油 | D.NaOH | d.萃取 | (4) | |
20.下图为硬脂酸甘油脂在碱性条件下水解的装置图。进行皂化反应的步骤如下:
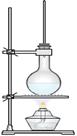
(1)在圆底烧瓶中装入7~8g的硬脂酸甘油脂,然后再加入2~3g 的氢氧化钠、5mL水和lOmL酒精加入的酒精的作用为:
.
(2)隔着石棉网用酒精灯给反应的混合物加热约lOmin,皂化反应基本完成,所得混合物为 (填“悬浊液”或“乳浊液”或“溶液”或“胶体”)。
(3)向所得的混合物中,加入 ,静置一段时间后,溶液分为上下两层,肥皂在 层,这个操作称为 。
(4)图中长玻璃导管的作用为 。
(5)写出该反应的化学方程式: 。
21、下列物质中:
①NaHC03②NH4C1③CH3COONH4④C6H50H⑤C6H5ONa⑥H2N―CH(CH3)-COONa⑦H2N―CH2-COOH⑧HOOC--CH(CH3)-NH2・HC1其中只能与盐酸反应的是 ,只能与NaOH溶液反应的是: ,既能与盐酸反应又能与NaOH溶液反应的是 。(不能用任何符号隔开)。
22、丙氨酸在强酸性溶液中以阳离子存在,在强碱性溶液中,以阴离子形式存在,在pH
=6时,以两性离子存在。丙氨酸在水溶液中存在下列关系:
![]()
现在以Pt电极在下列介质中电解丙氨酸的水溶液:
(1)在强酸性溶液中,在 极,析出丙氨酸。
(2)在强碱性溶液中,在 极,析出丙氨酸。
(3)在pH=6时,阳极的电极反应式是 。
三、推断题
23.在课外实验中,某学生用蔗糖、碳铵、生石灰和硫酸四种药品从AgNO3(内含少量Fe3
+和A13+)溶液中提取银。如下图所示,请回答下列问题。
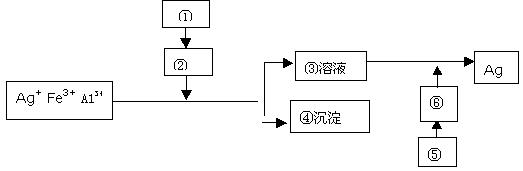
(1)写出方框中各物质的名称或化学式。
① ② ③ ④ ⑤ ⑥
(2)写出生成沉淀④的离子方程式:
、 。
(3)写出生成单质银的化学方程式:
四、计算题
24.有机物A仅含有C、H、N三种元素,其相对分子质量不超过200,其中氮元素的质
量分数为10.85%。
(1)有机物A的相对分子质量为 (取整数值)。
(2)写出A的所有可能的分子式 。
(3)关于A的说法正确的是
A.可能是芳香烃 B.可能是芳香族化合物
C.晶体的熔点可能很高 D.分子结构中可能只含有单键
25.生物学家预言21世纪也是木材化工生产的世纪。现在1 620t植物纯纤维素,理论
上可制得95%(质量分数)的酒精多少t?
参考答案:
1.C 2.B 3.C 4.A 5.A 6.D 7.B 8.D 9.BD 10.C 11.A 12.AB 13.BC 14.AB 15.C 16.B 17.C18.C
19.(1)Da(2)Ab(3)Ba(4)Cc
20.(1)溶解硬脂酸甘油酯(2)胶体 (3)食盐 上 盐析 (4)冷凝 (5)(C17H35COO)3
C3H5+3NaOH ![]() 3C17H35COONa+C3H5(0H)3
3C17H35COONa+C3H5(0H)3
21.⑤⑥;②④⑧;①③⑦
22.(1)阴 (2)阳 (3)40H-―4e- =2H20+02↑
23.(1)①NH4CO3、CaO②NH3 ③[Ag(NH3)2]OH④A1(OH)3、Fe(OH)3⑤蔗糖、稀硫酸⑥葡萄糖 (2)3NH3・H2O + A13+ ===== A1(OH)3↓ + 3NH4+ ;3NH3・H2O + Fe3+ ==== Fe(OH)3↓
![]() (3)CH2OH(CHOH)4CHO + 2[Ag(NH3)2]OH
CH2OH(CHOH)4COOH+2Ag↓+H2O+4NH3
(3)CH2OH(CHOH)4CHO + 2[Ag(NH3)2]OH
CH2OH(CHOH)4COOH+2Ag↓+H2O+4NH3
24.(1)129 (2)C9NH19 (3)BD
25.16.968t
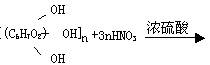
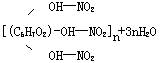 (纤维素三硝酸酯)
(纤维素三硝酸酯)