2005~2006学年上学期金山中学高一级期末考试
化学科试题
注意事项: 1.请将所有答案全部答在答题卷上,只上交答题卷;
2.可能用到的原子质量: N:14 O:16 Na:23 Al:27 Cl:35.5 Cu:64 Ba:137
第一卷(选择题,共60分)
一、选择题(每小题只有一个选项符合题意,每小题3分,共45分。)
1.下表是某城市空气质量每周公报的部分内容。对表中三个空气质量指标不会产生影响的是
| 项目 | 空气污染指数(API) | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒 | 52 | Ⅱ | 良 |
| 二氧化硫 | 7 | I | 优 |
| 二氧化氮 | 24 | I | 优 |
A.焚烧垃圾 B.使用含磷洗衣粉
C.汽车排放的尾气 D.用煤和石油产品作燃料
2.将表面已完全钝化的铝条,插入下列溶液中,不会发生反应的是
A.稀硝酸 B.稀盐酸 C.浓硝酸 D.氢氧化钠
3.新制氯水与久置的氯水相比较,下列结论不正确的是
A.颜色相同 B.前者能使有色布条褪色
C.都含有H+ D.加AgNO3溶液都能生成白色沉淀
4.漂白粉的有效成分是
A.次氯酸钙 B.氯化钙 C.次氯酸 D.次氯酸钙与氯化钙
5.下列气体不能用H2SO4干燥的是
A.CO2 B.NH3 C.SO2 D.HC1
6.自来水可用氯气消毒,某学生用这种自来水去配制下列物质溶液,会产生明显的药品变质问题的是
A.NaNO3 B.FeCl2 C.Na2SO4 D.AlCl3
7.下列物质受热分解后不留固体残渣的是
A.NaHCO3 B.NH4HCO3 C.KClO3 D.CaCO3
8.下列四种鉴别碳酸钠和碳酸氢钠的方法中可靠性最差的是
A.观察样品外观 B.在饱和溶液中滴入几滴酚酞
C.取少量的试样加热 D.分别取适量的样品加适量水溶解
9.SO2和Cl2都具有漂白性,若将等物质的量的这两种气体同时作用于潮湿的有色物质,可观察到有色物质
A.先褪色后复原 B.慢慢褪色 C.立刻褪色 D.颜色不褪
10.实验室在制备气体时,对某些气体来说,收集方法既可采用排水法,又可采用排空气法收集,下列气体中能同时采用上述两种收集方法的是
A.NH3 B.NO C.NO2 D.H2
11.在无色透明的溶液中可以大量共存的离子组是
A.H+、K+、Fe2+、NO3- B.OH-、Cl-、Na+、Mg2+
C.Al3+、K+、Cl-、NO3- D.Cu2+、NO3-、OH-、Cl-
12.取两份等量的铝粉,分别与足量的盐酸、浓氢氧化钠溶液反应,在相同状态下产生的气体体积之比是
A.1∶1 B.1∶2 C.1∶3 D.3∶2
13.下列五种有色溶液与SO2作用均能褪色,其实质相同的是
①品红溶液;②酸性KMnO4溶液;③溴水;④滴有酚酞的NaOH溶液;⑤含I2的淀粉溶液
A.①④ B.①②③ C.②③⑤ D.③⑤
14.将盛有N2和NO2 的混合气体的试管倒立于水中经过足够时间后,气体体积减少为原来的一半,则原混合气体中N2和NO2 的体积比是
A.1∶1 B.1∶2 C.1∶3 D.3∶1
15.在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶,则a和b分别是
| a(干燥气体) |
| |
| ① | NO2 | 水 |
| ② | CO2 | 4 mol・L-1NaOH溶液 |
| ③ | C12 | 饱和食盐水 |
| ④ | NH3 | l mol・L-1盐酸 |
A.①和② B.③和④ C.①和③ D.②和④
二、选择题(每小题有一至二个选项符合题意,每小题3分,共15分。)
16.关于钠的说法中错误的是
A.金属钠有强还原性,钠离子有弱氧化性
B.钠可以把钛、铌、钽等金属从它们的化合物的水溶液中还原出来
C.钠与Cl2反应,发出黄色火焰,并产生大量白雾
D.在自然界中,钠只能以化合态存在
17.下列混合气体通入水中后,有一种气体消失,一种气体体积增大的是
A.HCl和CO2 B.O2和F2 C.H2和H2S D.NO和NO2
18.下列离子方程式,正确的是
A.澄清石灰水中通入过量二氧化碳:Ca2+
+ 2OH- +CO2![]() CaCO3↓ + H2O
CaCO3↓ + H2O
B.碳酸钠溶液中加入二氧化硅:CO32- + SiO2![]() SiO32- + CO2↑
SiO32- + CO2↑
C.二氧化硅与烧碱溶液反应:SiO2 + 2OH-![]() SiO32- + H2O
SiO32- + H2O
D.硅酸与烧碱溶液中和:H2SiO3 + 2OH-![]() SiO32- + 2H2O
SiO32- + 2H2O
19.铜跟1mol/L的稀硝酸反应,若c(NO3-)下降了0.2mol/L,则c(H+)下降
A.0.8mol/L B.0.6mol/L C.0.4mol/L D.0.2mol/L
20.将过量的CO2通入下列溶液中,最终能产生沉淀的是
A.硅酸钠溶液 B.澄清石灰水 C.氯化钡溶液 D.偏铝酸钠溶液
第二卷(非选择题,共40分)
三、填空题(本题包括2小题,共11分)
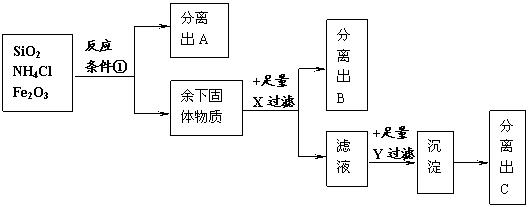 21.(5分)某混合物由NH4Cl、SiO2、Fe2O3三种物质组成,把这三种物质按下列列流程图进行分离:
21.(5分)某混合物由NH4Cl、SiO2、Fe2O3三种物质组成,把这三种物质按下列列流程图进行分离:
(1)写出下列物质的化学式:
A: B: X: Y:
(2)反应条件①是 。
22.(6分)已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应:
① A + H2O → B + C ② C + F → D ③ D + NaOH![]() F +
E + H2O
F +
E + H2O
写出各步反应的离子方程式,并指反应①的氧化剂和还原剂。
① 、氧化剂 、还原剂
②
③
四、实验题(本题包括2小题,共20分)
23.(10分)在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气反应的实验”。
 请回答该实验中的问题。
请回答该实验中的问题。
(1)写出该反应的化学方程式 ;
(2)实验前必须对整套装置进行的操作是 ;
(3)碱石灰的作用是 ;
(4)试管中收集到的气体是 ,如果要在A处玻璃管口处点燃该气体,则必须对该气体进行 ,检验这一操作的目的是 。
(5)如果改用排水集气法收集产生的气体,是否还需要用到碱石灰? ,理由是 。
24.(10分)运用所学知识,解决以下问题。
(1)浓硫酸与木炭粉在加热条件下的化学方程式为_________________________。
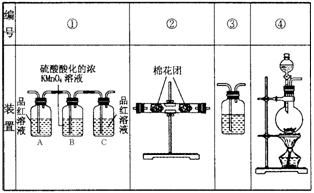
(2)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):__________→__________→__________→__________。
(3)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是__________,B瓶溶液的作用是________,C瓶溶液的作用是____________。
(4)装置②中所加的固体药品是_______________,可确证的产物是_______,确定装置②在整套装置中位置的理由是_____________________。
(5)装置③中所盛溶液是__________,可验证的产物是__________。
五、计算题(本题包括1小题,共9分)
25.将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。求:
(1)NO的体积为多少?
(2)NO2的体积为多少?
2005~2006学年上学期金山中学高一级期末考试
化学科试题・答题卷
第一卷(选择题,共60分)
选择题
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
第二卷(非选择题,共40分)
三、填空题(本题包括2小题,共11分)
21.(1)A: B: X: Y: (2) 。
22.① ;氧化剂 ;还原剂 ;
② ;
③ 。
四、实验题(本题包括2小题,共20分)
23.(1) ;
(2) ;
(3) ;
(4) , , 。
(5) , 。
24.(1)_______________________________________________________________________。
(2)__________→__________→__________→__________。
(3)________________________________;_______________________________________;
_________________________________________________________________________。
(4)_____________________________, _______________________________________,
________________________________________________________________________。
(5)________________________________________,_____________________________。
五、计算题(本题包括1小题,共9分)
25.将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为11.2L。求:
(1)NO的体积为多少?
(2)NO2的体积为多少?
2005~2006学年上学期金山中学高一级期末考试
化学科试题・参考答案及评分标准
第一卷 选择题(共60分,每小题3分,错选得0分,双选题只选一个且正确者得1分)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| B | C | A | A | B | B | B | A | D | D |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| C | A | C | C | D | BC | BD | CD | A | AD |
第二卷(非选择题,共40分)
21.(5分)NH4Cl、SiO2、HCl、NaOH(或NH4Cl、Fe2O3、NaOH、HCl);加热(每空1分)
22.(6分,每小题2分)
① 3NO2 + H2O![]() 2H+
+ 2NO3- + NO 氧化剂:NO2 ,还原剂:NO2
2H+
+ 2NO3- + NO 氧化剂:NO2 ,还原剂:NO2
③ H+ + NH3![]() NH4+
④ NH4+ + OH-
NH4+
④ NH4+ + OH-![]() NH3↑+ H2O
NH3↑+ H2O
23.(10分,每小题2分)
(1)3Fe+4H2O(g)![]() Fe3O4+4H2↑
Fe3O4+4H2↑
(2)检验装置的气密性
(3)干燥反应产生的气体
(4)H2;验纯;防止点燃时,氢气因含有氧气而爆炸。
(5)不需要;水槽中的水能将氢气中的水蒸气冷凝。
24.(10分,每小题2分)
(1)C+2H2SO4(浓)![]() 2SO2↑+CO2↑+2H2O↑
2SO2↑+CO2↑+2H2O↑
(2)④→②→①→③
(3)验证产物气流中是否有SO2;将SO2全部氧化吸收;确证产物中SO2已被B瓶溶液全部吸收;
(4)无水CuSO4(或变色硅胶);水蒸气;由于产物气流通过①、③时会带出水蒸气,所以②必须在①③之前;
(5)澄清石灰水;CO2
25.(9分)
解:设混合物气体中NO的物质的量为a,NO2的物质的量为b。
(1)4HNO3(浓)+Cu![]() Cu(NO3)2+2NO2↑+2H2O
Cu(NO3)2+2NO2↑+2H2O
随着反应的进行,硝酸的浓度逐渐减小,进行下列的反应
(2)8HNO3(稀)+3Cu![]() 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
由两个反应方程式中NO2与Cu,NO与Cu的计量关系,及已知数据可列方程组:
a+b=11.2L/22.4L・mol-1….…………………①
3a/2+b/2=32.64g/64g・mol-1….…………….②
解①②两个方程,得:a=0.26mol
b=0.24mol
所以NO的体积为:0.26mol×22.4 L・mol-1=5.8L
NO2的体积为:0.24mol×22.4 L・mol-1=5.4L
 b(液体)
b(液体)