第一章 《化学反应及其能量变化》
第二节 离子反应测验试卷 实验 班姓名
1.下列电离子方程式错误的是 ( )
A.NaHCO3=Na++H++CO32- B.NaHSO4=Na++H++SO42-
C.H2SO4=2H++SO42- D.KClO3=K++Cl-+3O2-
2.下列说法正确的是 ( )
A.CH3COOH与NaOH在相同条件下电离程度相等
B.NaCl溶液能导电是因为溶液中有Na+和Cl-
C.H2SO4在电流作用下在水中电离出H+ 和SO42-
D.检验CO32-或HCO3-离子的方法是取少许样品加入盐酸,将产生的气体通入澄清石灰水
3.下列离子方程式书写正确的是 ( )
A.碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O
B.硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓
C.氢氧化钠和少量氢硫酸反应 2OH-+H2S=S2-+H2O
D.铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu
4.下列物质的水溶液能导电而本身不是电解质的是 ( )
A.氨气 B.硫酸 C.二氧化碳 D.硫酸钠
5.不能用H++OH-=H2O表示的反应是 ( )
A.盐酸与氢氧化钾溶液反应 B.稀硫酸与氢氧化钡溶液反应
C.稀硝酸与氢氧化钠溶液反应 D.硅酸与氢氧化钠溶液反应
6.下列反应既是离子反应,又是氧化还原反应的是 ( )
A.二氧化硫与硫化氢作用生成硫和水
B.二氧化硫与氢氧化钠溶液作用生成亚硫酸钠
C.硫化氢通入氯化铁溶液中生成硫、氯化亚铁和盐酸
D.Zn粒与稀硫酸反应制取氢气
7.某无色溶液加入氯化钡溶液后有白色沉淀,再加稀硝酸沉淀不消失,则该溶液中( )
A.一定含有SO42- B.一定含有Ag+
C.至少含有SO42-或SO32-或Ag+ D.一定含有Ag+、SO42-
8.下列各组溶液不加任何试剂就能鉴别的是 ( )
A.盐酸、氢氧化钠、酚酞 B.氢氧化钠、氢氧化钡、硫酸
C.硫酸、碳酸钠、氢氧化钠 D.硫酸铜、盐酸、硫酸
9.下列各组中两个溶液间的反应,均可用同一离子方程式表示的是 ( )
A.CH3COOH和Na2CO3与CH3COOH和NaHCO3
B.AgNO3和HCl与Ag2SO3和HCl
C.BaCl2和Na2SO4 与Ba(OH)2与H2SO4
D.KOH和CH3COONH4与Ba(OH)2与NH4Cl
10.下列四种物质:Fe粉、石灰水、Na2CO3溶液、稀盐酸两两混合后,将发生的离子反应有( )
A.1个 B.2个 C.3个 D.4个
11.在某溶液中有K+、H+、SO42-、NO3-,则溶液中溶质的种类最多为 ( )
A.2种 B.3种 C.4种 D.5种
12.在酸性溶液中能大量共存而且为无色透明的溶液是 ( )
A.NH4+、Al3+、SO42-、NO3- B.K+、Na+、NO3-、SO32-
C.K+、MnO4-、NH4+、NO3- D.Na+、K+、HOO3-、NO3-
13.在碱性溶液中能大量共存且为无色透明的溶液是 ( )
A.K、Cl-、MnO4-、SO42- B.Na+、SiO32-、NO3-、CO32-
C.Na+、NO3-、SO42-、HCO3- D.Na+、SO42-、S2-、Cl-
14.和下列离子反应方程式相对应的化学方程式正确的是 ( )
A.Zn2++2OH-=Zn(OH)2↓ ZnCO3+2NaOH=Zn(OH)2↓+Na2CO3
B.Ba2++SO42-=BaSO4↓ Ba(OH)2+H2SO4=BaSO4↓+2H2O
C.Ag++Cl-=AgCl↓ AgNO3+NaCl=AgCl↓+NaNO3
D.Cu+2Ag+=Cu2++2Ag↓ Cu+2AgCl=2Ag+CuCl2
15.只能表示一个化学反应的离子方程式的是 ( )
A. Cu(OH)2+2HCl=CuCl2+2H2O Cu(OH)2+2H+=Cu2++2H2O
B. FeSO4+Ba(OH)2=Fe(OH)2↓+BaSO4↓ Fe2++SO42-+Ba2++2OH-=Fe(OH)2↓+BaSO4↓
C. Ba(OH)2+H2SO4=BaSO4↓+2H2O Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
D.2HCl+FeS=Fe2++H2S↑ 2H+FeS=Fe2++H2S↑
16.离子方程式Ba2++SO42-=BaSO4↑它表示①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应 ②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应 ③稀硫酸与可溶性钡盐溶液之间的反应 ④氢氧化钡溶液与稀硫酸反应 ( )
A.①② B.①②④ C.②③ D.①②③
17.对于离子以应H-+NH3=NH2-+H2↑的正确说法是 ( )
A.属于置换反应 B.被氧化的是H-
C.H2既是氧化产物又是还原产物 D.每产生1个分子H2必转移2个电子
18.在50g含1.17gNaCl和0.84g NaF溶液中滴入过量的AgNO3溶液,充分搅拌,静置,过滤、洗涤、干燥,称量得2.87g固体,由此可以得出正确结论是 ( )
A.氯离子只有一部分参加反应 B.氟离子只有一部分参加反应
C.氟化钠与硝酸银在溶液中无沉淀生成 D.氟化银难溶于水
19.今有三个氧化还原反应: ①2FeCl3+2KI=2 FeCl2+2KCl+I2 ②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
若某溶液中有Fe2+和I-共存,要氧化除去I-而又不影响Fe2+和Cl-。可加入的试剂是( )
A.Cl2 B.KMnO4 C.FeCl3 D.HCl
20.在xR2++yH++O2=MR3++nH2O的离子方程式中,对系数m和R3+的判断正确的是( )
A.m=4R3+是氧化产物 B.m=yR3+是氧化产物
C.m=2R3+是还原产物 D.m=yR3+是还原产物
二、填空题
21.将BaCl2溶液分别滴入到K2SO4、稀H2SO4溶液中,均有 产生,它们的离子方程式是 ,说明离子方程式不仅表示一定物质间的 ,而且表示了 离子反应。
22.向CuSO4溶液中滴加NaOH溶液,溶液中 离子的量减少, 离子的量增加, 离子的量没有变化,反应的离子方程式是 。
23.现有①铁片 ②NaCl ③氨水 ④醋酸 ⑤酒精 ⑥盐酸 ⑦浓H2SO4 ⑧KOH ⑨蔗糖 ⑩H2S,其中属于电解质的是 ,属于非电解质的是 ,属于强电解质的是 ,属于弱电解质的是 。
24.写出下列物质的电离方程式
(1)NaHSO4 (2)NaHCO3
(3)H2O (4)CH3COOH
(5)H2SO4 (6)Na2SO4
25.写出下列反应的化学方程式,属于离子反应的,写出离子方程式,属于氧化还原反应的标出电子转移的方向和数目
(1)氢氧化钡与稀硫酸反应
(2)碳酸钠溶液与盐酸反应
(3)铁片插到硝酸汞溶液中
(4)实验室制取氧气
(5)实验室制取二氧化碳
26.写出符合以下离子方程式的化学方程式各1个
(1)CO2+2OH-=CO32-+H2O __________________________________________
(2)HCO3-+H+=CO2↑+H2O _________________________________________
(3)CaCO3+2H+=Ca2++CO2↑+H20 _________________________________________
(4)Zn+Cu2+=Zn2++Cu _________________________________________
(5)H++OH-=H2O _________________________________________
27.完成下列离子方程式(给出物质的计量数不能改变)
(1)( )+2( )+( )+2( )=BaSO4↓+2H2O
(2)( )+Ca2++( ) =CaCO3↓+( )
(3)Cu2++( )+Ba2++( ) =BaSO4+Cu(OH)2↓
(4)( )+3H+=Fe3++( )
三、推断题
28.有A、B、C、D、E、F六种化合物,它们之间的反应关系如下所示:
① A+B→C+E ② C+NaOH→蓝色沉淀D+F
③
D![]() A+E
④ F+Ba(NO3)2→白色沉淀+NaNO3
A+E
④ F+Ba(NO3)2→白色沉淀+NaNO3
回答下列问题(1)写出它们的化学式:
A B C D E F 。
(2)写出①②③④反应的化学方程式,属于离子反应的只写离子方程式
①
②
③
④
29.有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl等混合而成,为检验它们做了如下实验: (1)将固体混合物溶于水,搅拌后得无色透明溶液
(2)往此溶液中滴加硝酸钡溶液,有白色沉淀生成
(3)过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解,试判断:
固体混合物中肯定有 ,肯定没有 ,可能有 ,对可能有的物质,可采用滤液中滴加 溶液方法来检验。
四、实验题
30.分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物 质 | 需加入的试剂 | 有关离子方程式 |
| HNO3(H2SO4) | ||
| Cu(Fe) | ||
| ZnSO4(CuSO4) | ||
| NaCl(Na2CO3) |
31.一学生设计了如下实验方法分离NaCl和CaCl2两种固体混合物
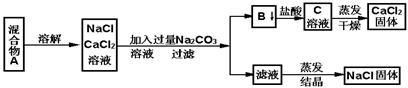
填空和回答下列问题
(1)B物质是 (写化学式)
(2)按此实验方案分离得到的NaCl,经分析含有杂质,是因为上述方案中某一步设计有毛病,这一步的正确设计方案应是 。
(3)若要测定该样品中NaCl和CaCl2的质量比,可称量干燥的B物质和另一物质的质量,这种物质是 。
五、计算题
32.在某一混合溶液中,经检测含有Na+、Fe3+、Cl-三种离子,有Na+质量为46g,Cl-质量为177.5g,问Fe3+质量为多少g?
33.向一价金属的碘化物中逐滴滴加AgNO3溶液,直到沉淀完全为止,已知生成的硝酸盐溶液质量等于原碘化物溶液的质量,求原硝酸银溶液的质量分数?
34.现有一定质量露置于空气中的KOH样品,测得其含KOH为90%,K2CO3为8%,H2O为2%,现向里加100g质量分数为14.6%的盐酸溶液恰好完全反应,问把溶液蒸发干可得晶体多少g?
参考答案
一、1.AD 2.D 3.BC 4.AC 5.BD 6.CD 7.C 8.AC 9.D 10.D 11.D 12.A 13.BD 14.C 15.BC 16.D 17.BC 18.C 19.C 20.AB
二、21.白色沉淀,Ba2++SO42-![]() BaSO4↓某个反应,所有同一类型 22.Cu2+,Na+,SO42- Cu2++2OH-
BaSO4↓某个反应,所有同一类型 22.Cu2+,Na+,SO42- Cu2++2OH-![]() Cu(OH)2↓ 23.2、4、8、10、5.9,2.8,4.10 24.略 25.略 26.略27.略 28.(1)CuO,H2SO4,CuSO4,Cu(OH)2,H2O,Na2SO4,(2)①CuO+2H+
Cu(OH)2↓ 23.2、4、8、10、5.9,2.8,4.10 24.略 25.略 26.略27.略 28.(1)CuO,H2SO4,CuSO4,Cu(OH)2,H2O,Na2SO4,(2)①CuO+2H+![]() Cu2++H2O ②Cu2++2OH-
Cu2++H2O ②Cu2++2OH-![]() Cu(OH)2↓ ③Cu(OH)2
Cu(OH)2↓ ③Cu(OH)2![]() CuO+H2O ④SO42-+Ba2+
CuO+H2O ④SO42-+Ba2+![]() BaSO4↓
BaSO4↓
29.Na2CO3,CuSO4 Na2SO4 CaCl2, NaCl,AgNO3稀HNO3
四、30.
| Ba(NO3)2 | Ba2++SO42- |
| HCl | Fe+2H+ |
| Zn | Zn+Cu2+ |
| HCl | 2H++CO32- |
31. (1)CaCO3 (2)加入适量盐酸至不产生气体 (3)A
五、32.56g 33.72% 34.29.8g