�߶���ѧ��ϰ(����������)
��I����ѡ���⣩
һ��ѡ����
1��2001��11�£�����Ϊ�������ɽ����Ŀֲ����ӣ�ʹ����һ����ΪBlu-82�ĸ���ȼ�Ͽ���ը��������Ҫ�ɷ�֮һ�ǻ������飨����ʽΪC2H4O�������йػ�������˵����ȷ���ǣ�
A�����������Ǽ�ȩ��ͬϵ� B���������Ļ������������������ֱ���ȫȼ�գ���������ͬ
C���������������ȶ�������ȼ�ա�D��������������ȩ��ͬ���칹�壬�ܷ���������Ӧ
2��2002��10�µף�����˹�ڽ�ȸ��Ժ����ʱʹ����һ����Чǿ����ʹҩ������̫Ŭ��������ͨ�����ƺ�����ѪҺѭ��ֹʹʹ�˸о���ľ������ʱ���»��Ժ�������
��ṹ��ʽ��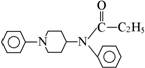 �� ����ڷ�̫Ŭ��˵������ȷ���ǣ�
�� ����ڷ�̫Ŭ��˵������ȷ���ǣ�
A������ʽΪC20H25ON2����B�������ڷ����廯���� C�����Լ��ԡ�D�������ڱ���ͬϵ��
3������ʵ����������ʵ��������������жϣ���ȷ����
A�����л��б��ӣ��ɼ���������Ũ��ˮ�ٽ��й���
B��������������ˮ�ⷴӦʱ���ô���ϡ��Һ�����������ռ�Ҫ��
C��1��2������������ռ���Ҵ���Һ��Ϻ�������ˮԡ�м����ܲ�����Ȳ
D����������Һ�е�������������ɫ����Һ
4����ȩ�������������ķ�Ӧ�ǣ���ȩ��CH3CH(OH)CH2CHO��CH3CH=CHCHO���������� �˹����еķ�Ӧ�ֱ�����
A���ӳɡ���ȥ���������������� B��ȡ������ȥ���ӳ�
C���ӳɡ���ȥ����ԭ���������� D����ԭ��ȡ�����ӳ�
5����֪����������ͬ���칹�塣�л���ף�C9H18O2��������������ˮ��Ϊ�Һͱ������л����ͬ��ͬѹ�£�ͬ�������Һͱ���������ռ�����ͬ����Ŀ��ܽṹ�У� ��
A��6�֡�������B��8�֡������� C��14�֡������� D��16��
6����֪��������Ա�����ǿ���������Զ���Ϊ����H+�������������������м�����ǿ������˳���� ��C6H5ONa ��CH3COONa�� ��C2H5ONa�� ��Na HCO3�� ��HCOONa ��NaOH
A���ۢޢ٢ܢڢݡ���B���ޢۢ٢ܢڢݡ� C���ݢڢ٢ܢۢޡ���D���ۢޢܢڢ٢�
7���Ͷ���Ľṹ��ʽΪCH3-CH=CH-COOH�����Т��Ȼ��� ����ˮ �۴�����Һ ��2-���� ���ữ�ĸ��������Һ���Ը�����ṹ�ص��ж���һ������������Ͷ��ᷴӦ�����������
A���ڢܢݡ���������B���٢ۢܡ�����������C���٢ڢۢ� D���٢ڢۢܢ�
8������������
������ˮ��Ӧ����
A����ϩ������������������ B�������顡����������C����ȩ�������������� D����������
9��ij���Ľṹ�ɱ�ʾΪ��CmH2m+1COOCnH2n+1
������m+n=5��������һ��ˮ����ᆳ��������ת����������һ��ˮ������ԭ��������
��A�������������� B����������������C������������� D���������
10����һ�������л�����ȼ�պ�IJ��ͨ��������ʯ��ˮ����ȫ���գ������˵ó���30g����Һ��������ԭʯ��ˮ����11.4g(�����Dz��������е����)�����л��������
A����ϩ���������� B���Ҵ�������C���Ҷ����������� D���������
11������ˮ��Һ����������ձ���ѧ�����Ƴ���һ��ʹɳĮ�������¼���,��������ɳĮ������һ�����ľ۱�ϩ����ˮ��Һ,ˮ��Һ�еĸ߷�����ɳ�����ӽ�ϣ��ڵر���30��50cm���γ�һ����0.5cm�ĸ�ˮ��,������ֹ���µ��η�����,�������ء������ˮ������.���жԾ۱�ϩ������˵������ȷ���ǣ�������
��������ĽṹʽΪCH2=CH-COOR�����¡���һ���������ܷ����ӳɷ�Ӧ
�á���һ���������ܷ���ˮ�ⷴӦ�������ġ�û�й̶����ܷе�
12���л���X��C��H��O����Ԫ�أ�����֪�����������ź�̼�������������ƺ�������������������������(���ۻ��ɱ�״���µ����)����X������������ܶȡ���X����������X�ķе㡣��ȷ��X�ķ���ʽ����Ҫ������������
A���ŢƢǢɡ�����B���ŢǢʡ������� C���ŢƢȡ�������D���ŢƢȢ�
13����Ȼά����P���ṹ��ͼ�������ڻ��������У�����һ��Ӫ��������������ά����P�������������
 A�����Ժ���ˮ��Ӧ����B�������л��ܼ���ȡ
A�����Ժ���ˮ��Ӧ����B�������л��ܼ���ȡ
C��������������������D��1molά����P���Ժ�4molNaOH��Ӧ
14��ŵ����һ��һԪ��������ʽΪC18H26O2���ǹ��ʰ�ί����ȷ�涨��Υ��ҩ������Ƴɱ�����ŵ����ŵ���ı�������������֪������ṹ��ʽΪC6H5CH2CH2COOH������ŵ���ķ���ʽΪ
A��C27H34O3������ B��C27H36O3������ C��C26H34O3������D��C27H36O4
15��ά����E�ڹ�������֮�������漣�衱����һ��֬����ά���أ��Կ�˥�ϵ����������ã����о�����ά����E�Ц����¡��á����������ͣ���ṹ��ʽ���£�
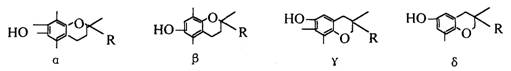
����RΪ-CH2CH2CH2[CH(CH3)CH2CH2]2CH(CH3)2����![]()
������Ϊͬ���칹�����
A���� �¡������� B���� �á������� C���� �ġ������� D���� ��
16�����ƣ�C6H5ONa����Һ��ͨ��������CO2���壬������Ӧ�Ļ�ѧ����ʽΪ
C6H5ONa��CO2��H2O��C6H5OH����NaHCO3�� ����˵������ȷ����
A�������H������������H2CO3��HCO3����C6H5OH
B�����H������������CO32����C6H5O����HCO3��
C����Ӧ2C6H5ONa��CO2��H2O��2C6H5OH����Na2CO3�ܹ�����
D����ӦC6H5OH��Na2CO3��C6H5ONa��NaHCO3
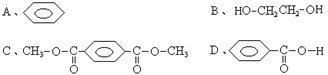
17���ܹ�����������Ʒ�������������Ⱦ�������ʳ�����Ϊ����ɫ��Ⱦ���Ϊ�˷�ֹ������Ⱦ����һ����Ҫ��;���ǽ��併��ΪС���ӡ�Ŀǰ�����½ṹ�����ϵĽ����Ѿ�ȡ�óɹ���
��������������![]()
�Է�������CH3OH�����������ܵõ����л��������
�� 
18�����Ҵ�Ϊԭ�ϣ�������6�����͵ķ�Ӧ�������� ����ȥ �ۼӳ� ������ ��ˮ��Ӿۣ����ϳ��Ҷ����Ҷ�����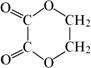 ������ȷ˳����
������ȷ˳����
A���٢ݢڢۢܡ���B���٢ڢۢݢܡ���C���ڢۢݢ٢ܡ��� D���ڢۢݢ٢�
19���������л�����ɵĻ�����һ���¶Ⱥ�ѹǿ����ȫ����Ϊ���塣����ͬ���¶Ⱥ�ѹǿ�£�ֻҪ�����������һ������ô���ۻ�����Ժ��ֱ�����ϣ�������ȫȼ��ʱ�����ĵ��������Ҳ��һ���ģ��������������������
A���Ҵ���C2H6O���ͱ�ϩ�ᣨC3H4O2����B������C6H6���ͱ����ᣨC7H6O2��
C����ȩ��C3H6O�����ͣ�C3H8O3������ D����ͪ��C3H6O���ͱ�������C3H8O2��
20������ʵ�����йظ����ʵ��жϲ���ȷ���ǣ�
A����������Ӧ������������������ˮ����
B����CH2O������Cu(OH)2����Һ�ķ�Ӧ�У�CH2O����ԭ����Cu(OH)2����ԭΪCu2O
C����ȩ���������ⷴӦʱ������������������
D���Ҵ�����Ҫ��ԭ�ϣ���ҵ�ϴ���������ȡ��ϩ����ȩ
21�����Ӻ˴Ź����ף�PMR�����о��л�����ӽṹ����Ч����֮һ��ÿһ�ṹ�еĵ�����ԭ����PMR����������Ӧ�ķ壨�źţ������ǿ����ṹ�е�Hԭ���������ȡ���ô������������PMR���е��źź�ǿ�ȷֱ�Ӧ����
A�������źţ�ǿ��֮��Ϊ1��1���� B�������źţ�ǿ��֮��Ϊ3��2��1
C�������źţ�ǿ��֮��Ϊ3��1���� D�������źţ�ǿ��֮��Ϊ1��1��1
�ڢ������ѡ���⣩
�༶������������ ���������������� ��ѧ����������
��������⡡
23���ڡ��ǵ䡱��Ű�ڼ䣬�ҹ����������˹����ᣨ���������������ֳƹ������ᣩ��Ϊ�����������������ʽΪC2H4O3��һ����Ʒ�������ǻ��д����ˮ��Һ����������40%�����������Ժ�ǿ�ĸ�Ч����������Ѹ��ɱ����ϸ��������ȣ���ʹ��-30��ĵ�����Ҳ����Ч��ɱ��Ч���ȸ������֡�ʯ̿�ᶼ�ã�����գ�
��д��������Ľṹ��ʽ���������������������� ��
����Ʒ�������Ƿ��д̼�����ζ�������������� ����С���û�С�����
���ܷ���Ʒ������ֱ�Ӳ�Ϳ��Ƥ��������������������������� �������������ʲ��ȶ����ܷ����ܷⱣ������Ͱ�У����������������� ����ܡ����ܡ�����
�ȹ�������ɴ�������������������������ʱ���ö��ã�д������ʽ��
������������������������������������������������������������������������������ ��
����ʱҲ������ȩ�Ĵ�����Һ�ó����������ã�д������ʽ��
������������������������������������������������������������������������������ ��
24������ʯ�ij��������֣�һ��Ϊ�����ͣ�һ��Ϊ���̴��ͣ�������������ü��嶡�����Ƴ������ע�䲡�λ����ʱ�ٽ������Һ���ȡ���������Ʒ������Իش�
�����ü��嶡���ѵ����ƹ����У����嶡���ѿ�ʹ���̴��ͽ�ʯ������ĸ������
A���ܽ⡡ B�����ԡ� C��������D���ֽ�Ϊ����
�����м��ұ��������Ʊ����嶡���ѵķ�����
���ף�CH3ONa +(CH3)3CCl��CH3OC(CH3)3+NaCl���� ��NaOH�Ĵ���Һ�У�
�ң�CH3Cl+NaOC(CH3)3��CH3OC(CH3)3+NaCl
����CH3I+NaOC(CH3)3��CH3OC(CH3)3+NaI������NaOH�����¼��ȣ�����
������CH3OH+HOC(CH3)3��CH3OC(CH3)3+H3O��
��֪��ȥHX�����׳̶�ΪX-C(CH3)3 �� X-CH(CH3)2 �� X-CH2CH3 �������ѣ�,���ڳ���������ԭ����ֻ��CH3ClΪ��̬,�����Լ���ΪҺ̬��
һ����Ϊ���������ַ����б�Ϊ��ѣ���ΪҺ�巴Ӧ���Ӵ���������ڷ�Ӧ�������������ɡ���������������IJ���֮����
�ף������������������������������������������������������������������� ������
�ң����������������������������������������������������������������������� ��
�������������������������������������������������������������������������� ����������������������������������������
25��2003��1�£�ԭ�⾭ó�������Բ����ձ�������ʱ���¹��ȹ��ҵı�����ȫ���ڱ�������������ȡ��ʱ��������ʩ��
�� ����(C8H4O3)��һ�ְ�ɫ���壬��������ˮ��ˮ��Ϊ�ڱ������ᣬ����(C10H8)���ڶ��ױ������ڷ���ʱ���ȿ����������á���Ҫ������Ⱦ�ϡ�ҩ��������ܼ��͵��ڵȡ�ij�л���J��C19H20O4��������ˮ�����Եͣ��������ϩ������ϩ����֬�������������ԣ������Ϲ�ҵ��Ҫ���ܼ��������ñ����������з����ϳ�֮��
��֪��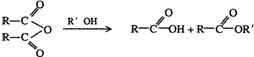
�ϳ�·�ߣ�
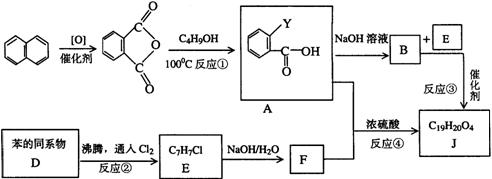
���������У���������Ӧ A��B�������кͷ�Ӧ��������F��Ũ��ˮ��ϲ�������ɫ������
��ָ����Ӧ���ͣ���Ӧ�������������� ��Ӧ�������������� ��
��д���ṹ��ʽ��Y������������������ F������������������ ��
��д��B��E��J�Ļ�ѧ����ʽ�������������������������������������� ��
��д��D��E�Ļ�ѧ����ʽ�������������������������������������� ��
��F��ͬ���칹���ж��֣�������FeCl3��Һ������ɫ�Ľṹ��ʽ�ǣ����������������� ��
26����ѧʽΪC8H10![]() O�Ļ�����A�����������ʣ�
O�Ļ�����A�����������ʣ�
�١��� A+Na���������ݡ������� �� A+RCOOH���й���ζ�IJ��
��A�ܱ�KMnO4������Һ����Ϊ�����ᡡ�� ��A�Ĵ�������ﲻ�ܷ���������Ӧ
��A��ˮ��Ӧ�IJ��ᆳ�ۺϿ��Ƴ�һ��������Ʒ
�Իش� ��A�Ľṹ��ʽ�������������������������������� ��
��A��Na��Ӧ�ķ���ʽ������������������������������������������������������ ��
��A����ᷴӦ�ķ���ʽ���������������������� �������������������������������� ��
��A��ˮ��Ӧ�IJ�����ۺϷ�Ӧ�ķ���ʽ�������������������������������������� ��
27����ѧʽC7H7NO2���л���A��B��C��D��E��F�����о����б�����
(1)A��B��C3���л���������ǿ�ᣬ��������ǿ���A��B��C�Ľṹ��ʽΪ��
A____________��B____________��C____________��
(2)D��E��F�Ȳ�����ǿ�ᣬ�ֲ�����ǿ���D��E��F�Ľṹ��ʽΪ��
D________��E____________��F____________��
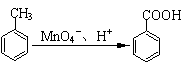 28��������ڸ�����ص������£��������������Ȼ�������
28��������ڸ�����ص������£��������������Ȼ�������
������A��E��ת����ϵ��ͼ1��ʾ����֪��A�Ƿ��㻯���ֻ������3��һ�廯���B�����ԣ�C�dz������ܼ���D���л��ϳɵ���Ҫ�м���ͳ��û�ѧ�Լ���DҲ��������ԭ�ϴ������õ�����E��һ�ֳ��õ�ָʾ����̪���ṹ��ͼ2��
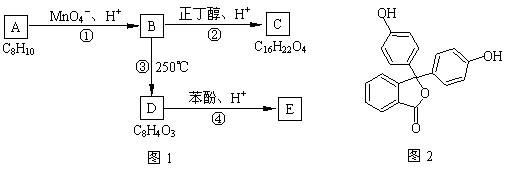 |
д��A��B��C��D�Ľṹ��ʽ��
A_____________________________��B______________________________��
C_____________________________��D______________________________��
29������ˮ�м���������ȩ��Һ�����Կ�����ˮ��ɫ���Բ����������ԭ�����������ֲ��룺����ˮ����ȩ����ȡ����Ӧ����������ȩ�������в����ͼ�����ˮ����ȩ�����ӳɷ�Ӧ����������ȩ���л�ԭ�ԣ���ˮ����ȩ����Ϊ���ᡣΪ̽����һ�ֲ�����ȷ��һ�о���ѧϰС���������������ʵ�鷽����
����һ��������ɫ����Һ������ԡ�
���������ⶨ��Ӧǰ��ˮ��Br2�����ʵ����ͷ�Ӧ��Br�����ӵ����ʵ�����
�ŷ���һ�Ƿ���У�_____________��������_____________________________________��
�Ƽ����÷�Ӧǰ��ˮ��Br2�����ʵ���Ϊa mol������÷�Ӧ��n(Br��)��______mol��˵����ˮ����ȩ����ȡ����Ӧ������÷�Ӧ��n(Br��)��______mol��˵����ˮ����ȩ�����ӳɷ�Ӧ������÷�Ӧ��n(Br��)��______mol��˵����ˮ����ȩ����Ϊ���ᡣ
30��������ͬѧ���п���ʵ�飬��ȡ250 mL��ɫ������ƿһֻ�����μ���4 g�������ơ�4 g�����ǡ���ƿˮ��3��0.2%���Ǽ�����Һ��һ��������ԭָʾ��������ƿ������Һ����ɫ�����ú���Һ��Ϊ��ɫ�����ٴ����ֳ���ɫ�����ú��ֱ�Ϊ��ɫ����η�����������������������ɫ��ʧ����ƿ�ڼ���ˮ����ƿ������ȴ���ٳ�����ɫ������Ϊ������Ũ�Ȳ�ͬ����ġ�����Ʋ������һ��ʵ�飬�����ҵ�˵��������Ϊ��ʵ��IJ����������ǣ�___________________________________________________________������ֵ���ɫ��Ҫ��__________�йأ���д��ѧʽ����ͬ������ɫ��ʧ����____________�йء�
31������ʽΪC3H6O3�������ж���ͬ���칹�壬��д����������Ҫ��ĸ���ͬ���칹��Ľṹ��ʽ��˵�����ٲ�����ͬһ̼ԭ�����������ǻ�������Ȳ�����ȷ�����ͬ��ԭ�ӻ�ѧ������ͬ�����顢����ȷ�����ͬ��ԭ�ӻ�ѧ���������֡�
�ż�����û�м�����1 mol ������������Na��Ӧ����1 mol H2����������NaHCO3��Һ��Ӧ����Ľṹ��ʽΪ���������������ܷ���������Ӧ����Ľṹ��ʽΪ�������� ��
���ҷ���������ͬ��ԭ�ӵĻ�ѧ������ͬ���Ҳ������Na��Ӧ�����ҽṹ��ʽΪ�������� ��
�DZ�������̼�����ֱ������ֻ�ѧ��������Ļ�ѧ������ͬ���ұ������Na����Ӧ������ṹ��ʽΪ���������������������� ��
32�����������۾����ɾۼ���ϩ��������(HEMA)�Ƴɳ�����Ƭ����ϳ�·�߿����ǣ�
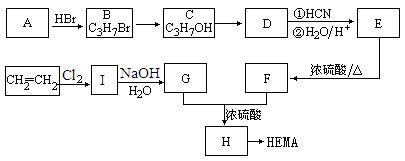
��֪��![]()
�� ��CH3COOCH2CH2OH����������������
�����
��A��E�Ľṹ��ʽ�ֱ�Ϊ��A������������������ ��E������������������ ��
��д�����з�Ӧ�ķ�Ӧ���ͣ�C��D�� �������� ��E��F���������� ��
��д������ת���Ļ�ѧ����ʽ��I��G������������������������������������������ ��
G+F��H������������������������������������������������������������ ��
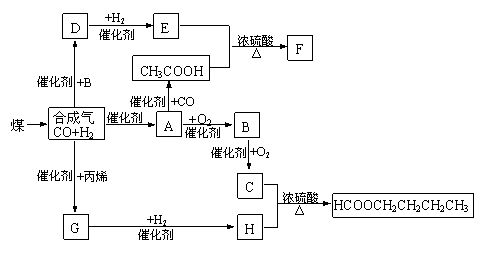 33��ú��������Һ����ʹú��������Դ����Ч;����ú��������Ҫ��Ӧ�ǣ�C+H2O(g)
33��ú��������Һ����ʹú��������Դ����Ч;����ú��������Ҫ��Ӧ�ǣ�C+H2O(g)![]() CO+H2��CO��H2�Ļ�������Ǻϳɶ����л����ԭ��������ͼ�Ǻϳ�ijЩ���ʵ�·�ߡ�
CO+H2��CO��H2�Ļ�������Ǻϳɶ����л����ԭ��������ͼ�Ǻϳ�ijЩ���ʵ�·�ߡ�
���У�D������ˮ������CH3COOH��Ϊͬ���칹�壻F�����е�̼ԭ������D��3����H���������ɵõ�G����ش��������⣺
��д���������ʵĽṹ��ʽ��
A______������ __��H__________����������ָ��A��H�Ĺ�ϵ������������ ��
��д�����з�Ӧ�Ļ�ѧ����ʽ��
CH3COOH+E��F___________________���������� _____________________��
D������Cu(OH)2����_______________________________________________��
����������
34��ij�л���X��C��H��O����Ԫ����ɣ�X�ķе�Ϊ471K����֪��
��һ�����¶Ⱥ�ѹǿ��(�ڴ��¶Ⱥ�ѹǿ��1mol�κ�����������Ϊ42L)����4.2L X��������18.9 L ����(����)��Ϻ��ȼ����ַ�Ӧ���¶�ѹǿ�ָ���ԭ��״̬���õ��������A 29.4 L���ٸı��¶Ⱥ�ѹǿʹA���ڱ�״������ʱ���������Ϊ8.96L,�ܶ�Ϊ1.696g/L�����ƶϣ�A�и���ֵ����ʵ������� ��X�Ļ�ѧʽ��
����1molX�������Ʒ�Ӧ��1molH2��д��X�������Ҷ���(H2C2O4)��Ӧ���ɵĻ�״�ṹ�����ʵĽṹ��ʽ�����ơ�
35��������CO��HCOOH��OHC��COOH�ֱ�ȼ��ʱ������O2������CO2������ȶ���1��2�������ߵķ���ʽ���Կ�����(CO)(H2O)��(CO)2(H2O)����ֻҪ����ʽ���ϣ�(CO)m(H2O)n��(m��nΪ������)�ĸ����л������ȼ��ʱ����O2������CO2������ȶ���1��2��
����һЩֻ��C��H��O��Ԫ�ص��л������ȼ��ʱ����O2������CO2������ȶ���3��4��
��1����Щ��������ʽ����С�����ʵĻ�ѧʽ���������������������� ��
��2��ij����̼ԭ������ͬ�������л������ʽ���ֱ�Ϊa��b(a��b),�� b-a�ض������� ��������������
������������һ���֣���
��3��������һ��Ҳֻ��C��H��O��Ԫ�ص��л������ȼ��ʱ����O2������CO2������ȶ���5��4��������������ͨʽ�ɱ�ʾΪ���������������� �����������ʽ����С�����ʵĽṹ��ʽ���������������������������� ��