高二化学会考练习(选择、填空、推断)
一.选择题(每小题只有一个正确答案)
1.下列物质中,属于纯净物的是
A.碱石灰 B.生石灰 C.汽油 D.铝热剂
2.下列各组物质中,互为同位素的是
A.氕和氘 B.蓝矾和胆矾 C.金刚石和石墨 D.丁烷和异丁烷
3.实验室制取下列气体时,只能用排水法收集的是
A.CH4 B.CO2 C.NO D.NO2
4.在自然界里,既有以游离态又有以化合态的形式存在的元素是
A.Cl B.P C.S D. Na
5. 常温下,将铁片放入下列溶液中,能明显观察到有气体产生的是
A.浓硫酸 B.稀硫酸 C. ZnSO4溶液 D.CuSO4溶液
6. 下列物质露置在空气中,不会发生化学变化的是
A.白磷 B.氢硫酸 C. 烧碱溶液 D. 硝酸钠溶液
7.欲除去铁粉中混有的少量铝粉,应选用的试剂的是D
A.稀盐酸 B.稀硝酸 C.氨水 D.氢氧化钠溶液
8.若将乙醛通过下列两步反应转变成溴乙烷:
![]()
这两步反应分别属于有机反应类型中的
A.加聚反应和水解反应 B.消去反应和加成反应
C.加成反应的取代反应 D.加成反应的消去反应
9.下列物质在固态时,晶体类型相同的是
A.SiO2和CO2 B.NaCl和HCl C.I2和金刚石 D.NH3和H2O
10.将下列气体通入水中,既能生成含氧酸,又能生成无氧酸的的A
A.氯气 B.二气体氧化氮 C.硫化氢 D.二氧化碳
11.下列关于碱金属的叙述中,不正确的是
A.钾元素比钠元素的金属性强 B.钾和钠的焰色分别为紫色和黄色
C.碱金属都能和水起反应,生成氢氧化物并放出氢气
D.碱金属的熔点随着电子层数的增加而升高
12.下列变化中,通过下一步反应就可以直接完成的是
A.Al2O3→ Al(OH)3 B.CaCO3→ Ca(OH)2 C.P2O5 →H3PO4 D.CO→ NaHCO3
13.下列说法正确的是
A.摩尔是物质的质量单位 B.氢气的摩尔质量是2g
C.1molOH-的质量是17g D.气体摩尔质量就是1mol气体所占的体积
14.下列关于硅和硅的化合物性质的叙述,正确的是
A.二氧化硅溶于水可制得硅酸 B.硅酸的酸性比碳酸弱B
C.二氧化硅是酸性氧化物,不跟任何酸起反应
D.硅在常温下能跟氢气起反应生成SiH4
15.在强酸性溶液中能大量共存的离子是
A.S2- B.AlO2- C.HCO3- D.NH4+
16.下列各组中两种微粒的半径(用r表示)之比小于1的是
A.r(Na)/ r(Na+) B.r(S)/ r(S2-) C.r(Mg)/r(Al) D.r(Cl)/r(F)
17. 在接触法制硫酸、氨的催化氧化法制硝酸和炼铁的工业生产中,都需要用到的一种原料是
A.氢气 B.空气 C.石灰石 D.硫铁矿
18.下列分离或提纯物质所用的方法不正确的是
A.用加热的方法除去Na2CO3中混有的NaHCO3
B.用分液的方法分离乙醛和水的混合物
C.用萃取的方法提取碘水中的碘
D.用结晶的方法分离氯化钠和硝酸钾的混合物
19.丙烯醛的结构简式为:![]() 下列试剂中,不能跟丙烯醛反应的
下列试剂中,不能跟丙烯醛反应的
A.溴水 B.新制的Cu(OH)2 C.Na2CO3溶液 D.KMnO4酸性溶液
20.X、Y、Z三种短周期元素在周期表中的位置如下图所示。
若这三种元素的原子序数之和为32,则Y元素是
A.碳 B.氧 C.硫 D.氯
21.苯分子中的两个氢原被氯原子取代后,生成的同分异构体有
A.1种 B.2种 C.3种 D.4种
22.下列反应的离子方程式正确的是
A.碳酸钙跟盐酸反应: CO32-+2H+==CO2↑+H2O
B.氨水跟盐酸反应: OH- + H+ == H2O
C.氢氧化钡跟稀硫酸反应: Ba2+ + OH- + H+ + SO42- == BaSO4↓+ H2O
D.铁跟氯化铁溶液反应: Fe +2 Fe3+ ==3Fe2+
23.X、Y都是短周期元素,若X的原子序数为n,X2+与Y2-具有相同的电子层结
构,则Y的原子序数是
A.n-2 B.n-4 C.n-6 D.n-8
24.在同温同压下,某气体与氧气体积相同,质量之比为2∶1,则该气体的式量为:A
A、64 B、44 C、28 D、16
25.在盛有足量Na2O2的密闭闭容器中充入3molCO2和1molCO,不断用电火花引燃,充分反应后,容器内剩余气体的物质的量为D
A.0 B.0.5mol C.1mol D.1.5mol
| 题 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| 答 | B | A | C | C | B | D | D | C | D | A | D | D | C |
| 题 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | |
| 答 | B | D | B | B | B | C | C | C | D | B | A | D |
可能用到的原子量: H-1 C-12 N-14 O-16 Na-23 Mg-24 Al-27 Cl-35.5
二、填空题
26.在硅晶体、二氧化硅、硫酸钙、硫酸钡四种物质中,可用作制造光导纤维
的重要原料的是二氧化硅,常用作“钡餐”的是硫酸钙。
27.某元素原子的最外层电子数是次外层电子数的两倍,该元素的名称是碳,其原子结构示意图为![]() 。
。
28.在钠的化合物中,俗名叫小苏打的是NaHCO3;具有强氧化性的是Na2O2 。
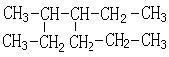 29.某有机物的结构简式为:
29.某有机物的结构简式为:
它的主链上有7个碳原子,按系统命名法
的名称是三甲基-四乙基庚烷。
30.漂白粉的有效成分是(填化学式)Ca(ClO)2;石膏的化学式是CaSO4.2H2O。
31.向溴化钠溶液中通入过量氯气,反应后将溶液蒸干并灼烧,最后得到的固体物质是氯化钠,溴化钠跟氯气反应的离子方程式是 2Br-+Cl2 ==2Cl-+Br2。
![]()
![]() 32.制备有机物[CH2-CHCl]n 的单体是CH2=CHCl(写结构简式)。
32.制备有机物[CH2-CHCl]n 的单体是CH2=CHCl(写结构简式)。
33.配平下列氧化还原反应方程式:
3 K2S + 8 HNO3 == 6 KNO3 + 2 NO↑+ 3 S + 4 H2O
当反应中有3mol电子发生转移时,有 4 mol HNO3参加反应。
34.NO是污染大气的有毒气体,为了消除NO的污染,可将它跟氨气在催化剂的作用下反应,生成水和一种完全无污染的气态单质,该单质是空气的主要成分之一,这种单质是N2. 该反应的化学方程式是6NO +4 NH3==5N2 +6H2O
35.将a g MgCO3与b g NaHCO3分别加入到100mL1mol/L的盐酸溶液中,若反
应后所得两种溶液的质量相等,则a和b的关系及取值范围是: 0![]() a=b
a=b![]() 4.2。
4.2。
三、 推断题
36.已知一定条件下,单质X、Y、Z与化合物甲、乙之间存在如下变化关系:

(1) 若X是O2,Y是S,Z是H2,化合物甲是一种可燃性气体,则化合物甲是
H2S ,化合物乙是 H2O 。
(2) (2)若X是Mg,Y是C,Z是O2,化合物甲是一种不可燃气体,则化合物甲是CO2 ,化合物乙是 MgO 。
37.A.B.C.D四种有机物,在一定条件下有如下转化关系:
![]()
已知D的分子式为C4H8O2,试推断A、B、C、D各是什么物质。(用结构简式表示)
A CH3CH2OH B CH3CHO C CH3COOH D CH3COOCH2CH3