高二化学第二学期三月考试试卷
考试时间:120分钟,分值:150分
命题及校对:邓伟
本卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷1~4页,第Ⅱ卷5~8页。
注意事项:
1.答Ⅰ卷前,考生务必将自己的姓名、考试号、考试科目用2B铅笔涂写在答题卡上。
2.每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案,不能答在试题卷上。
3.考试结束后,将答案卡和第Ⅱ卷一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24
Al-27 P-31 S-32 Cl-35.5 Fe-56 Cu-64 He-4
第I卷(选择题 共80分)
一.选择题(本题包括10小题,每小题4分,共40分。每小题只有一个选项符合题意。)
1、H2C=CHOH不稳定,在常温下为液体,很容易转化成稳定的CH3CHO,然而,2002年的美国《科学》杂志报道:外太空的某一个星球的大气层含有大量的H2C=CHOH。请预测该星球的温度是:
A. 较低温度 B. 较高温度
C. 无法判断温度的高低 D. 上述说法都不正确
2.大气污染物氟里昂-12的分子式是CF2Cl2,它是一种卤代烃,关于它的说法正确的是
A.它有两种同分异构体 B.它是极性分子
C.它的空间构型为正四面体 D.它不属于有机物
![]() 3.某有机物链状分子中含n个-CH2-,m个 -CH-,a个-CH3,其余为—Cl。则—Cl的个数为
3.某有机物链状分子中含n个-CH2-,m个 -CH-,a个-CH3,其余为—Cl。则—Cl的个数为
A.2n+3m-a B.m+2-a C.n+m+a D.m+2n+2-a
4.有下列物质,其分子为正四面体型的是
①金刚石;②白磷(P4);③甲烷;④氯仿;⑤四氯化碳;⑥二氧化硅
A.②③⑤ B.①②③④⑤ C.①③⑤⑥ D.全部
5.下列芳香烃的一氯取代物的同分异构体的数目最多的是
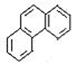
![]() A、连二苯:
B、菲
A、连二苯:
B、菲
![]()
![]() C、蒽
D、连三苯
C、蒽
D、连三苯
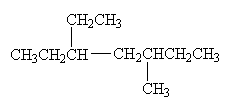 6.分子中含有一个叁键的炔烃完全加氢后的产物结构如下
6.分子中含有一个叁键的炔烃完全加氢后的产物结构如下
则该炔烃可能的结构有
A.1种 B.2种 C.3种 D.4种
![]() 7.某种有机物化学式为C5H11Cl,分子中有 2个—CH3,2个—CH2—,1个
,1个—Cl,则该有机物可能的结构有
7.某种有机物化学式为C5H11Cl,分子中有 2个—CH3,2个—CH2—,1个
,1个—Cl,则该有机物可能的结构有
A.1种 B.2种 C.3种 D.4种
8.常温常压下,某气态烃和氧气的混合气体nL,完全燃烧后,通过浓硫酸恢复到原来的温度和压强,气体体积为原来的一半,假设烃在燃烧后无剩余,则该烃的组成可能是下列组合中的
①甲烷 ②乙烯 ③乙炔 ④乙烷
⑤丙烯 ⑥丙炔 ⑦丙烷 ⑧丁炔
A.①②③④ B.⑤⑥⑦⑧ C.①③⑤⑦ D.①②④⑦
9、A、B两种烃组成的混合物,当混合物质量一定时,无论A、B以何种比例混合,完全燃烧 消耗氧气的量为一恒量:那么A、B两种烃①互为同分异构体;②互为同系物;③具有相同的最简式;④含碳的质量分数相同,正确的结论是
![]() A.①②③④ B.①③④ C.②③④ D.③④
A.①②③④ B.①③④ C.②③④ D.③④
10. 某有机高分子由两种结构单元 和 _ _ 组成,
且它们自身不能相连,该有机高分子中C、H两原子物质的量之比是
A、2:1 B、3:2 C、8:5 D、19:22
二.选择题(每题有一个或两个选项符合题意。每小题4分,共40分。)
11.下列变化中,由加成反应引起的是
A.乙炔通入酸性高锰酸钾溶液中,高锰酸钾溶液褪色
B.乙烯在一定温度、压强和催化剂的作用下,聚合为聚乙烯
C.在一定条件下,苯滴入浓硝酸和浓硫酸的混合液中,有油状生成
D.在催化剂作用下,乙烯与水反应生成乙醇
12、设阿佛加德罗常数为NA,则下列说法正确的是
A.15g甲基(-CH3)所含有的电子数是10NA
B.常温常压下,4g氦气所含有的原子数目为NA
C.标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为
(5/22.4)NA
D.常温常压下,1mol丙烷所含有的共价健数为12NA
13、下列说法正确的是
A、苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅
B、酸性高锰酸钾溶液和溴水都能鉴别直馏汽油和裂化汽油
C、煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来
D、石油中含有C5~C11的烷烃,可以通过分馏得到汽油
14、下列有关同分异构体数目的叙述中,不正确的是
A、甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
B.质量相同的甲、乙两有机物完全燃烧,产生质量相同的水,则甲、乙两分子所含氢原子的个数一定相等。
C、含有5个碳原子的饱和链烃,其一氯取代物有8种
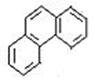
D、菲的结构简式为 ,它与硝酸反应,可生成5种一硝基取代物
15、下列实验操作中正确的是
A、将液溴、铁粉和苯混合加热即可制得溴苯
B、除去溴苯中红棕色的溴,可用稀NaOH溶液反复洗涤,并用分液漏斗分液
C、用苯与浓硝酸、浓硫酸反应制取硝基苯时需水浴加热,温度计应放在混合液中
D、制取硝基苯时,应取浓硫酸2mL,再加入1.5mL浓硝酸,再滴入苯约1mL,然后放在水浴中加热
16、将1molCH4和适量的氧气在密闭容器中点燃,充分反应后,甲烷和氧气均无剩余,且产物均为气体(101kPa,120℃),其总质量为72g,下列有关叙述不正确的是
A.若将产物通过碱石灰,则可全被吸收,若通过浓硫酸,则不能被完全吸收
B.产物的平均摩尔质量为24
C.若将产物通过浓硫酸充分吸收后恢复至(120℃),则压强变为原来的1/3
D.反应中消耗的氧气为56g
17、实验室制少量氯乙烷的方法可行的是
A. 乙烯气体通入稀盐酸中 B. 乙烷和氯气在光照条件下反应
C. 将乙烯通入氯水中 D. 乙醇和浓盐酸回流加热
18.已知烯烃在酸性KMnO4溶液中双键断裂形式为
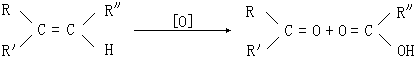
现有二烯烃C10H18与KMnO4溶液作用后可得到三种有机物:(CH3)2CO、 CH3COOH、 CH3CO(CH2)2COOH,由此推断二烯烃可能的结构简式为
A.(CH3)2C=CHCH2CH2CH2CH=CHCH3
B.(CH3)2C=CHCH2CH2C(CH3)=CHCH3
C.CH3CH=C(CH3)CH2CH2CH2C(CH3)=CH2
D.CH2CH=C(CH3)CH2CH2CH2CH=CHCH3
19.在烃分子中去掉2个氢原子形成双键是吸热反应,大约需117~125kJ/mol的热量,但1,3-环己二烯失去2个氢原子变成苯是放热反应,反应热为23.4kJ/mol,以上事实表明
A、1,3-环己二烯加氢是吸热反应 B、苯加氢生成环己烷是放热反应
C、1,3-环己二烯比苯稳定 D、苯比1,3-环己二烯稳定
20.有机物的结构简式可以用“键线式”表示,如维生素A的结构简式可写为:
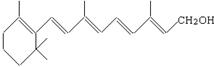 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来。已知利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光光照转化成四环烷(Q)的反应为:
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来。已知利用某些有机物之间的转化可贮存太阳能,如原降冰片二烯(NBD)经太阳光光照转化成四环烷(Q)的反应为:
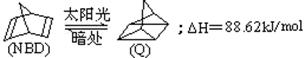
以下叙述中错误的是
A. NBD和Q互为同分异构体 B. NBD的二氯代物有8种
C. Q的一氯代物只有3种
D. NBD的二氯代物的数目小于Q的二氯代数目
 第II卷(非选择题
共70分)
第II卷(非选择题
共70分)
三、(本题包括2小题,共14分)
21、(1)(2分)某学生设计了下述实验室分馏石油的实验,分为五个步骤。
①将蒸馏烧瓶放在铁架台上,在蒸馏烧瓶上塞好带温度计的橡胶塞。
②连接好冷凝管,把冷凝管固定在铁架台上,将冷凝管的一端和水龙头连接,将出水口一端的橡胶管放入水槽中。
③把酒精灯放在铁架台上,根据酒精灯高度调整铁圈的高度,放好石棉网。
④向蒸馏烧瓶中放入碎瓷片,再用漏斗向烧瓶中加入原油,塞好带温度计的塞子,将牛角管接在冷凝管的末端,并深入锥形瓶中。
⑤检查气密性(利用给固定装置微热的方法)。
正确的操作顺序是 。(填序号)
(2)(6分)请选用适当的试剂和分离装置除去下列物质中所含的杂质(括号内为杂质),将作选的试剂及装置的编号填入表中。
试剂: a.水 b.溴的CCl4溶液 c.溴水
分离装置: A.分液 B.过滤 C.洗气
| 混合物 | 需加入的试剂 | 分离方法 |
| 1—氯丙烷(乙醇) | ||
| 乙烷(乙烯) | ||
| 溴化钠溶液(碘化钠) |
22.(6分) 某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是ag/cm3。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:①准确量取该卤代烷6mL,放入锥形瓶中。②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。③反应完成后,冷却溶液,加稀HNO3酸化,滴加过量AgNO3溶液,得白色沉淀。④过滤,洗涤,干燥后称重,得到cg固体。回答下面问题:
(1)装置中长玻璃管的作用是 。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的 离子。
(3)该卤代烷中所含卤素的名称是 ,判断的依据是 。
(4)该卤代烷的相对分子质量是 (列出算式)。
(5)如果在步骤③中加HNO3的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码) 。
A.偏大 B.偏小 C.不变 D.大小不定
四、(本题包括2小题,共18分)
23、(8分)原子簇化学是当前化学中最饶有兴趣而又极其活跃的领域之一。凡以3个或3个以上原子直接键合构成的多面体或笼为核心,连接外围原子或基团而形成的结构单元称原子簇.分子式为CnHn的多面体碳烷是典型的主族簇合物,下面是已经报道的碳烷多面体。
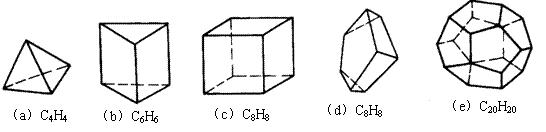 |
(1)(a)分子中碳-碳键的夹角为 。(b)的二氯代物有 种。
(2)上述分子中,若总键数为x,则x与碳原子数n的关系为 。
(3)若上述多面体的边数为m,则总键数x与m、n的关系为 。
24、(10分)(1)某有机物的结构简式如图所示,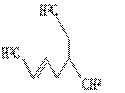 其名称是
其名称是
。
(2)将xmol O2 、ymol CH4和zmol Na2O2放入密闭容器中,在150℃时用电火花引发反应后,容器内压强为0。则x、y、z的关系为 。
(3)具有![]() 结构分子中,回答以下问题:在同一直线上的原子最多为_________个, 一定处同一平面的原子数最多为_________个,可能处同一平面的原子最多为__________个。
结构分子中,回答以下问题:在同一直线上的原子最多为_________个, 一定处同一平面的原子数最多为_________个,可能处同一平面的原子最多为__________个。
五、(本题包括2小题,共22分)
25、(12分)烃A1、A2 互为同分异构体,它们各加 1mol H2 都可得到烃 B。A1、A2 各加 1mol HCl都可得到 C1 。而B在光照下与氯气反应,只得到两种一氯代烃 C1和C2 。产物中 C2 比 C1多。
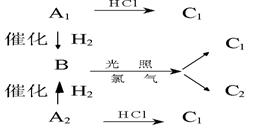 B的含碳质量分数为 83.7%, 求 A1、A2、B和 C1、C2
的结构简式,并回答,为什么B氯化的产物中 C2
比C1多?
B的含碳质量分数为 83.7%, 求 A1、A2、B和 C1、C2
的结构简式,并回答,为什么B氯化的产物中 C2
比C1多?
⑴
A1————————————— ————— A2—————— ——————————
B———————————————————— C1—————————— ———————————C2———————————————
⑵为什么B氯化的产物中 C2 比C1多?
26、(10分)已知:(1)乙炔是基本有机化工原料,用于合成许多有机产品,乙炔可与极性试剂加成:HCºCH+H—Z(Z为电负性大的元素)→CH2=CH—Z,也可以发生自身加成,下面是乙炔的反应:
![]()
![]() B
B![]() C
C
![]() D
D![]() E
E
乙炔+
![]() F
F![]() G
G![]() 氯丁橡胶
氯丁橡胶
![]() H(H中所有碳碳键键长相等)
H(H中所有碳碳键键长相等)
![]() I
I![]() J
J
![]() K(一种增塑剂)
K(一种增塑剂)
(2)具有烯醇结构的化合物通常不稳定,易发生分子内重排
![]() H
H
![]()
![]()
![]() C=C—H C C=O
C=C—H C C=O
H
①写出结构式C、 D、
H、 J 。
|
六、(本题包括2小题,共16分)
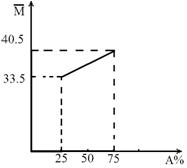
27、(6分)由A、B两种物质组成的混合气体,其平均相对分子质量随A的物质的量分数变化关系如右图所示。
(1)A的相对分子质量为__________。
(2)若测得混合气体中仅含两种元素,A、B都是无机物时,化学式分别为_________、________,A、B都是有机物时,化学式分别为_________、________。
28.(10分)在400℃、101.3kPa时,3L某烃A蒸气在mL氧气中完全燃烧,燃烧后测得气体体积为(m+6)L(气体体积均在同温同压下测定)试回答下列问题:
(1)通过计算说明,烃A的组成中应该满足的条件。
(2)通过计算推断,当m=27时烃A可能的分子式(写出常见的三种即可)。
(3)通过计算确定,若烃A在常温常压下为气体时,m的取值范围。
参考答案:
1 B 2 B 3 B 4 A 5 B 6 B 7 D 8 D 9 B 10 B 11 BD 12 B 13 D 14 B 15 B 16 AB 17 D 18 B 19 BD 20 BD
21、(1)②③①⑤④(2分)
(2)(每格1分共6分)
| 混合物 | 需加入的试剂 | 分离方法 |
| 1—氯丙烷(乙醇) | a | A |
| 乙烷(乙烯) | c | C |
| 溴化钠溶液(碘化钠) | b | A |
22.(每格1分共6分)解答:(1)防止卤代烷挥发(或冷凝)。
(2) ![]() 和
和 ![]() 。
。
(3)氯;得到的卤化银沉淀是白色的。(4) ![]() 。(5)A。
。(5)A。
23、(1)600 (2分) 3(2分)(2)x=2.5n(2分)(3)x=m+n或x=4n- m(2分)
24、(1).5-甲基-2-庚烯(2分)
(2) z≥3y=6x (2分)
(3) 6;(2分)14;(2分)29(2分)
25、(每格2分共12分)
![]()
![]()
![]()
|
|
|
|
|
|
|
|
|
![]()
![]()
![]()
|
|
|
|
|
|
|
|
26.(1)(每格1分共4分)![]() (1)①B、CH2=CHCl D、CH3CHO H、
(1)①B、CH2=CHCl D、CH3CHO H、
(2)(每格2分共6分)
27.(6分)
⑴44 (2分)
⑵N2O NO C3H8 C2H6 (每组2分,共4分)
28、(10分)(1)设烃的分子式为CxHy
![]() CxHy+(x+y/4)O2 xCO2+
CxHy+(x+y/4)O2 xCO2+![]() H2O 差量
H2O 差量
1
X+![]()
![]() —1
—1
3 (m+6)—(m—3)
列比例:1︰X+![]() =3︰[(m+6)—(m-3)] y=8 (3分)
=3︰[(m+6)—(m-3)] y=8 (3分)
(2)当m=27时,氧气恰好完全反应,也可能过量。
所以有关系: ![]() ≥
≥![]() 解之得:x≤7
解之得:x≤7
A的可能分子式:C3H8、C4H8、C5H8、C6H8、C7H8(写出其中的三个分子式就可以)
(每个1分,共3分)
(3)当A常温常压下为气体时,则x![]() ≤4 (4分)
≤4 (4分)
![]() ≥
≥![]()