期中复习练习
一、选择题(每题只有一个答案符合题意)
1.下列各组物质中,全部属于纯净物的是 ( )
A.福尔马林、白酒、醋 B.丙三醇、氯仿、乙醇钠
C.苯、汽油、无水酒精 D.甘油、冰醋酸、煤
2.下列物质中属于醇类且发生消去反应的是 ( )
A. ![]() B.
B. ![]()
C.![]() D.
D.
![]()
3.下列试剂中,能用于检验酒精中是否含水的是 ( )
A.新制生石灰 B.无水硫酸铜 C.浓硫酸 D.金属钠
4. 质量相同的下列各种醇,与乙酸发生酯化反应时,消耗乙酸最多的是 ( )
A.丙三醇 B.乙二醇 C.乙醇 D.甲醇
5. 下列配制银氨溶液的操作中,正确的是 ( )
A.在洁净的试管中加入1~2mLAgNO3溶液,再加入过量浓氨水振荡混合
B.在洁净的试管中加入1~2mL浓氨水,再加入AgNO3溶液至过量
C.在洁净的试管中加入1~2mL稀氨水,再逐滴加入2% AgNO3溶液至过量
D.在洁净的试管中加入2% AgNO3溶液1~2mL,逐滴加入2%稀氨水至沉淀恰好溶
解为至
6.下列各组物质中,互为同系物的是 ( )
A.![]() 与
与![]() B.
B.![]() 与
与![]()
C.硬脂酸与油酸 D.甲醇与乙二醇
7.不洁净玻璃仪器洗涤方法正确的是 ( )
A.做银镜反应后的试管用氨水洗涤
B.做碘升华实验后的烧杯用酒精洗涤
C.盛装苯酚后的试管用盐酸洗涤
D.实验室制取O2后的试管用稀HCl洗涤
8.下列物质中,在不同条件下可以发生氧化、消去、酯化反应的为 ( )
A.乙醇 B.乙醛 C.苯酚 D.乙酸
9.32克某饱和一元醇与足量的金属钠反应,得到11.2L(标准状况下)H2,该醇是( )
A.CH3OH B.C2H5OH C.C3H7OH D.C4H9OH
10.鉴别苯酚、硫氰化钾、乙酸、氢氧化钠四种溶液,可用的一种试剂是 ( )
A.盐酸 B.食盐
C.新制的氢氧化铜 D.氯化铁
二、选择题(每题有1~2个选项符合题意)
11.用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是 ( )
A.18O只存在于乙酸乙酯中
B.18O存在于水、乙酸、乙醇以及乙酸乙酯中
C.18O存在于乙酸乙酯、乙醇中
D.若与丙酸反应生成的酯的相对分子质量为102
12.下列有关除杂质(括号中为杂质)的操作中,错误的是 ( )
A.福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物
B.乙醇(乙醛):加新制Cu(OH)2溶液,加热至沸腾,过滤取溶液
C.苯(苯酚):加溴水,振荡,过滤除去沉淀
D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层
13.某有机物的结构简式如下图。则此有机物可发生的反应类型有 ( )
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和 。
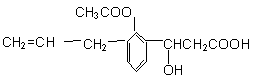 |
A.①②③⑤⑥ B.②③④⑤⑥ C.①②③④⑤⑥ D.①②③④⑤⑥⑦
14. 乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
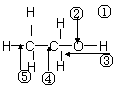 A.和金属钠作用时,键①断裂
A.和金属钠作用时,键①断裂
![]() B.和浓硫酸共热至170 ℃时,键②和④断裂
B.和浓硫酸共热至170 ℃时,键②和④断裂
C.和乙酸、浓硫酸共热时,键②断裂
D.在铜催化下和氧气反应时,键①和③断裂
15.甲醛、乙酸和丙醛组成的混合物中,氧元素的质量分数是37%,则碳元素的质量分数为 ( )
A.27% B.28% C.54% D.无法计算
三、(本题包括2小题)
16.(1)区分下列各组有机物(填“操作―现象―判断”)
①1―丙醇和丙三醇
②苯甲醇和苯酚
③乙醇和乙醚
④乙烯、苯、苯酚
(2)除去下物质中的少量杂质(括号内的物质),加入的试剂及操作方法分别为:
①乙醇(水)_______________;②溴乙烷(乙醇)_________________。
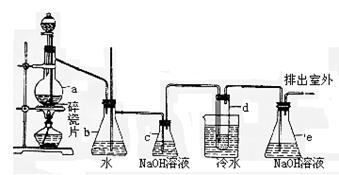
17.
|
(1)写出本题中制备1,2―二溴乙烷的两个化学反应方程式: ,
。
(2)安全瓶 b可以防止倒吸,并可以检查实验进行时试管d是否发生堵塞。请写出发生堵塞时瓶b中的现象: 。
(3)容器c中NaOH溶液的作用是 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,试分析其可能的原因。
四、(本题包括3小题)
18.某工业反应混合液中仅可能含有的组分是:乙醚(C4H10O)、乙醇和水,经分析,液体中C、H、O的原子数之比为16:42:5。
(1)若混合液中只含2种组分,则所有可能的组合是 。
(2)若混合液中含有3种组分,在628g混合液中有1mol H2O,此时乙醇和乙醚的物质的量各是多少?
19.饱和链烃A和不饱和链烃B在常温下均为气体,其中A含有的碳原子数多于B。
(1)将A和B按一定比例混合,1L混合气体完全燃烧后得到3.6LCO2气体,试推断混合气体A和B所有可能的组合及A、B的体积比,并将结果填入下表:
| 编号 | A的分子式 | B的分子式 | VA/VB |
| ① | |||
| ② | |||
| ③ | |||
| ④ |
(2)1mol该混合气体恰好能使含0.4mol溴的四氯化碳溶液完全褪色,推断上表中符合该条件的A、B的分子式,填入下表:
| A的分子式 | |||
| B的分子式 |
(3)120℃时,1LA、1LB与足量O2混合点燃后,在同温、同压下总体积增大2L,试通过计算确定A和B的分子式。
参考答案
1B。2C。3B。4A。5D。6B。7B。8A。9A。10D。11C。12BC。13D。14BC。15C。
16.①分别加入新制的Cu(OH)2悬浊液,充分振荡,出现绛蓝色的为丙三醇。
②加水溶解,分别滴入FeCl3溶液,出现紫色的为苯酚(或加入过量浓溴水,出现白色沉淀的为苯酚。)
③分别加入金属钠,发生反应放出气体的是乙醇。
④分别加入浓溴水,充分振荡能使溴水褪色的为乙烯;出现白色沉淀的为苯酚;溶液出现分层,上层为橙红色,下层为无色的为苯。
(2)①生石灰;蒸馏。 ②水;分液。
17.
(1)CH3CH2OH![]() CH2=CH2↑+H2O
CH2=CH2↑+H2O
CH2=CH2+Br2![]() CH2Br-CH2Br
CH2Br-CH2Br
(2)b中水面下降,玻璃管中水柱上升,甚至溢出。
(3)除去乙烯中带出的酸性气体(或除去CO2、SO2)
(4)①乙烯发生(或通过液溴)速度过快。
②实验过程中,乙醇和浓硫酸的混合液没有迅速达到170℃。
18.(1)乙醚和乙醇、乙醚和水。(2)乙醇2mol;乙醚7mol。
19.(1)
| 编 号 | A的分子式 | B的分子式 | VA/VB |
| ① | C4H10 | C2H2 | 4:1 |
| ② | C4H10 | C2H4 | 4:1 |
| ③ | C4H10 | C3H4 | 3:2 |
| ④ | C4H10 | C3H6 | 3:2 |
(2)
| A的分子式 | C4H10 | C4H10 |
| B的分子式 | C2H2 | C3H6 |
(3)由下列反应式分析1L烃燃烧后的体积增加△V。
![]() △V1=1.5(L)
△V1=1.5(L)
![]() △V2=-0.5(L)
△V2=-0.5(L)
![]() △V3=0(L)
△V3=0(L)
![]() △V4=0
△V4=0
![]() △V5=0.5(L)
△V5=0.5(L)
因△V1+△V5=2.0L,故混合烃中A是C4H10,B是C3H6。