2003��2004ѧ�����ѧ��
����ѧ��ѧ������ѵ��
��
�߶���ѧͬ�����ԣ�6������ѧƽ��
һ��ѡ���� (�������10С�⣬ÿС��2�֣�ÿС��ֻ��һ���𰸷�������)
1�����淴Ӧ�ﵽƽ�����Ҫ�����ǡ��������������������������������� �������� ��������
�� ��A����Ӧֹͣ�ˡ��� ������������������������������ B�����淴Ӧ�����ʾ�Ϊ��
�� ��C�����淴Ӧ�����ڼ������С� ��������������D�����淴Ӧ���������
![]() 2��ij�¶��£���һ�ݻ��ɱ�������У���Ӧ2A��g��+B��g����������
2C��g���ﵽƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ4mol��2 mol��4 mol�������¶Ⱥ�ѹǿ���䣬��ƽ�����������ߵ����ʵ��������µ�������ʹƽ�����Ƶ��ǣ�2003��ȫ�����ۣ����������� ��������
2��ij�¶��£���һ�ݻ��ɱ�������У���Ӧ2A��g��+B��g����������
2C��g���ﵽƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ4mol��2 mol��4 mol�������¶Ⱥ�ѹǿ���䣬��ƽ�����������ߵ����ʵ��������µ�������ʹƽ�����Ƶ��ǣ�2003��ȫ�����ۣ����������� ��������
������A�������롡�������������� B�����ӱ��������������� C��������1 mol ���� D��������1 mol
3����һ�������£���ӦA2���磩��B2���磩 ![]() 2AB���磩�ﵽƽ��״̬�ı�־
2AB���磩�ﵽƽ��״̬�ı�־
�� �ǡ������������������������������������������������������������� ������ ��������
�� A����λʱ��������n mol A2��ͬʱ������n mol��AB
�� B�������ڵ���ѹǿ����ʱ����仯
�� C����λʱ��������2n mol AB��ͬʱ������n mol��B2
�� D����λʱ���ڣ�����n mol A2��ͬʱ������n mol��B2
4����HI��������ܱ������У���һ�������·�����Ӧ.��������������������
�� 2H�ɣ��磩
![]() H2���磩����2���磩���ڷ�Ӧ����ƽ��״̬�Ĺ����У�����˵
H2���磩����2���磩���ڷ�Ӧ����ƽ��״̬�Ĺ����У�����˵
�� ����ȷ���ǡ��������������������������������������������������� ���������� ��������
�� A��HI���������ʵ�����ֽ����ʡ���
 ���� B��HI����������С����ֽ�����
���� B��HI����������С����ֽ�����
�� C��HI���������ʴ�����ֽ�����
�� D�����ж�HI���������ʺͷֽ����ʵ���Դ�С
5����Ӧ2�أ��磩���٣��磩
![]() 2�ڣ��磩��������
2�ڣ��磩��������
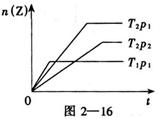
�� �ڲ�ͬ�¶�(��1����2)��ѹǿ��p1��p2���£�����Z��
�� ���ʵ����������ڣ����뷴Ӧʱ�䣨�����Ĺ�ϵ��ͼ
�� 2��16��ʾ���������ж���ȷ���� ������ ������ ��
�� A����1����2��p1��p2�������� ����������������B����1����2��p1��p2
�� C����1����2��p1��p2�������� ����������������D����1����2��p1��p2
6��ѹǿ�仯����ʹ���л�ѧ��Ӧ��ƽ�ⷢ���ƶ����ǡ������������������� ��������
�� A��H2(��)��I2(��) ![]() 2HI(��)��������B�� 3H2(��)��N2(��)
2HI(��)��������B�� 3H2(��)��N2(��) ![]() 2NH3(��)
2NH3(��)
�� C��2SO2(��)��O2(��) ![]() 2SO3(��)����D�� C(��)��CO2(��)
2SO3(��)����D�� C(��)��CO2(��) ![]() 2CO(��)
2CO(��)
7�����ݻ���ͬ��A��B�����ܱ������У��ֱ����2 mol SO2��1 mol O2,ʹ��������ͬ
�� �¶��·�����Ӧ.2SO2+O2 ![]() 2SO3,���ﵽƽ��,�ڷ�Ӧ�����У���A��������
2SO3,���ﵽƽ��,�ڷ�Ӧ�����У���A��������
�� ������䣬B��������ѹǿ���䣬��A�е�SO2��ת����Ϊ25%ʱ����B������SO2
�� ��ת����Ӧ�ǡ��������������������������������������������������� ������ ��������
�� ��A��25%������������ B����25%����������C����25%������ ����D��12.5%
8��ͬ��ͬѹ�£�����Ӧ��ֽ���8��ʱ�������Ҳ����8�����ǡ����������� ��������������
�� A��2NH3(g) ![]() ��N2(g)+3H2(g)��������B��2NO(g)
��N2(g)+3H2(g)��������B��2NO(g) ![]() ��N2(g)+O2(g)
��N2(g)+O2(g)
�� C��2NO3(g) ![]() ��4NO2(g)+O2(g)������������������������������������ D��2NO2(g)
��4NO2(g)+O2(g)������������������������������������ D��2NO2(g) ![]() ��2NO(g)+O2(g)
��2NO(g)+O2(g)
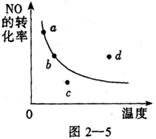 9��ͼ2��5�е������DZ�ʾ��������һ��ʱ��
9��ͼ2��5�е������DZ�ʾ��������һ��ʱ��
�� 2NO��O2 ![]() 2NO2���ų���������Ӧ��NO��ת������
2NO2���ų���������Ӧ��NO��ת������
�� �¶ȵĹ�ϵ���ߣ�ͼ�б���a��b��c��d�ĵ㣬���б�ʾ
�� δ�ﵽƽ��״̬����v(��)��v(��)�ĵ��ǡ������� ������ ��
A��a�㡡����B��b�㡡 ����������C��c�㡡����D��d��
10���Ѿ�������ѧƽ���ij���淴Ӧ�����ı�����ʹƽ����
�� ����Ӧ�����ƶ�ʱ�������й���������ȷ���ǡ��������� ��
�� ��A�����������������һ�����ӡ�������������B������������ʵ���һ������
�� ��C����Ӧ���ת����һ�����ӡ� ��������������D����Ӧ���Ũ��һ������
����ѡ����(�������12С�⣬ÿС��3�֣���36�֡�ÿ����1-2��ѡ������⣬��ѡ
�� ��2�֣���ѡ����ѡ��������)
11����������˵������֤����Ӧ.N2��3H2 ![]() 2NH3�Ѵﵽƽ��״̬�� ������������������������
2NH3�Ѵﵽƽ��״̬�� ������������������������
�� ��A��1��N��N�����ѵ�ͬʱ����3��H��H���γ�
�� ��B��1��N��N�����ѵ�ͬʱ����3��H��H������
�� ��C��1��N��N�����ѵ�ͬʱ����6��N��H������
 �� ��D��1��N��N�����ѵ�ͬʱ����6��N��H���γ�
�� ��D��1��N��N�����ѵ�ͬʱ����6��N��H���γ�
12��14����һ���¶��£�������ijһ��Ӧ��M��N����
�� �ʵ����淴Ӧʱ��仯��������ͼ�����б�������ȷ
�� ���ǡ������������������������������� ��������
�� ��A����Ӧ�Ļ�ѧ����ʽΪ.2M![]() N
N
�� ��B��t2ʱ�����淴Ӧ������ȣ��ﵽƽ��
�� ��C��t3ʱ������Ӧ���ʴ����淴Ӧ����
�� ��D��t1ʱ��N��Ũ����MŨ�ȵ�2��
13����һ�ܱ������У���Ӧ��aA������![]() bB������
bB������
�� ��ƽ������¶Ȳ��䣬�������������һ�������ﵽ�µ�ƽ��ʱ��B��Ũ����ԭ
�� ����60%���������������������������������������������������� ������ ��������
�� ��A��ƽ��������Ӧ�����ƶ��ˡ��� ����������B������A��ת���ʼ�����
�� ��C������B���������������ˡ����� ������ D��a>b
14��������ʵ�в���Ӧ����ɳ����ԭ�������͵��ǡ��������������������� �������� ��������
�� ��A����H2Sˮ��Һ�м���NaOH������S2������
������ B��������������ڰ���������Ӧ
�� ��C����ѹ�Ժϳɰ���������
������ D��500�����ұ����¸������ںϳɰ��ķ�Ӧ
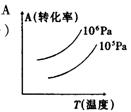 15����һ��ѧƽ��mA(g)+nB(g)
15����һ��ѧƽ��mA(g)+nB(g)
![]() PC(g)+qD(g),��ͼ��ʾ��
PC(g)+qD(g),��ͼ��ʾ��
�� ת������ѹǿ���¶ȵĹ�ϵ���ɴ˵ó�����ȷ�����ǣ�
�� ��A������Ӧ�����ȷ�Ӧ����m+n������p+q����
�� ��B������Ӧ�����ȷ�Ӧ����m+n������p+q��
�� ��C������Ӧ�Ƿ��ȷ�Ӧ����m+n������p+q����
�� ��D������Ӧ�Ƿ��ȷ�Ӧ����m+n������p+q��
16��������NH4�������ܱ������У���ij�¶��·������з�Ӧ.
�� NH4�ɣ���![]() NH3���磩��H��(��)��2HI(��)
NH3���磩��H��(��)��2HI(��) ![]() H2(��)��I2(��)������Ӧ��
H2(��)��I2(��)������Ӧ��
�� ��ƽ��ʱ������H2����0.5 mol������1������H�ɣ���4 mol������1����NH3��Ũ��Ϊ��������
�� A��3.5 mol������1������B��4 mol������1���� C��4.5 mol������1���� D��5 mol������1
17�����淴Ӧ.3A(��)==3B(?)+C(?)�����������������¶����ߣ�����ƽ����Է�����
�� ���б�С���ƣ��������ж��� ȷ���ǡ����������������������������� �������� ��������
�� ��A��B��C���ܶ��ǹ��塡������ �������� B��B��Cһ����������
�� ��C����CΪ���壬��Bһ�������塡���� D��B��C���ܶ�������
18��ij����ɱ���ܱ�����,ʢ��������A��B�Ļ������,��һ�������·�����
�� Ӧ:A+3B![]() 2C��ά���¶Ⱥ�ѹǿ����,���ﵽƽ��ʱ,���������ΪV��,����C��
2C��ά���¶Ⱥ�ѹǿ����,���ﵽƽ��ʱ,���������ΪV��,����C��
�� ������ռ10%,�����ƶ���ȷ���ǡ������������������������������� ����������������
�� ��ԭ�����������Ϊ1.2V��������������ԭ�����������Ϊ1.1V��;
�� �۷�Ӧ��ƽ��ʱ����A���ĵ�0.05V��; �ܷ�Ӧ��ƽ��ʱ����B���ĵ�0.05V��;
�� A���ڢۡ��� ������������B���ڢ� ��������������C���٢ۡ��� ����������D���٢�
19�����Ѵﻯѧƽ������з�Ӧ���� 2X��g����Y��g��![]() 2Z��g��
2Z��g��
�� ��Сѹǿʱ���Է�Ӧ������Ӱ���ǡ���������������������������������������������������������������������������
�� ��A���淴Ӧ������������Ӧ���ʼ�С��ƽ�����淴Ӧ�����ƶ�
 �� ��B���淴Ӧ���ʼ�С������Ӧ��������ƽ��������Ӧ�����ƶ�
�� ��B���淴Ӧ���ʼ�С������Ӧ��������ƽ��������Ӧ�����ƶ�
�� ��C�������淴Ӧ���ʶ���С��ƽ�����淴Ӧ�����ƶ�
�� ��D�������淴Ӧ���ʶ�����ƽ��������Ӧ�����ƶ�
20����֪ij���淴Ӧ���ܱ������н���.
�� A���磩��2B���磩 ![]() C���磩��D���ų���
C���磩��D���ų���
�� ����ͼ������a����һ�������¸÷�Ӧ�Ĺ��̡���ʹa
�� ���߱�Ϊb���ߣ��ɲ�ȡ�Ĵ�ʩ�ǡ������� ������ ��
�� ��A������A��Ũ�ȡ� ������������������������������ B����С�������ݻ�
�� ��C�����������������������������������������������D�������¶�
21��������A���磩����B���磩 ![]() ��C���磩����D���磩��ƽ����ϵ����������
��C���磩����D���磩��ƽ����ϵ����������
�� ��ʱ����ϵ��ƽ�����Ħ��������26��Ϊ29��������˵����ȷ���ǡ����������� ��������
�� A��m+n��p+q������Ӧ�Ƿ��ȷ�Ӧ������������B��m+n��p+q������Ӧ�����ȷ�Ӧ
�� C��m+n��p+q���淴Ӧ�Ƿ��ȷ�Ӧ ���������� D��m+n��p+q���淴Ӧ�����ȷ�Ӧ
22�����ܱ������У��������з�Ӧ.����������������������������������������������������
�� 2A���磩��B���磩��C���� ![]() D���磩���ţ��磩�� ��������
D���磩���ţ��磩�� ��������
�� �ﵽƽ�������˵������ȷ���ǡ��������������������������������� ��������
�� ��A�������¶�������£�����һЩϡ������ѹǿ����ƽ�ⲻ�ƶ�
�� ��B�������¶�ѹ�����£�����C���磩����B��ת���ʽ�����
�� ��C�����������£�����ƽ����ϵ��A��������������С
�� ��D�����¶ȡ�ѹǿ���ݻ�����ͬʱ������һ�ܱ������м���2 mol A��1 mol B��1 molC��
�� ����ƽ��ʱ����������D��E��Ũ�ȷֱ����
���������
23��(9��)�������ʵ�����A��B��C��D�������ʻ��,�������·�Ӧ: aA+bB![]() cC(��)+dD
cC(��)+dD
�� ����Ӧ����һ��ʱ����A������nĦ��B������![]() nĦ��C������
nĦ��C������![]() nĦ��D
nĦ��D
�� ������nĦ,��ʱ�ﵽ��ѧƽ��:
�� ��1���û�ѧ����ʽ�и����ʵ�ϵ��Ϊ :a =______��b=________��c=______��d=______��
�� ��2����ֻ�ı�ѹǿ,��Ӧ�ٶȷ����仯,��ƽ�ⲻ�����ƶ�,�÷�Ӧ�и����ʵľۼ�״̬:
������ A___________��B__________��C____________��D________________
�� ��3����ֻ�����¶�,��Ӧһ��ʱ���,��֪�������������ʵ����ִﵽ���,��÷�ӦΪ
���� __________________��Ӧ(����ȡ������ȡ�)
24����9�֣���ѧƽ���ƶ�ԭ����ͬ��Ҳ����������ƽ�⣬��֪�ڰ�ˮ�д�������ƽ��.
�� NH3��H2O ![]() NH3��H2O
NH3��H2O ![]() NH4+��OH-
NH4+��OH-
�� ��1����ˮ�м���MgCl2����ʱ��ƽ����__________�ƶ���OH����Ũ��__________��
���� �� NH4+��Ũ��_____��
��2����ˮ�м���Ũ���ᣬƽ����___________�ƶ�����ʱ��Һ��Ũ�ȼ�С��������
������___________��___________��___________��
�� ��3����Ũ��ˮ�м�������NaOH���壬ƽ����______�ƶ�����ʱ���������� __________��
25����6�֣���ij�̶��ݻ����ܱ������У��������л�ѧƽ��.
�� ��A���磩
![]() ��B���磩����C���磩�����¶Ȳ���������£����������ٳ���
��B���磩����C���磩�����¶Ȳ���������£����������ٳ���
�� һ������A���ʣ����´ﵽƽ��ʱ���ж�������������й��������ı仯����
�� �������пհ�����д��������С�����䡱��
�� ��1����a=b+cʱ��B�����ʵ�������___________��
�� ��2����a��b+cʱ��A�����ʵ�������___________��
�� ��3����a��b+cʱ��A��ת����___________��
26����8�֣���һ���¶��£���2 mol SO2��1 mol O2ͨ��һ��һ���ݻ����ܱ��������
�� �����·�Ӧ.2SO2��O2��![]() 2SO3�����˷�Ӧ���е�һ���̶�ʱ����Ӧ�����
2SO3�����˷�Ӧ���е�һ���̶�ʱ����Ӧ�����
�� �ʹ��ڻ�ѧƽ��״̬�����ڸ������У�ά���¶Ȳ��䣬��a��b��c�ֱ������ʼ����
�� ��SO2��O2��SO3�����ʵ���(mol)�����a��b��cȡ��ͬ����ֵ�����DZ�������һ
�� �������ϵ�����ܱ�֤�ﵽƽ��ʱ����Ӧ���������������İٷֺ����Ը�����ƽ
�� ��ʱ��ȫ��ͬ������д���пհ�.
�� ��1����a=0��b=0����c=������ ��
�� ��2����a=0.5��b=������ ��c=������ ��
�� ��3��a��b��cȡֵ���������һ��������(������������ʽ��ʾ������һ��ֻ��a��c��
���� ����һ��ֻ��b��c)_________________
27����12�֣���ˮ��Һ�гȺ�ɫ��C��2O72-���ɫ��C��O42-������ƽ���ϵ.
����C��2O72-��H2O ![]() 2C��O42-��2H+���ѣ�2C��2O7����ˮ���ϡ��Һ�dz�ɫ��
2C��O42-��2H+���ѣ�2C��2O7����ˮ���ϡ��Һ�dz�ɫ��
�� ��1����������Һ�м���NaOH��Һ����Һ��___________ɫ����Ϊ__________��
�� ��2�����Ѽ���NaOH��Һ��(1)���ټ������ϡH2SO4������Һ��___________ɫ��
���� �� ��Ϊ__________��
�� ��3����ԭ��Һ�м���Ba(NO3)2��Һ(��֪B��C��O4Ϊ��ɫ����)��ƽ��___________����������
��Һ��ɫ��__________��
���
һ��ѡ���� (�������10С�⣬ÿС��2�֣�ÿС��ֻ��һ���𰸷�������)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | C | C | B | C | A | B | A | C | B |
����ѡ����(�������12С�⣬ÿС��3�֣���36�֡�ÿ����1-2��ѡ������⣬��ѡ
�� ��2�֣���ѡ����ѡ��������)
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| AC | D | AC | BD | A | D | CD | A | C | BC |
| 21 | 22 | ||||||||
| BD | AC |
���������
23����2��1��3��2
�������̻�Һ���̡���
�Ƿ���
24�����ң���С������
���ң�OH-��NH3•H2O��NH3
����NaOH�����ܽ⣬��Һ�в�������
25���Ų��䡡 �Ƽ�С�� �Ǽ�С
26����c = 2������ b = 0.25��c = 1.5������ a + c = 2,2b + c = 2
27���Żƣ��к�H+ƽ��������Ӧ�����ƶ�
�ƳȺ�ɫ������������Ũ��ƽ�����淴Ӧ�����ƶ�
������Ӧ�ƶ�����dz