期中测试卷
一、选择题(每小题只有一个正确选项,每小题2分,共计20分)
1、下列四种元素中,与其它三种元素分类不同的是 ( )
A.N B.As C.Sn D.Bi
2、将一定量的Ag2SO4固体置于容积不变的容器中,在某温度下发生下列反应:![]() ,经10分钟后,反应达到平衡,此时C(SO3)=0.4摩/升,C(SO2)=0.1摩/升,则下列陈述不正确的是
( )
,经10分钟后,反应达到平衡,此时C(SO3)=0.4摩/升,C(SO2)=0.1摩/升,则下列陈述不正确的是
( )
A.SO3的分解率为20% B.平衡时,VO2=0.005摩/升・分
C.容器内气体的密度为40克/升 D.加压,容器内固体质量不变
3、NO和CO都是汽车尾气里的有害物质,它们能缓慢地反应生成N2和CO2。对此反应,下列叙述正确的是 ( )
A.使用催化剂不能改变反应速率 B.使用催化剂能加快反应速率
C.改变压强对反应速率没有影响 D.降低压强能增大反应速率
4、使用化肥普钙和重钙最好是 ( )
A.与草木灰并用 B.与农家肥料(厩肥)并用
C.施用于碱性土壤 D.施用于含Fe3+的酸性土壤
5、可逆反应2SO2+O2![]() 2SO3达平衡时, 通入18O2, 再次平衡时, 18O存在于
2SO3达平衡时, 通入18O2, 再次平衡时, 18O存在于
A.SO3 O2 B.SO2 SO3 C.SO2 O2 D.SO2 O2 SO3
6、白磷跟热的KOH溶液发生如下反应:P4+OH―+H2O ® H2PO2―+PH3,此反应中氧化剂与还原剂的物质的量之比为 ( )
A.1∶3 B.3∶1 C.4∶3 D.3∶4
7、在一密封烧瓶中注入 NO2,在 25℃时建立下列平衡: 2NO2(g) ![]() N2O4(g)( 正反应是放热反应),若把烧瓶置于100℃的沸水中,下列哪些物理量不变: ①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
( )
N2O4(g)( 正反应是放热反应),若把烧瓶置于100℃的沸水中,下列哪些物理量不变: ①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度
( )
A.③⑤ B.③④ C.②④ D.①③
8、V1升H2和V2升N2在一定条件下反应,反应达平衡后混和气体为V3升(都在同温同压下测得),则生成NH3的体积是 ( )
A.V1+ V2- V3 B.V1+
V2+V3
C.2(V1+ V2)- V3 D.不知氮气的转化率,无法计算
9、改变以下反应的条件,能提高反应物活化分子百分率的是 ( )
①温度 ②浓度 ③压强 ④正催化剂
A.①④ B.②③ C.①② D.③④
10、将浓硝酸滴在蓝色石蕊试纸上,产生的现象为 ( )
A.变红色 B.变黑色 C.变白色 D.先变红,后褪色
二、选择题(本题每小题有1-2个正确选项,每小题2分,共30分)
11、下列反应起了氮的固定作用的是 ( )
A.N2和H2在一定条件下反应生成NH3 B.NO和O2反应生成NO2;
C.NH3经催化氧化生成NO; D.由氨气制碳铵和硫铵
12、为消除NO和NO2对大气的污染,常用碱液吸收混合气。现有m molNO2和n molNO组成的混合气体,用浓度为a mol/L的氢氧化钠溶液吸收,无任何气体剩余,则至少需要NaOH溶液的体积为:(单位:L) ( )
A.m/a B.2m/3a C.2(m+n)/3a D.(m+n)/a
13、对于A+2B![]() C(正反应是放热反应)的可逆反应,已知C是气体,达平衡后同时升高温度并降低压强,又达到新的平衡。若第二次平衡时混和物中C的含量与第一次平衡相同,则下列推断正确的是 ( )
C(正反应是放热反应)的可逆反应,已知C是气体,达平衡后同时升高温度并降低压强,又达到新的平衡。若第二次平衡时混和物中C的含量与第一次平衡相同,则下列推断正确的是 ( )
A.B不一定是气态物质 B.B一定是气态物质
C.A一定不是气态物质 D.A一定是气态物质
14、对于mA(g)+nB(g)=pC(g)+q D(g)的平衡体系,当升高温度时,体系的平均相对分子质量从33变成33.8,则下列说法正确的是 ( )
A.m+n>p+q 正反应是放热反应 B.m+n>p+q 正反应是吸热反应
C.m+n<p+q 逆反应是放热反应 D.m+n<p+q 逆反应是吸热反应
15、(NH4)2Cr2O7是一种受热易分解的盐,下列各组对(NH4)2Cr2O7受热分解产物的判断,符合实际的是 ( )
A.Cr2O3+N2+H2O B.CrO3+N2+H2O C.Cr2O3+NH3+H2O D.CrO3+NO+H2O
16、密度为0.91g/cm3的氨水,质量分数为25%,该氨水用等体积的水稀释后,所得溶液溶质的质量分数为 ( )
A.12.5% B.大于12.5% C.小于12.5% D.无法确定
17、将充满NO2和O2的量筒倒立于盛有水的水槽中,经过一段时间后,水上升到量筒体积的一半处停止了,则剩余气体的成份是 ( )
A.NO2 B.NO C.O2 D.NO或O2
18、在11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,1molCu2+能氧化P的物质的量为 ( )
A.0.4mol B.2.2mol C.0.2mol D.0.33mol
19、在一定温度下,在一固定容积的密闭容器中存在着如下的平衡:2NO2(g) ![]() N2O4(g)现在维持容器温度和容积均不变的情况下,向容器中补充a克NO2,待建立新的平衡时,平衡混和物中NO2的含量比原平衡状态 ( )
N2O4(g)现在维持容器温度和容积均不变的情况下,向容器中补充a克NO2,待建立新的平衡时,平衡混和物中NO2的含量比原平衡状态 ( )
A.增大 B.减小 C.不变 D.以上三种情况都有可能
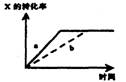 20、见右图,曲线 a表示一定条件下,可逆反应:
20、见右图,曲线 a表示一定条件下,可逆反应:
X(g)+ Y(g)![]() 2Z(g)+ W(s)(正反应是吸热反应)X的转化率与时间的关系。若欲使a曲线变为b曲线,可采取的措施是 ( )
2Z(g)+ W(s)(正反应是吸热反应)X的转化率与时间的关系。若欲使a曲线变为b曲线,可采取的措施是 ( )
A.加入负催化剂 B.增大Y的浓度
C.降低温度 D.减小反应体系压强
21、有一个固定体积的密闭容器中,保持一定温度,进行以下反应:
H2(g)+ Br2(g)![]() 2HBr(g),已知加入 l mol H2和 2mol Br2时,达到平衡后,生成 a molHBr。在相同条件下, 起始时加人H2、Br2、HBr的物质的量分别为x、y、z(均不为零),如果仍保持平衡后各组分的物质的量分数不变,以下推断正确的是 (
)
2HBr(g),已知加入 l mol H2和 2mol Br2时,达到平衡后,生成 a molHBr。在相同条件下, 起始时加人H2、Br2、HBr的物质的量分别为x、y、z(均不为零),如果仍保持平衡后各组分的物质的量分数不变,以下推断正确的是 (
)
A.x、y、z应满足的关系是 y=2x
B.x、y、z应满足的关系是 4x+z=2y
C.达平衡时 HBr的物质的量为(x+y+z)a/3
D.达平衡时HBr物质的量一定仍为a mol
22、下列图像中,能表示可逆反应A2(g)+3B2(g)![]() 2AB3(g)(正反应为放热反应)平衡体系的是
( )
2AB3(g)(正反应为放热反应)平衡体系的是
( )

23、在一定温度下,将n摩的PCl5通入定容积的密闭容器中达平衡:PCl5(气)![]() PCl3(Q气)+Cl2(气),测得压强为P1,若再向容器中通入n摩的PCl5,又达到平衡后,压强为P2,则下列关系式正确的是 ( )
PCl3(Q气)+Cl2(气),测得压强为P1,若再向容器中通入n摩的PCl5,又达到平衡后,压强为P2,则下列关系式正确的是 ( )
A.P1=2P2 B.2P1=P2 C.2P1>P2 D.2P1<P2
24、![]() 一定温度时于密封容器中发生反应:mA(g)+nB(g) pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是 (
)
一定温度时于密封容器中发生反应:mA(g)+nB(g) pC(g),达平衡后,若将气体体积压缩到原来的1/2。当再达平衡时C的浓度是原来的1.9倍,则下列叙述正确的是 (
)
A.平衡向正反应方向移动 B.C气体的质量分数增大
C.气体A的转化率降低 D.m+n>p
25、将N2、H2以体积比1:1混合均匀,分成三等份,分别充入甲、乙、丙三个装有相同催化剂且容积不变的真空密闭容器中,在相同温度下使其分别达到化学平衡状态。已知平衡时甲中N2的转化率为20%,乙中H2的转化率为30%,丙中混合气体的平均相对分子质量为16,则有关三容器内反应的叙述正确的是( )
A.容器中起始反应速率相同
B.三容器平均反应速率的大小关系为:甲>乙>丙
C.三容器的平均反应速率的大小是:丙>乙>甲
D.平衡时,丙中NH3的体积分数比甲中NH3的体积分数大。
三、填充题(本大题共5小题,共计32分)
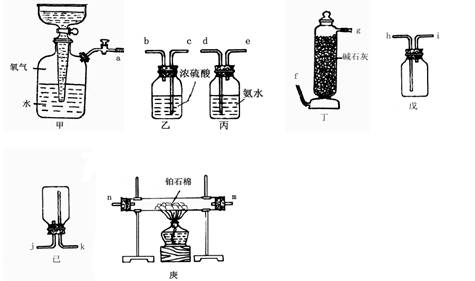
26、(14分)氨的催化氧化制硝酸的关键步骤是用氧气来氧化氨气制取二氧化氮。请用以下提供的仪器及试剂(所提供的仪器和试剂有多余的),设计组装一套实验装置,以铂为催化剂用氧气氧化氨气制取二氧化氮。
(1)应选用的仪器是:________________ (填仪器下边的甲、乙、丙 … 等符号)
(2)用玻管和胶管(未画出)连接上述仪器,这些仪器的接口的连接顺序是 (a、b、c … 等填写) :a接______,________接_______ ,_______接________,______接________,_______ 接_______ ,…
(3)庚装置中发生的化学反应的方程式是:____________________ 。
(4)写出获得甲装置中的氧气的任意两种制取方法(用两个反应方程式来表示):
_________________________________、________________________ 。
28、(8分)有甲、乙两个容积相等的密闭容器,反应过程中,甲能保持恒温恒容,乙能保持恒温恒压。现在温度相同情况下,两容器中均发生:
![]() 3A(g)+B(g)
2C(g)+D(g)。
3A(g)+B(g)
2C(g)+D(g)。
(1)取2 molC和1 molD放在甲中,取6 molA和2 molB放入乙中,均达平衡后,甲中C%与乙中C%的关系是:甲 乙。(填<、>、=或无法确定,下同)
(2)取3molA和2molB放入甲中,取2molC、1molD和1molB放入乙,达平衡时,D的体积分数的关系是:甲 乙。
(3)取2molC和1molD及1mol稀有气体放入甲中,取3molC、1molD放入乙中,达到平衡后,D的转化率的关系是:甲 乙。
(4)取1.5molA、0.5molB、1molC和0.5molD放入甲容器中,取3molA、1molB放入乙中,达到平衡时,B的质量分数的关系是:甲 乙。
29、(10分)某化学反应2A==B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
|
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800 | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800 | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空;
(1)在实验1,反应在l0min至20 min时间内平均速率为_____mol/(L・min)
(2)在实验2,A的初始浓度c2= _________mol/L,反应经达平衡,可推测实2中还隐含的条件是________________________________。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1,则υ3_υ1;(填>、=、<,且C3 _________1.0mol/L (填>、=、<).
(4)比较实验4和实验1,可推测该反应是__________反应(选填吸热、放热)
四、计算题(本大题共2小题,共计18分)
30、(8分)常温常压下,将30mLNO2和O2的混合气体通入倒置于水槽并充满水的量筒中,充分反应后,剩余5mL尾气。试问在原来的混合气体里NO2和O2各多少亳升?
30、(10分)在80℃和1.01×105Pa下,用图示装置进行如下实验,A、C两筒分别装有无色气体,它们可能含有NH3、O2、N2、H2S、NO、CO2等气体,B管内装有固体,推动A的活塞使A筒内气体缓缓地全部通过B后进入C筒,C中的气体由无色变成红棕色,但其体积换算成同温同压时并未变化。
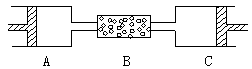
(1)C中发生的反应为 _____ 。已知C中是单一气体,它是 ___ (若有多种可能的答案,需一一列出),将反应后C中的气体用水充分吸收,在同温同压下气体体积减少一半,则与水反应前C中的气体是 ______ (有多种可能答案需一一列出)。
(2)若实验前A、C中的气体体积(换算成标况)分别为1.40L和2.24L,且A中的气体经过B管后,B管质量增加1.40g,通过计算机推理可判断A中含气体是 ____ ,其质量为 ____ ___g。
期中测试卷参考答案
1、C 2、D 3、B 4、B 5、D 6、A 7、A 8、A 9、A 10、D
11、A 12、D 13、C 14、BD 15、A 16、C 17C 18、C 19、B 20、AD 21、BC 22、AC 23、C 24、C 25、B
26、 (1) 甲、丙、丁、戊、庚 ( 3分)
(2) a 接d , e 接 f , g 接 n , m 接h ( 4分)
(3)4NH3+5O2![]() 4NO+6H2O;2NO+O2=2NO2
4NO+6H2O;2NO+O2=2NO2
(4)2KCl03 ![]() 2KCl+3O2↑;2H2O2
2KCl+3O2↑;2H2O2![]() 2 H2O+O2↑
2 H2O+O2↑
27、(1)<,(2)=,(3)<,(4)=
28、(1)0.013 (2) 1.0 , 催化剂 (3)>, > (4)吸热
29、(1)2NO+O2=2NO2,NO,NO、NO2;CO2和O2,2.6g
32、NO2:20 mL, O2:10 mL 或者:NO2:27 mL, O2:3mL