理科综合能力测试[化学部分](六)
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
原子量: O 16,S 32,Fe 56,
1.蒸馒头时,在发酵粉的面团里加入些纯碱溶液的作用是:①使馒头变白;②增加甜味;③除去发酵时生成的酸;④产生CO2使馒头体积膨胀
A.①③ B.② C.③④ D.①④
2.用惰性电解M(NO3)x的水溶液,当阴极上增重a g时,在阳极上同时产生b L O2(标准状况),从而可知M的相对原子质量为
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
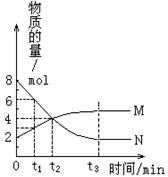 3.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如右图,下列表述中正确的是
3.在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如右图,下列表述中正确的是
A.反应的化学方程式为:2M![]() N
N
B.t2时,正逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
4. 某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO―与ClO3―的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为
A.21:5 B.11:3 C.4:1 D.3:1
5.V mLFe2(SO4)3溶液中含a g SO42―,取出溶液![]() mL,用水稀释成2V mL,则稀释后溶液Fe3+的物质的量浓度是
mL,用水稀释成2V mL,则稀释后溶液Fe3+的物质的量浓度是
A.![]() mol・L―1 B.
mol・L―1 B.![]() mol・L―1
mol・L―1
C.![]() mol・L―1
D.
mol・L―1
D.![]() mol・L―1
mol・L―1
6.pH=5的NH4Cl溶液由水电离出来的H+离子浓度为a mol・L―1,pH=5的HCOOH溶液由水电离出来的H+离子浓度为b mol・L―1,下列a和b的关系正确的是
A.a=b B.a=10―4b C.a=104b D.无法确定
7.L―多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下:
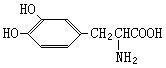
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果。下列关于L―多巴酸碱性的叙述正确的是
A.既没有酸性,又没有碱性 B.既具有酸性,又具有碱性
C.只有碱性,没有酸性 D.只有酸性,没有碱性
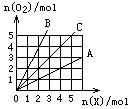 8.右图中横坐标表示完全燃烧时耗用可燃性气体X(X=A、B、C)的物质的量n(X),纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃性气体,C是A和B的混合气体,则C中n(A)与n(B)的比为
8.右图中横坐标表示完全燃烧时耗用可燃性气体X(X=A、B、C)的物质的量n(X),纵坐标表示消耗O2的物质的量n(O2),A、B是两种可燃性气体,C是A和B的混合气体,则C中n(A)与n(B)的比为
A.2:1 B.1:2
C.1:1 D.任意比
第Ⅱ卷
(非选择题,共3小题,共50分)
9.(18分)如图所示:黑色固体A有以下转化关系,每个方框表示有一种反应或生成物(反应条件及生成的水已略去),其中C、F常温下为无色气体,D、E有共同的阳离子。
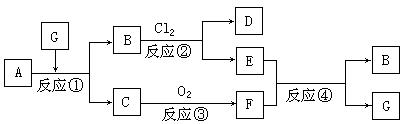
(1)写出B和C的化学式:B_______________,C_______________
(2)写出反应①、②、④的离子方程式
① ________________________________________
② ________________________________________
④ ________________________________________
10.(16分)某有机物A(C4H6O5)广泛存在于许多水果内,尤以苹果、葡萄、西瓜、山楂为多。该化合物具有如下性质:
① 在25℃时,电离常数K1=3.99×10―4,K2=5.5×10―6
② ![]()
③ 1 molA![]() 慢慢产生1.5 mol气体
慢慢产生1.5 mol气体
④ A在一定温度下的脱水产物(不是环状化合物)可和溴水发生加成反应
试回答:
(1)根据以上信息,对A的结构可作出的判断是___________(多选扣分)
A.肯定有碳碳双键 B.有两个羧基
C.肯定有羟基 D.有―COOR官能团
(2)有机物A的结构简式(不含―CH3)为______________________
(3)A在一定温度下的脱水产物和溴水反应的化学方程式:
_____________________________________________________________
(4)A的一个同类别的同分异构体是________________________________
11.(16分)氯气和二氧化氮气体在室温下可以化合生成一种新的气态化合物A,为了测定A的组成进行以下实验:取Cl2、NO2混合气体5 L,测定反应后所得气体体积随Cl2在原混合气体中所占体积分数x的变化而变化的规律。实验测知当Cl2所占体积分数为0.2或0.6时,反应后的总体积均为4 L。
(1)(6分)通过分析和计算求得化合物A的化学式为_________________,发生反应的化学方程式为__________________________________________________。
(2)(10分)试讨论当x的取值范围不同时,反应后总体积V随x变化的函数关系。将讨论结果填写在下列表格中:
| x的取值范围 | 反应后的总体积V |
理科综合能力测试(化学部分)参考答案及评分标准
Ⅰ卷 每小题6分,共48分
1.C 2.C 3.D 4.C 5.A 6.C 7.B 8.A
Ⅱ卷 包括3小题,共50分
9.(18分)
(1)FeSO4,H2S (每空3分,共6分)
(2)① FeS+2H+=H2S↑+Fe2+
② 2Fe2++Cl2=2Fe3++2Cl―
④ 2Fe3++SO2+2H2O=2Fe2++SO42―+4H+
(每式4分,共12分)
10.(16分)
(1)BC (4分)
(2)
![]() (4分)
(4分)
(3)
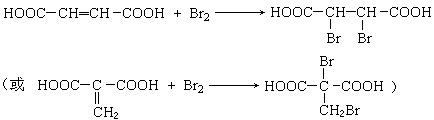 (4分)
(4分)
(4) 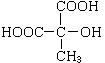 (其它合理答案也对)(4分)
(其它合理答案也对)(4分)
11.(16分)
(1)NClO2(元素符号顺序可颠倒),Cl2+2NO2=2NClO2 (每空3分,共6分)
(2)
| x的取值范围 | 反应后的总体积V |
| x≤ | V=5(1―x) (3分) |
| x> | V=2.5(x+1) (3分) |
(共10分)