08届高三年级理综第五次模拟考试
理科综合能力试题
理科综合能力测试试题卷分选择题和非选择题两部分。第一部分(选择题),第二部分(非选择题)。共300分,考试时间150分钟。
注意事项:
1.答题前,考生务必将姓名和准考证号填写在每一页答题纸上的指定位置;
2.将每科答案按照要求填写在答题卡指定位置,填写在试卷上无效;
以下数据可供解题时参考;
相对原子质量(原子量):H―1;O―16;S―32;Fe―56;Cu―64
第Ⅰ卷(选择题,21小题,共126分)
一、选择题(本题包括13小题,每小题只有一个选项符合题意)
1.2007年10月24日18时05分,嫦娥一号绕月卫星发射成功。是、中国科学院院士、中国探月工程首席科学家欧阳自远在此间举行的一次学术柏高会上介绍说,科学技术的发展,将使月球上两中资源给地球能源问题带来希望;一是月球的太阳能;二是月壤中气体,如氢、氦、氖、氩、氮等资源。下列有关氮元素的叙述不正确的是 ( )
A.硝化细菌可将氨态氮转化为硝态氮,有利于植物对氮元素的吸收。
B.反硝化细菌属于分解者,在无氧条件下可将氨态氮转化为氮气中耕松土可防止氮元素的流失。
C.土壤中的含氧量将影响氮元素的吸收。
D.圆褐固氮菌可独立固氮,属于异养型生物。
|
A.该细胞在抗原再次进入体内时,能够识别抗
原并迅速分泌大量抗体从而清除抗原。
B.该细胞可与骨髓瘤细胞融合,融合时可
产生3种类型的杂交瘤细胞。
C.抗体蛋白上的糖基团是在2中形成的。
D.如果抗体种氨基酸数目为a,则细胞核
内控制该抗体蛋白合成基因的编
码去的碱基数目等于6a.
3.下列各项中与右图曲线变化相符的是 ( )
(1)光照强度对光合作用速率的影响
(2)在有限环境条件下,之、种群增长速率随种群的增长时间(过程)的关系。
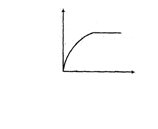 (3)二氧化碳浓度对光合作用速率的影响。
(3)二氧化碳浓度对光合作用速率的影响。
(4)菠菜叶片从幼叶生长至老叶过程中,钙离子相对含量的变化
(5)血浆中氧气浓度对红细胞吸收氧气速率的影响。
(6)氧浓度对水稻吸收硅元素相对速率的影响
(7)大豆种子萌芽至幼苗生长过程中自由水/结合水比值的变化。
A.(1)(3)(4)(5)(7) B.(1)(3)(5)(6)
C.(1)(3)(5) D.(2)(4)(5)(7)
4.关于“克隆羊”、“试管羊”、“转基因羊”的说法合理的是 ( )
A.在培育过程中,都用到了动物细胞培养技术、核移植技术、胚移植技术、
B.它们的遗传物质都只来自一个亲体。
C.它们是通过相同的生殖方式获得的
D.它们在形成过程中,一般都有卵细胞参与。
5.下表各种概念之间的关系,其中与在多细胞生物中“1个体、2器官、3组织、4细胞”四个概念之间的关系相似的是 ( )
| 选项 | 1 | 2 | 3 | 4 |
| A | 特异性免疫 | 细胞免疫 | T细胞 | 抗体 |
| B | DNA | 基因 | 非编码区 | 内含子 |
| C | 生殖 | 无性生殖 | 营养生殖 | 植物组织培养 |
| D | 应激性 | 本能 | 非条件反射 | 印随学习 |
6.有关化学用语正确的是 ( )
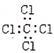 A.乙烯的最简式C2H
A.乙烯的最简式C2H
B.四氯化碳的电子式
C.用铜为阳极电解硫酸铜液体的阳极反应式:4OHˉ―4eˉ=O2↑+2H2O
D.以知0.5稀硫酸与1mol NaOH稀溶液反应放热57.3KJ,则热化学方程式:
H2SO4(aq)+2NaOH(aq)=Na2SO4(aq)+2H2O(l);△H=-114.6kJ/mol
7.下列反应的离子方程式真确的是 ( )
A.向沸水中滴入少量饱和氯化铁溶液 Fe3++3H2O Fe(OH)3↓+3H+
B.漂白粉溶液中通入过量二氧化碳:Ca2++2ClOˉ+H2O+CO2 CaCO3↓+2HClO
C.碳酸氢钠溶液与少量石灰水反应:HC3Oˉ+Ca3++OHˉ CaCO3↓+ H2O
D.氢氧化钠溶液中滴加少量氯化铝溶液:Al3++4OHˉ AlO2ˉ+2H2O
8.下列有关比较中,大小顺序排列错误的是 ( )
A.热稳定性:PH3>H2S>HB>NH3
B.物质的熔点:石英>食盐>冰>贡
C.结合质子的能力:CO32->CH3COOˉ>SO42-
D.分散系中分散质粒子的直径;Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
9.一种新型的燃料电池,它的多孔镍板为电极插入KOH溶液中,然后分别向两级通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH=4K2CO3+10H2O,有关此电池的推断正确的是
( )
A.负极反应为14H2O+7O2+28eˉ=28OHˉ
B.放电一段时间后,负极周围的pH升高
C.放电过程中KOH的物质的浓度不变
D.每消耗1molC2H6,则电路上转移的电子为14mol
|
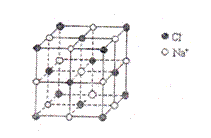 10.用表示阿伏伽德罗常数,下列说法中正确的是 ( )
10.用表示阿伏伽德罗常数,下列说法中正确的是 ( )
A.1L1mol/L的醋酸溶液中离子总数为2NA
B.0.5mol熔融的KHSO4中含有阳离子的数目
为0.1NA
C.0.4molNaCl晶体中含有右图所示的结构单元
的数目为0.1NA
D.标准状况下,22.4LCH2Cl2和CHCl3 的混合
物所含有分子数目为NA
11.对于相同体积的溶液(浓度为c1)和(NH4)2CO3溶液(浓度为c2),若其中CO32―的物质的量浓度相同,则c1和c2的关系是 ( )
A.c1=2c2 B.c1>c2 C.c1=c2 D.c1<c2
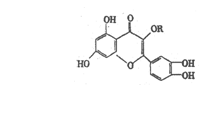 12.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是 ( )
12.天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂,关于维生素P的叙述错误的是 ( )
A.可以和溴水反应
B.1mol维生素P最多可以和8molH2加成
C.分子中有三个苯环
D.1mol维生素P可以和4molNaOH反应
13.a g 铁粉与含有H2SO4 的CuSO4溶液完全反应后,铁完全消失,并得到a g铜,则参与反应的CuSO4与H2SO4的物质的量之比为: ( )
A.1:7 B.7:1 C.7:8 D.8:7
二、选择题(本题包括8小题,每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对得6分,选对但不全的得3分,有选错的得0分)
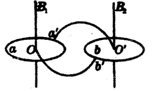
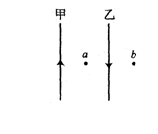 14.如图所示,同一平面内有两根固定的相互平行的长直导线甲和乙,现通有大小相等方向相反的电流。a、b两点与两导线共面。其中a点与两导线间距离均为r,b点在导线乙的右侧,与乙距离也为r。测得a点磁感应强度的大小为B,则去掉导线甲后,b点的磁感应强度方向和大小为 ( )
14.如图所示,同一平面内有两根固定的相互平行的长直导线甲和乙,现通有大小相等方向相反的电流。a、b两点与两导线共面。其中a点与两导线间距离均为r,b点在导线乙的右侧,与乙距离也为r。测得a点磁感应强度的大小为B,则去掉导线甲后,b点的磁感应强度方向和大小为 ( )
A.垂直纸面向外,3B
B.垂直纸面向外,2B
C.垂直纸面向外,B
D.垂直纸面向外,![]()
15.两个完全相同的条形磁铁,放在平板AB上,磁铁的N、S极如图所示,开始时平板及磁铁皆处于水平位置,且静止不动。
(1)现将AB突然竖直向上平移(平板与磁铁之间始终接触),并使之停在![]() c处,结果发现两个条形磁铁吸在了一起
c处,结果发现两个条形磁铁吸在了一起
 (2)如果将AB从原来位置突然竖直向下平移,并使之停在位置
(2)如果将AB从原来位置突然竖直向下平移,并使之停在位置![]() 处,结果发现两条形磁铁也吸在了一起,则下列说法正确的是 ( )
处,结果发现两条形磁铁也吸在了一起,则下列说法正确的是 ( )
A.开始时两磁铁静止不动说明磁铁间的作用是排斥力
B.开始时两磁铁静止不动说明磁铁间的吸引力等于静摩擦力
C.第(1)过程中磁铁开始滑动时,板正在向上减速
D.第(2)过程中磁铁开始下滑时,平板正在向下减速
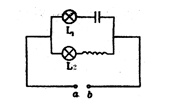 16.两个相同的白枳灯,L1和L2,接到如图所示的电路中,灯L1与电容器串联,灯 L2与电感线圈串联,当a、b处接电压最大Um,频率为f的正弦交流电源时,两灯都发光,且亮度相同,更换一个新的正弦交流电源达到稳定工作后,灯L1的亮度高于L2的亮度,新电源的电压最大值和频率可能是 ( )
16.两个相同的白枳灯,L1和L2,接到如图所示的电路中,灯L1与电容器串联,灯 L2与电感线圈串联,当a、b处接电压最大Um,频率为f的正弦交流电源时,两灯都发光,且亮度相同,更换一个新的正弦交流电源达到稳定工作后,灯L1的亮度高于L2的亮度,新电源的电压最大值和频率可能是 ( )
A.最大值仍为Um,而频率大于f
B.最大值仍为Um,而频率小于f
C.最大值小于Um,而频率仍为f
D.最大值小于Um,而频率小于f
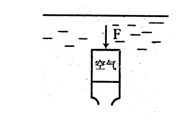 17.如图,某同学将空的薄金属筒开口向下压入水中,设水温均匀且恒定,筒内空气无泄漏,不计气体分子间相互作用,则被淹没的金属筒在缓慢下降过程中,筒内空气体积减小时
17.如图,某同学将空的薄金属筒开口向下压入水中,设水温均匀且恒定,筒内空气无泄漏,不计气体分子间相互作用,则被淹没的金属筒在缓慢下降过程中,筒内空气体积减小时
( )
A.气体向外界放热
B.气体分子热运动的平均动能不变
C.气体在单位时间与器壁单位面积
上碰撞的分子数不变
D.筒上外加压力F在逐渐减小
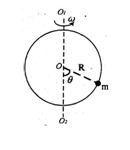 18.一种玩具的结构如图所示。竖直放置的光滑铁圈环的半径为R=20cm,环上有一个穿孔的小球m,仅能沿环作无摩擦滑动,如果圆环绕着通过环心的竖直轴O1O2以10rad/s的角速度旋转,(g取10
18.一种玩具的结构如图所示。竖直放置的光滑铁圈环的半径为R=20cm,环上有一个穿孔的小球m,仅能沿环作无摩擦滑动,如果圆环绕着通过环心的竖直轴O1O2以10rad/s的角速度旋转,(g取10![]() )则小球相对环静止时与环心O
)则小球相对环静止时与环心O
的连线与O1O2的夹角![]() 可能是
( )
可能是
( )
A.30°
B.45°
C.60°
D.75°
|
盘顺时针转动时 ( )
A.b盘总是顺时针转动
B.b盘总是逆时针转动
C.若B1、B2同向,b盘顺时针转动
D.若B1、B2反向,b盘顺时针转动
|
( )
A.物体与地面间的动摩擦因数
B.推力F在0~4s内的冲量
C.物体在0~4s内的位移
D.物体在0~4s内的动能变化量
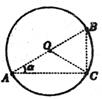
21.如图所示,在匀强电场中有一半径为R的圆O,场强方向与圆O所在平面平行,场强大小为E,电荷量为q的带正电的微粒以相同的初动能沿着各个方向从A点进入圆形区域中,只在电场力作用下运动,从圆周上不同点离开圆形区域,其中从C点离开圆形区域的带电微粒的动能最大,图中O是圆心,AB是圆的直径,AC是与AB成α角的弦,则
( )
|
B.匀强电场的方向沿OC方向
C.从A到C电场力做功为2qER![]()
D.从A到C电场力做功为2qER![]()
第Ⅱ卷 (共10大题,共174分)
|
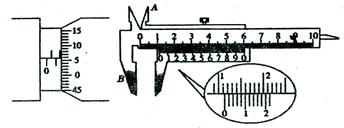
(1)①用螺旋测微器测一金属丝的直径,示数如图所示,由图可读出金属丝的直径为_________________mm。
|
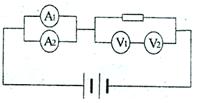
(2)如图所示,四个相同的电流表分别改装成两个安培表和两个伏特表。安培表A1的量程大于A2的量程,伏特表V1的量程大于V2的量程,把它们按图入电路,则
|
①安培表A1的读数___________安培表A2的读数
②安培表A1的偏转角__________安培表A2的偏转角
③伏特表V1的读数_____________伏特表V2的读数
④伏特表V1的偏转角_____________伏特表V2的偏转角
(填“大于”“小于”或“等于”)
|
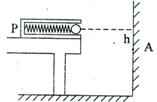
复再次弹射是让P可以在桌面上自由滑动,则同一
小球从同一位置谈射出后,将击中A点正_______方
的B点(填“上”或“下”),已知弹射器P的质量
为M,两次弹射时压缩弹簧的弹性势能相等,则A
和B之间的距离![]() ___________
___________
23.(12分)已知地球半径R,一只静止在赤道上空的热气球(不计气球离地面高度)绕地心运动的角度为![]() ,在距地面h高处圆形轨道上有一颗人造卫星。设地球质量为M,热气球的质量为m,人造卫星的质量为m1,根据上述条件,有一位同学列出以一下两个式子:
,在距地面h高处圆形轨道上有一颗人造卫星。设地球质量为M,热气球的质量为m,人造卫星的质量为m1,根据上述条件,有一位同学列出以一下两个式子:
对热气球有:![]() 。。。。。。。。。。。。。。。。。。。。。。。。。。。1
。。。。。。。。。。。。。。。。。。。。。。。。。。。1
对人造卫星有:![]() 。。。。。。。。。。。。。。。。。。。。2
。。。。。。。。。。。。。。。。。。。。2
进而求出了人造地球卫星绕地球运行的角速度![]() 。该同学的解法中有一个公式是错误的。请指出错误的是哪一个,然后你自己针对该错误解法重新补充一个条件,再求出
。该同学的解法中有一个公式是错误的。请指出错误的是哪一个,然后你自己针对该错误解法重新补充一个条件,再求出![]() 。
。
|
(1)0―1.0×10-2s时间内,
通过电阻R的电荷量;
(2)1min内电流通过电阻
R产生的热量;
(3)线圈中所产生的感应电流的有效值。
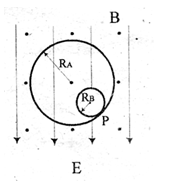
25.(21分)如图所示,空间存在着正交匀强电磁场,电场方向竖直向下,场强为E,磁场方向水平向外,磁感应强度为B,两个带电小球A和B,都能在面内做匀速圆周远动(两球间的库仑力可以忽略)运动轨迹如图,已知两带电小球质量关系为mA=3mB,轨迹半径为RA=3RB=9cm
(1)说明小球A和B带什么电性?求出它们所带电量之比
(2)指出A,B绕行方向?求出它们绕行速率之比?
(3)设球A和球B在图位置P处相碰,碰后原先在小圆轨迹上运动的B恰好能沿大圆的轨迹运动,求A球碰后圆运动的半径?(碰撞时两球间电荷量不发生转移 )
 |
26.(12分)A、B、C、D、E是原子序数依次增大的短周期主族元素,且互不同族;其中只有两种为金属;A原子的 最外层电子数与次外层电子数相等;A与E、B与D这两对原子的最外层电子数之和均为i9.五种元素的单质在一定条件下都可与NaOH溶液反应,C元素在地壳中的含量占第二位。请回答下列问题:
(1)B、D、E的原子半径由小到大的顺序是_______________(用元素符号表示)
(2)DE2的电子式是______________,它在常温下呈液态,形成晶体时,属于___________晶体。
(3)A与B化学性质相似,则A与浓的NaOH溶液反应的化学方程式是:_____________。
(4)硅酸盐工业用C的氧化物在玻璃窑中的两个主要反应方程式:____________。
27.请按要求填空:(18分)
(1)下列操作正确的是_________、___________。(填编号)
A.将未经湿润的pH试纸浸到某溶液中,之后取出与标准比色卡比较,测得该溶液pH
B.制备时Fe(OH)2,将盛NaOH(aq)的滴管伸入到试管内FeSO4(aq)的液面下
C.焰色反应操作是:将铂丝放在稀盐酸中洗涤,然后直接蘸取待检物置于酒精灯或煤气灯的火焰上灼烧,观察火焰的颜色
D.中和滴定中,锥形瓶用蒸馏水洗净后未干燥直接往其中注入一定量的待测溶液
E.各放一张质量相同的滤纸于天平的托盘上,将NaOH固体放在左盘纸上称量
F.配置0.1mol-1L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释
G.用盐酸析法去淀粉溶液中混有的NaCl杂质
|
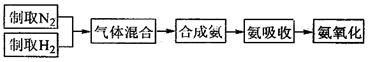
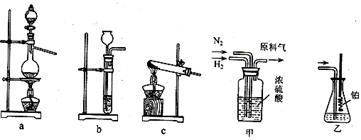
|
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
①从图中选择制取气体的适合装置:氮气_____________、氢气_____________。
②氮气和氢气通过甲装置,甲装置的作用除了将气体干燥外,还有___________ _
__________________的作用。
![]() ③用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
,锥形瓶中还可观察到红棕色气体和白烟产生。
③用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是:
,锥形瓶中还可观察到红棕色气体和白烟产生。
④写出乙装置中氨氧化的化学方程式:_________________________。
⑤反应结束后锥形瓶内的溶液中含有H+、OH-、__________、__________离子
28.(14分)乙烯和乙烷混合气体共a mol,与b mol,的氧气共存于一密闭的容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45水。试求:
(1)CO和CO2混合气体的物质的量=________,生成的水的物质的量=_________。
(2)当=1时,乙烯和乙烷的物质的量之比n(乙烯)n(乙烷)=_______________。
(3)当=1时,且反应后CO和CO2混合气体的物质的量为反应前氧的2/3时,则b=
;得到的CO和CO2的物质的量之比n(CO) : n(CO2)=_________________.
(4)的取值范围是_________________;的取值范围是________________
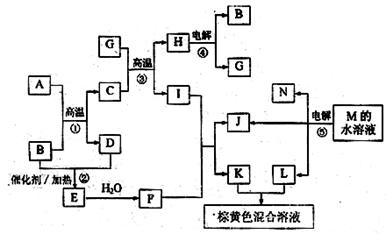
29.(16分)根据反应框图填空,已知反应1~5均为工业生产及应用中常见反应,其中B、G、I、J、L均为常见单质,其中B、J、L为气体,C为红棕色粉末状固体。
|
(1)写出A、B的化学方程式A ______________;B______________。
(2)写出下列化学反应方程式
反应③的化学方程式___________________________________。
反应⑤的离子方程式___________________________________。
(3)工业生产中,由E转化F的反应是在(设备)中进行的,并常用________________
来吸收E,优点是__________________________
(4)写出K与L反应的离子方程式___________________________
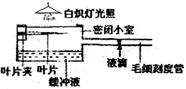
30.(16分)某同学利用下列装置研究CO2含量以及光照强度对某种绿叶光合作用的综合影响。实验过程用同种、状况相同的若干新鲜叶片在室温25℃下进行,通过缓冲液调节密闭小室空间CO2浓度的相对恒定。对相应装置精确测量的结果如下表。请分析回答:
|
| 组 别 | 实验条件 | 液滴移动mL/h | |||||||||
| 光强(Lx) | CO2(%) | |||||||||||
| 1 | 800 | 0.03 | 右移6.0 | |||||||||
| 2 | 1000 | 0.03 | 右移9.0 | |||||||||
| 3 | 1000 | 0.05 | 右移11.2 | |||||||||
| 4 | 1500 | 0.05 | 右移11.2 | |||||||||
| 5 | 1500 | 0.03 | 右移9.0 | |||||||||
(1)第3组装置中液滴右移的生理原因是 。该装置2h内,缓冲液释放到密闭小室空间的CO2约为 mg。第3、4两组的结果相同,限制4装置光合作用的非生物因素主要是 。
(2)装置虽均置于25℃环境下,但有同学认为液滴移动的量不一定真正代表光合作用释放O2的量,因为光照引起的 会导致密闭小室内气体的物理性膨胀。
(3)某同学认为本实验不能令人信服地说明光照强度和CO2浓度的相互作用,使光合作用进一步增强。该同学又增设了一组实验,请写出该同学增设的这组实验的条件组合 。
(4)请您利用该装置研究叶片有氧呼吸强度随时间而变化的趋势。
A.方法步骤:①用同种、状况相同的新鲜叶片和相应的死叶片分别完成题中装置(各三套),置于温度相同的暗室中;②每隔一定时间, ;
③
B.预期结果:液滴向 移,且速率惭慢,直至不再移动。
|
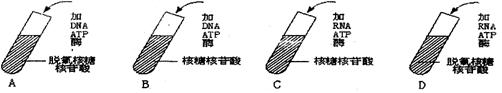
(1)A、D两试管内的产物是 ,你认为A试管模拟的是 过程,D试管模拟的是 过程。
(2)B、C两试管的产物都是 ,但B试管模拟的是 过程,C试管模拟的是 过程。
(3)若B试管内加入的DNA是一段360个碱基对的基因,则B的产物中最多含有
个碱基,有 个密码子。
(4)1978年美国科学家利用工程技术,将人类胰岛素基因拼接到大肠杆菌的DNA分子中,然后通过大杨杆菌的繁殖,生产出了人类胰岛素。请回答:
①上述人类胰岛素的合成是在 处进行的,其决定氨基酸
排列顺序的mRNA的模板是由 基因转录而来的。
②合成的该胰岛素含51个氨基酸,有两条肽链组成,那么决定它的合成的基因中至少应含有碱基 个;若核苷酸的平均相对分子质量为300,则与胰岛素分子对应的mRNA的相对分子质量为 ;若氨基酸的平均相对分子质量为90,该胰岛素的相对分子质量约为 。
参考答案
生物部分
|
30.(1)光合作用产生的O2大于呼吸作用消耗的O2 44 CO2
(2)温度变化(升高) (3)光强为800Lx,CO2浓度为0.05%
(4)A ②观测毛细刻度管液滴移动的量,取相同处理结果的平均值;
③记录结果 B 左
31.(1)DNA DNA的复制 逆转录 (2)RNA 转录 RNA的复制
(3)360 120 (4)①大肠杆菌的核糖体 人类胰岛素 ②306 43164 3708
化学部分
6.D 7.D 8.A 9.D 10.C 11.D 12.C 13.B
 26.(1)Cl<S<Al (用元素符号表示)
26.(1)Cl<S<Al (用元素符号表示)
(2): Cl : S : Cl : 分子
|
|
SiO2+CaCO3 CaSiO3+CO2↑
27.(1)B D (2)①a;b。②调整氮气和氢气达到最佳混合比;
|
④4NH3+5O2 4NO+6H2O ⑤NH4+ NO3―
28.(1)2a mol 2.5mol (2)1:1 (3)3 1:3
(4)5/6<a<5/4 25/12<b<15/4
29.(1)FeS2 O2
|
|
2NaCl+2H2O 2NaOH+H2↑+Cl2↑
(3)吸收塔;98.3%的浓硫酸;不能产生酸雾,吸收效率高。
(4)2Fe2++Cl2=2Fe3++2Cl―
物理部分
一、选择题(48分)
14.D 15.BC 16.A 17.ABD 18.C 19.D 20.BC 21.BD
二、实验题(18分)
22.Ⅰ.(1)1.556―1.558mm (2)A 11.08~11.10MM
Ⅱ.大于 等于 大于 等于
Ⅲ.下 ![]()
三、计算题:
23.(12分)解:第一个等式不正确
解1:补充地面附近重力加速度g。 有 ![]() …………①
…………①
与 ![]() …………② 联立
…………② 联立
解得:![]()
解2:补充第一宇宙速度V1, 有![]() 与②式联立可得
与②式联立可得
解得: 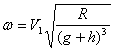
解3:补充同步卫星离地面的高度H。有![]() 与②式联立
与②式联立
解得: 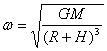
24.(21分)(1)在0~1.0×10―2s内感应电动势 ![]()
通过电阻R的电流 ![]()
所以通过R的电量 ![]()
(2)一个周期内电阻R产生热量 ![]()
在1min内电阻R产生热量 ![]()
(3)设感应电流有效值为I。在一个周期内,
![]()
![]()
解得 ![]()
25.(21分)(1)带负电 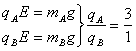
(2)逆时针: 据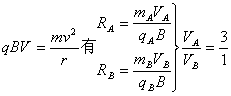
(3)分析是A追撞B
由动量守恒定律有:![]()
据:![]()
得出:![]()
已知:![]()
解得:![]()