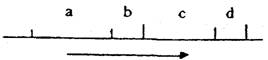高考成都名师联盟模拟试卷(理科综合)
可能用到的相对原子质量:
H 1 He 4 C 12 N 14 O 16 Na 23 Si 28 K 39 Cl 35.5 Ba 137
一 选择题(共126分 6分/小题)
1.碱基互补配对不发生在
A.细胞膜上 B.线粒体内 C.叶绿体内 D.核糖体上
2.下列中全部都正确的一组是
| 生物种类 | 细胞结构 | 核苷酸种类 | 代谢类型 | 生殖方式 | 变异来源 |
| A.艾滋病病毒 | 无 | 8 | 异养、需氧 | 自我复制 | 基因突变 |
| B.青霉菌 | 原核细胞 | 8 | 异养、需氧 | 孢子生殖 | 基因突变 |
| C.变形虫 | 原生生物 | 4 | 异养、需氧 | 分裂生殖 | 基因突变 基因重组 染色体变异 |
| D.小麦 | 真核生物 | 8 | 自养、需氧 | 卵式生镇 | 基因突变 基因重组 染色体变异 |
3.连续分裂的细胞,相邻的两个细胞周期可表示为下图,下列叙述正确的是
|
①a+b为一个细胞周期
②c、d两段都要消耗ATP
③b段的主要变化是DNA的复制及有关蛋白质的合成
④d段主要完成遗传物的平均分配
⑤若该细胞为植物细胞,则在b段最初时期高尔基本体活动增强
A.①②④ B.③④⑤ C.②④⑤ D.①③⑤
4.下面是几个放射性同位素示踪实验,对其结果的叙述不正确的是
A.小白鼠吸入18O2较长时间后呼出的二氧化碳不含C18O2,但尿中的水含H218O
B.在含葡萄糖(C6H12O6)和乳糖(14C12H22O11)的培养液中培养大肠杆菌,要过一段
时间后才会出现含14C的细菌细胞
C.用被32P标记的T2噬菌体去感染未被标记的细胞,经过短时间的保温后,在细胞内
能检测到放射性
![]() D.用含15N标记的胸腺嘧啶脱氧核苷酸的营养液培养根尖分生区细胞,一段时间后分离获得具有放性的细胞器,可在这类细胞器内进行的生理过程有[H]+O2 H2O
D.用含15N标记的胸腺嘧啶脱氧核苷酸的营养液培养根尖分生区细胞,一段时间后分离获得具有放性的细胞器,可在这类细胞器内进行的生理过程有[H]+O2 H2O
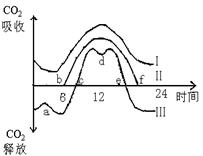 5.右图表示一农田中一昼夜温度变化I、光照强度变化Ⅱ、植物吸收CO2的变化Ⅲ的数量关系。下列不正确的叙述是
5.右图表示一农田中一昼夜温度变化I、光照强度变化Ⅱ、植物吸收CO2的变化Ⅲ的数量关系。下列不正确的叙述是
A.Ⅲ与时间轴交点c、e顶示光合作用吸收的CO2等于呼吸作用释放的CO2
B.a点的数值变化主要与夜间低温有关
C.植物从c点开始合成有机物,至e点有机物合成停止
D.增大曲线Ⅲ与时间轴围成的正面积的措施包括提高光照强度、提高CO2浓度、适宜的温度和充足的水分供应等
6.下列实验能够成功的是( )
A.只用溴水一种试剂可鉴别甲苯、乙烯、乙醇、四氯化碳四种液体
B.将乙醇加热到170℃可制得乙烯
C.用乙醇、冰醋酸及pH=0的H2SO4加热可制乙酸乙酯
D.用饱和的Na2CO3溶液除去CO2中的HCl
7.NA为阿伏加德罗常数,下列叙述正确的是( )
A.80g硝酸铵含有氮原子数为2NA
B.1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA
C.标准状况下,11.2L四氯化碳所含分子数为0.5 NA
D.在铜与硫的反应中,1mol铜失去的电子数为2 NA
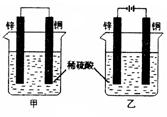 8. 将纯锌片和纯铜片按右图所示方式插入同浓度的稀H2S04
中一段时间,以下叙述正确的是:
8. 将纯锌片和纯铜片按右图所示方式插入同浓度的稀H2S04
中一段时间,以下叙述正确的是:
A.两烧杯中铜片均有气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的PH 均增大
D.甲中的锌比乙中的锌腐蚀慢
![]()
![]() 9.据最新报道,科学家发现了如下反应:
,已知
为离子化合物(中Pt 为+5 价),对于此反应,下列说法正确的是
9.据最新报道,科学家发现了如下反应:
,已知
为离子化合物(中Pt 为+5 价),对于此反应,下列说法正确的是
A.在02(PtF6 )中不存在共价键
B.在此反应中,O2是氧化剂,PtF6 是还原剂
C.在此反应中,每生成lmol 02(PtF6)则转移lmol 电子
D.由02(PtF6)形成的晶体为分子晶体
10.下列各组数据关系中,前者比后者大的是
A.常温常压下,pH=10的KOH溶液和pH=10的KCN溶液中,由水电离的OH-浓度。
B.纯水在1000C和200C时pH。
C.250C,浓度相同的苯酚钠溶液与CH3CH2ONa溶液的pH。
D.100mL0.1mol/L醋酸溶液与10mL1mol/L醋酸溶液中H+的数目。
11.已知A、B是第一周期以外的短周期元素,它们可以形成离子化合物AmBn。在此化合物中,所有离子均能形成稀有气体原子的稳定结构。若A的核电荷数为![]() ,则B的核电荷数不可能是( )
,则B的核电荷数不可能是( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
12.对复杂的有机物结构可用“键线式”表示。如苯丙烯酸1-丙烯酯:
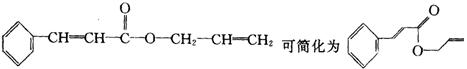 |
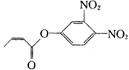 杀虫剂“阿乐丹”的结构表示如右式:若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是
杀虫剂“阿乐丹”的结构表示如右式:若它在稀酸作用下能发生水解反应生成两种有机物,则此两种有机物具有的共同性质是
A.遇FeCl3溶液均显紫色 B.均能发生银镜反应
C.均能与溴水发生加成反应 D.均能与NaOH溶液发生反应
13.将pH=1的稀硫酸慢慢加入―定量的BaCl2的溶液中,恰好使Ba2+沉淀完全,此时溶液的体积为100mL(混合时溶液体积的变化忽略不计),且混合溶液的pH=2,则原BaCl2溶液中Cl-的浓度为( )
A.0.011mol/L B.0.22mol/L C.0.022mol/L D.0.11mol/L
二、选择题(本题共8小题,每小题6分,共48分.在每小题给出的四个选项中,有的小题只有一个选项正确,有的小题有多个选项正确.全部选对的得6分,选不全的得3分,有选错的或不答的得0分)
14.一位质量为m的运动员从下蹲状态向上起跳,经△t时间,身体伸直并刚好离开地面,速度为v. 在此过程中,下列说法正确的是
A.地面对他的冲量为mv+mg△t,地面对他做的功为![]()
B.地面对他的冲量为mv+mg△t,地面对他做的功为零
C.地面对他的冲量为mv,地面对他做的功为![]()
D.地面对他的冲量为mv-mg△t,地面对他做的功为零
15.如图所示,E为电池,L是电阻可忽略不计、自感系数足够大的线圈,D1、D2是两个规格相同的灯泡,S是控制电路的开关。对于这个电路,下列说法正确的是
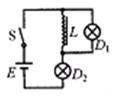 A.刚闭合S的瞬间,通过D1、D2的电流大小相等
A.刚闭合S的瞬间,通过D1、D2的电流大小相等
B.刚闭合S的瞬间,通过D1、D2的电流大小不等
C.闭合S待电路达到稳定后,D1熄灭,D2比S刚闭合时暗
D.闭合S待电路达到稳定后,再将S断开瞬间,D2不立即熄灭,D1立即熄灭
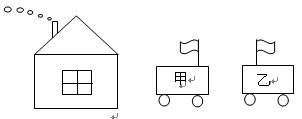 16.观察图中烟囱冒出的烟和车上的小旗,关于甲、乙两车相对于房子的运动情况,下列说法正确的是
16.观察图中烟囱冒出的烟和车上的小旗,关于甲、乙两车相对于房子的运动情况,下列说法正确的是
A.甲、乙两车一定向左运动
B.甲、乙两车一定向右运动
C.甲车可能运动,乙车向右运动
D.甲车可能静止,乙车向左运
17.一定质量的气体,由状态A变化到状态B,压强和体积均增大,忽略气体分子势能的变化,下列说法中正确的是
A.气体分子平均动能不变 B.气体分子平均动能减小
C.气体吸热 D.外界对气体做功
 18.如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,则
18.如图所示,小物体A沿高为h、倾角为θ的光滑斜面以初速度v0从顶端滑到底端,而相同的物体B以同样大小的初速度从同等高度处竖直上抛,则
A.两物体落地时速度相同
B.从开始至落地,重力对它们做功相同
C.两物体落地时重力的瞬时功率相同
D.从开始运动至落地过程中,重力对它们做功的平均功率相同
19.环型对撞机是研究高能粒子的重要装置,其核心部件是一个高真空的圆环状的空腔。若带电粒子初速可视为零,经电压为U的电场加速后,沿圆环切线方向注入对撞机的环状空腔内,空腔内存在着与圆环平面垂直的匀强磁场,磁感应强度大小为B。带电粒子将被局限在圆环状空腔内运动。要维持带电粒子在圆环内做半径确定的圆周运动,下列说法正确的是 A.对于给定的加速电压,带电粒子的比荷q/m越大,磁感应强度B越大
B.对于给定的加速电压,带电粒子的比荷q/m越大,磁感应强度B越小
C.对于给定的带电粒子,加速电压U越大,粒子运动的周期越大
D.对于给定的带电粒子,不管加速电压U多大,粒子运动的周期都不变
20.如图所示,沿![]() 方向的一条细绳上有
方向的一条细绳上有![]() 、
、![]() 、
、![]() 、
、![]() 四点,已知
四点,已知![]() ,质点在垂直于
,质点在垂直于![]() 轴的方向上做简谐运动,形成沿
轴的方向上做简谐运动,形成沿![]() 方向的横波。若
方向的横波。若![]() 时刻,
时刻,![]() 点从平衡位置开始向上运动,
点从平衡位置开始向上运动,![]() 时刻
时刻![]() 点第一次到达最大位移处,这时
点第一次到达最大位移处,这时![]() 点从平衡位置开始向上运动,由此可以判断,在
点从平衡位置开始向上运动,由此可以判断,在![]() 时刻,质点
时刻,质点![]() 和
和![]() 的运动情况是
的运动情况是
![]() A.
A.![]() 点位于
点位于![]() 轴上方
轴上方
B.![]() 点位于
点位于![]() 轴上方
轴上方
C.![]() 点正向下运动
点正向下运动
D.![]() 点正向上运动
点正向上运动
 21.如图所示,在水平方向的匀强电场中,绝缘细线的一端固定在O点,另一端系一带正电的小球在竖直平面内做圆周运动,小球所受的电场力大小等于重力大小,比较a、b、c 、d这四点,小球
21.如图所示,在水平方向的匀强电场中,绝缘细线的一端固定在O点,另一端系一带正电的小球在竖直平面内做圆周运动,小球所受的电场力大小等于重力大小,比较a、b、c 、d这四点,小球
A.在最高点a处动能较其他三点都小
B.在最低点c处重力势能最小
C.在水平直径右端b处机械能最大
D.在水平直径左端d处总能量最大
II卷 生物(2007.2.)
班级 学号 姓名
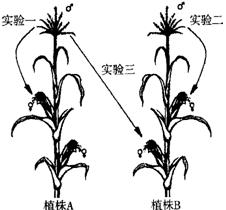 |
30.(21分)玉米是一种雌雄同株的植物,通常其顶部开雄花,下部开雌花。在一个育种实验中,选取A、B两棵植株进行了如图所示的三组实验:
实验一:将植株A的花粉传授到同一植株的雌花序上。
实验二:将植株B的花粉传授到同一植株的雌花序上。
实验三:将植株A的花粉传授到植株B的另一雌花序上。
上述三组实验,各雌花序发育成穗轴上的玉米粒的颜色数如下表所示:
| 实验 | 黄色玉米粒 | 白色玉米粒 |
| 一 | 587 | 196 |
| 二 | 0 | 823 |
| 三 | 412 | 386 |
请根据以上信息,回答下列问题:
(1)在玉米粒颜色这一对相对性状中,隐性性状是 ,判断的理由是
(2)如果用G代表显性基因,g代表隐性基因,则植株A的基因型为 。植株B的基因型为 ,实验一中,黄色玉米粒的基因型是 。
(3)如果植株A接受植株B的花粉,在植株A上,所结种子的种皮和胚乳细胞的基因型依次是: 、 。
31.(21分)探究在有限的养分中和不同的温度下酵母菌种群数量的动态变化。
材料用具:酵母菌母液、蒸馏水、无菌水、酵母膏、蛋白胨、葡萄糖、1mol/L硫酸溶液、烧杯、试管、滴管、量杯、漏斗、1mL刻度吸管、标签、玻璃棒、酒精灯、pH试纸、天平、计数板、恒温箱、显微镜、高压蒸汽灭菌锅等。
(一)探究思路:
(1)设计对照实验。为了探究培养液中酵母菌种数量的动态变化,某同学按下表完成了有关实验。
| 试管编号 | 培养液/mL | 无菌水/mL | 酵母菌母液/mL | 温度/℃ |
| A | 10 | ― | 0.1 | 28 |
| B | 10 | ― | 0.1 | 5 |
| C | ― | 10 | 0.1 | 28 |
(2)实验操作:
配制培养基→ →接种→ →计数→分析数据,得出结论。
(二)问题探讨:
①请写出该同学研究的课题名称: 。
②用显微镜定期测酵母菌数日,结果仅A管中第3天开始个体数日迅速增加,第5天开始A管中个体数目达到最大,实验至第6天结束。请将A、B、C三组预期结果的走势图绘制在坐标系中。
③培养的酵母菌种增长曲线是否呈“S”型?为什么?
。
④酵母菌增殖方式即可以是出芽方式又可以是有丝分裂。在酵母菌有丝分裂全过程中其基因是否都在表达? ;有丝分裂过程需要的蛋白质有很多种类,这些蛋白质是在 的直接指导下合成的。
高2007级2月月考理科综合―化学试题Ⅱ卷(60分)
班级__________姓名___________学号_______
可能用到的相对原子质量:
H 1 He 4 C 12 N 14 O 16 Na 23 Si 28 K 39 Cl 35.5 Ba 137
26.(15分)根据下列事实完成下列反应方程式:
(1)AsH3是一种很强的还原剂,室温下,它能在空气中自燃,其氧化产物为As2O3,写出反应的化学方程式
(2)NaNO3与氢碘酸反应,放出NO气体并有单质碘生成
(3)白磷在一定条件下可被HClO3的水溶液氧化,生成磷的最高价态化合物,而氯元素被还原为最低价态 ______________________________________
(4)砷为氮族元素,其氧化物As2O3俗称砒霜,有剧毒可用马氏试砷法来检验,其原理是:将锌、盐酸和食物试样混合,若含有砒霜,则会产生砷化氢气体,这一反应的离子方程式是
(5)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼和足量液态H2O2反应,生成氮气和水蒸气,放出256.65kJ的热量。
写出此反应的热化学方程式: 。
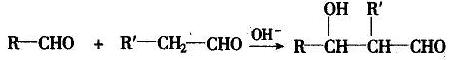 27. (12分)已知:
27. (12分)已知:
有机物G(C20H18O4)是一种酯,合成路线如下:
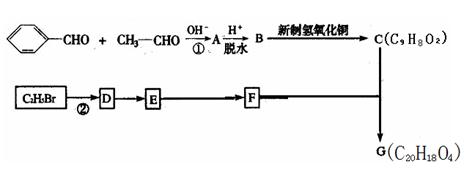 |
试回答下列问题:
(1)指出反应类型:反应①__________;反应②_________。
(2)A的结构简式是________________;F的结构简式是_______________。
(3)B转化为C的化学方程式是(有机物用结构简式表示):
________________________________________________________________________
(4)写出有机物C的所有同时含碳碳双键、苯环和羧基的同分异构体(不包括有机物C本身):
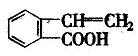 |
、 ______________、 _____________、 。
28.(13分)物质A~D相互关系如下图,其中A为酸式盐,B为某二价主族金属的碳化物,等物质的量A、B与适量水充分混合能恰好完全反应,常温常压下,C、D均为气态,反应④和反应⑤分别是工业上生产化合物J和化合物G的重要方法
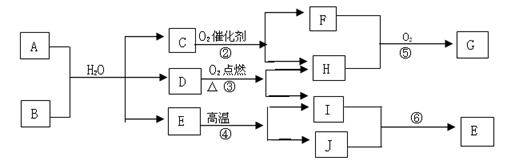 |
(1)C的电子式是 ,E的化学式是 ,G的化学式
(2)完成下列反应的化学方程式
B+H2O
C+O2
A溶液与过量NaOH溶液反应的离子方程式:
29.(20分)(I) 下图甲和乙是某学校王老师制备NH3 并进行性质实验时的改进装置。按图甲把仪器安装好,称取2g 固体氯化铵装入试管底部,再快速称取2g 氢氧化钠覆盖在氯化铵上方;立即用带有滴管的塞子塞紧(滴管预先吸入约2mL 浓氨水);烧杯内盛滴有酚酞试液的水:把浓氨水滴入试管里,可立即观察到试管内发生剧烈反应,有大量气泡.
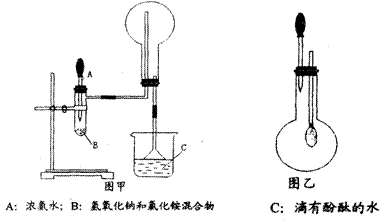 |
将上述中收满NH3 的圆底烧瓶取下,改装成图乙所示的装置,胶头滴管内事先预吸入2mLH2O ,此时小气球系在玻璃棒上呈自然松驰状态;将滴管内的水慢慢滴入烧瓶中,轻轻晃动烧瓶,通过观察实验现象便可以验证NH3 的某个性质。按要求回答下列问题:
(1)中学化学教材中是用与制O2相同的制备装置来加热制取NH3的,该化学方程式为:
___________________________________________________________________________
(2)下面是某同学关于王老师能用图甲制取NH3的原因分析,有道理的是__________。
①在NH3
・ H2O
中有平衡![]() 使平衡向左移动
使平衡向左移动
②在NH3・ H2O 中有平衡![]() 使平衡向左移动
使平衡向左移动
③Na0H 溶于水时放热,使体系的温度升高,NH3 的溶解度减小
④NH4Cl与NaOH 在此情况下可反应生成NH3,![]()
⑤NH4Cl 会分解释放出NH3
(3)图甲中的NH4Cl 与NaOH 固体混合物能否用CaO 固体代替 (填”能”与”不能”)
(4)如何判断图甲中烧瓶己收满NH3 ?_____________________________________________
(5)图乙中胶头滴管中的水挤入烧瓶后,观察到的现象是 它说明了NH3
 (Ⅱ)如图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL,则原混合气体中NO2和NO的物质的量之比为
(Ⅱ)如图所示:在B槽中装有500 mL水,容积为a mL的试管A充满了NO2和NO的混合气体(标准状况),将试管A倒插入B槽的水中。充分反应后,试管A中余下气体的体积为0.5a mL,则原混合气体中NO2和NO的物质的量之比为
通过导气管C往余下0.5a mL气体的试管A中持续通入氧气,A中可能观察到的现象是:______________________________
___________________________________________________
有关反应的化学方程式为:____________________________________________________________
当试管A中充满气体时停止通入氧气,然后将试管取出水槽,则共通入氧气的体积为 ________mL,水槽B中溶液的物质的量浓度为 mol・L-1(设溶液的体积仍为500 mL)
物 理 Ⅱ 卷(2007.2.26)
班级 学号 姓名
22.实验题(18分)
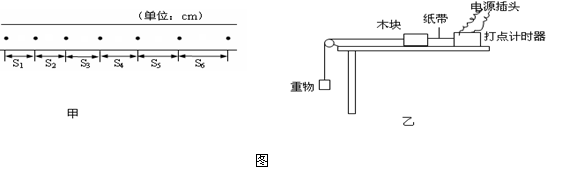
(Ⅰ).(8分)在探究加速度与物体质量、物体受力的关系实验中,实验装置如图乙所示:一木块放在水平光滑长木板上,左侧拴有一不可伸长的细软线,跨过固定在木板边缘的滑轮与一重物相连,重物的质量为m .木块右侧与穿过打点计时器的纸带相连,在重物牵引下,木块在木板上向左做匀加速运动.图甲给出了打点计时器在纸带上打出的一些连续的点,它们之间的距离分别为S1、S2、S3、S4、S5、S6,打点计时器所用交流电周期为T. 根据给以上数据求:
(1)木块加速度的表达式是 a= .
(2)细线对木块拉力的表达式是T= .
 |
(Ⅱ).(10分)测量一个电阻Rx阻值(约为70Ω),给你如下器材:
A.电流表(50mA,内阻约10Ω)
 B.电压表(0-3V-15V 内阻分别是3kΩ和15kΩ)
B.电压表(0-3V-15V 内阻分别是3kΩ和15kΩ)
C.电源(1.5V干电池2节)
D.滑动变阻器R1(0―10Ω)
E.滑动变阻器R2(0―1kΩ)
F.电键、导线若干
(1)根据所给定的器材和实验要求,在方框中画出实验电路图
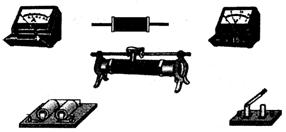
(2)实验中电压表选择 量程,滑动变阻器选择 .
(3)根据电路图和选择的仪器连接好下面的实物线路图。
23.(16分)为了安全.在公路上行驶的汽车之间应保持必要的距离。我国公安部门规定:高速公路上行驶汽车的安全距离为200m,汽车行驶的最高速度为120km/h。g=9.8m/s2,请你根据下面提供的资料.说明计算安全距离为200m的依据。
资料一:驾驶员的反应时间:0.3s-0.6s之间
资科二:各种路面与轮胎之间的动摩擦因数:
| 路面 | 动摩擦因数 |
| 干沥青与混凝土路面 | 0.7-0.8 |
| 干碎石路面 | 0.6-0.7 |
| 湿沥青与混凝土路面 | 0.32-0.4 |
24.(18分) 如图甲所示,光滑且足够长的金属导轨MN、PQ平行地固定的同一水平面上,两导轨间距L=0.20m,两导轨的左端之间所接受的电阻R=0.40
如图甲所示,光滑且足够长的金属导轨MN、PQ平行地固定的同一水平面上,两导轨间距L=0.20m,两导轨的左端之间所接受的电阻R=0.40![]() ,导轨上停放一质量m=0.10kg的金属杆ab,位于两导轨之间的金属杆的电阻r=0.10
,导轨上停放一质量m=0.10kg的金属杆ab,位于两导轨之间的金属杆的电阻r=0.10![]() ,导轨的电阻可忽略不计。整个装置处于磁感应强度B=0.50T的匀强磁场中,磁场方向竖直向下。现用一水平外力F水平向右拉金属杆,使之由静止开始运动,在整个运动过程中金属杆始终与导轨垂直并接触良好,若理想电压表的示数U随时间t变化的关系如图乙所示。求金属杆开始运动经t=5.0s时,
,导轨的电阻可忽略不计。整个装置处于磁感应强度B=0.50T的匀强磁场中,磁场方向竖直向下。现用一水平外力F水平向右拉金属杆,使之由静止开始运动,在整个运动过程中金属杆始终与导轨垂直并接触良好,若理想电压表的示数U随时间t变化的关系如图乙所示。求金属杆开始运动经t=5.0s时,
(1)通过金属杆的感应电流的大小和方向;
(2)金属杆的速度大小;
(3)外力F的瞬时功率。
25.(20分)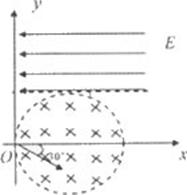 如图所示,真空中有(
如图所示,真空中有(![]() ,0)为圆心,半径为
,0)为圆心,半径为![]() 的圆柱形匀强磁场区域,磁场的磁感应强度大小为B,方向垂直于纸面向里,在
的圆柱形匀强磁场区域,磁场的磁感应强度大小为B,方向垂直于纸面向里,在![]() 的虚线上方足够大的范围内,有方向水平向左的匀强电场,电场强度的大小为
的虚线上方足够大的范围内,有方向水平向左的匀强电场,电场强度的大小为![]() ,从
,从![]() 点向不同方向发射速率相同的质子,质子的运动轨迹均在纸面内,设质子在磁场中的偏转半径也为
点向不同方向发射速率相同的质子,质子的运动轨迹均在纸面内,设质子在磁场中的偏转半径也为![]() ,已知质子的电量为
,已知质子的电量为![]() ,质量为
,质量为![]() ,不计重力及阻力的作用,求
,不计重力及阻力的作用,求
(1)质子射入磁场时的速度大小
(2)速度方向沿![]() 轴正方向射入磁场的质子,到达
轴正方向射入磁场的质子,到达![]() 轴所需的时间
轴所需的时间
(3)速度方向与![]() 轴正方向成
轴正方向成![]() 角(如图中所示)射入磁场的质子,到达
角(如图中所示)射入磁场的质子,到达![]() 轴的位置坐标。
轴的位置坐标。
成都石室中学高2007级理科综合测试 (2007.2.26)
理科综合―生物答案:
1-5ADAAC
30.(每空3分,共21分)(1)白粒 由实验一可知,植株A自交,后代出现性状分离,且黄粒:白粒=3:1(或植株A自交,后代出现性状分离) (2)Gg gg GG和Gg(缺一不得分)(3)Gg GGg或ggg(缺一不得分)
31.(每空3分,共21分)(一)(2)灭菌 培养
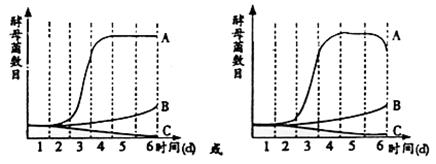 |
(二) ①温度和营养物质以对酵母菌生长的影响
②
![]() ③否,应该是
型,最后阶段是衰亡期 ④否mRNA
③否,应该是
型,最后阶段是衰亡期 ④否mRNA
化学参考答案及评分标准
6. B 7. C 8. D 9. D 10. A 11. B 12. A 13. C
26.(13分)(1)分子(2分) O2(2分)
(2)加热 (3分)
(3)![]() ==CO2↑+H2O(3分)
==CO2↑+H2O(3分)
SO2+Cl2+2H2O==
4H++![]() +2Cl-(3分)
+2Cl-(3分)
27.(18分)(1)分液漏斗的活塞未关闭(2分)
(2)无(1分) 此时硫酸的质量分数为23%,小于60%,其氧化性弱,所以无明显现象(2分)
铜粉上产生气泡(1分),溶液渐成蓝色(1分) B管中品红褪色(1分)
(3)①2H2SO4(浓)+C![]() CO2↑+2SO2↑+2H2O(2分)
CO2↑+2SO2↑+2H2O(2分)
②无水硫酸铜(1分) 检验H2O(1分)
品红溶液(1分) 检验SO2(1分)
足量酸性KMnO4溶液(1分,其它合理答案也给分) 除尽SO2(1分)
澄清石灰水(1分) 检验CO2(1分)
28.(13分)(1)碳碳双键、羧基(2分) (2)②③(2分)
![]()
(3)HCOOH+CH3OH HCOOCH3+H2O(3分)
![]() (4)CH3OH(1)+
(4)CH3OH(1)+![]() O2(g)
CO2(g)+2H2O(1);ΔH=-726.4kJ・mol-1(3分)
O2(g)
CO2(g)+2H2O(1);ΔH=-726.4kJ・mol-1(3分)
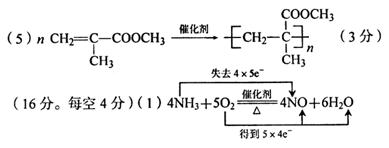
(2)3NOx+2xNH3 ![]()
![]() N2+3xH2O (3) ≥1 12.5%(提示:只需用O2将多余NO的一半氧化为NO2,即可按题给的后一反应全部被NaOH溶液吸收)
N2+3xH2O (3) ≥1 12.5%(提示:只需用O2将多余NO的一半氧化为NO2,即可按题给的后一反应全部被NaOH溶液吸收)
理科综合―化学试题参考答案
6.A 7.A 8.C 9.C 10.D 11.B 12.D 13.A
26.(15分)每小题3分
(1) 2AsH3+3O2= As2O3+3H2O (2)2NaNO3+8HI=2NO+3I2+2NaI+4H2O
(3)3P4+10 HClO3 +18H2O=12H3PO4+10HCl (4)6Zn+As2O3+12H+=6Zn2++2AsH3↑+3H2O
(5)N2H4(l)+2 H2O 2(l)= N2(g) + 4H2O(g); △H= -641.625 kJ.mol-1
27. (12分)
(1)加成反应 消去反应 (各1分)
(2)C6H5-CH(OH)CH2CHO HOCH2CH2OH(各2分)
![]() (3)C6H5-CH=CHCHO+2Cu(OH)2
Cu2O↓+2H2O+C6H5-CH=CHCOOH (3分)
(3)C6H5-CH=CHCHO+2Cu(OH)2
Cu2O↓+2H2O+C6H5-CH=CHCOOH (3分)
 |
(4)
(各1分)
28.(13分)
![]() (1) (2分) CaCO3 HNO3 (各1分)
(1) (2分) CaCO3 HNO3 (各1分)
(2)CaC2+2H2O=Ca(OH)2+C2H2↑ 4NH3+5O2 4NO+6H2O (各3分)
(3)NH4++HCO3-+2OH-=NH3.H2O+H2O+CO32(3分)
![]() 29. (20分)
29. (20分)
(Ⅰ)(1) (2分)
(2)①②③④ (2分) (3)能 (1分) (4) 烧杯内的溶液变红(1分)
(5)气球逐渐变大(1分);极易溶于水(1分)
(Ⅱ)(1)3:1 (2分)
(2)无色气体变为红棕色气体(1分),试管中液面不断上升至全充满(1分),继续通入氧气后,试管中液面下降(1分),最后充满无色气体(1分)。[2NO+O2=2NO2(1分) 3NO2+H2O=2HNO3+NO (1分)]或 4NO+3O2+2H2O=4HNO3 (2分)(3)1.375a (2分) a/11200(2分)
理科综合―物 理 答 案
14.B 15.A 16.D 17.C 18.B 19.B 20.BC 21.BC
22.实验题(18分)(Ⅰ).(8分)
(1)![]() (4分,不用逐差法表示3分)
(4分,不用逐差法表示3分)
(2)![]() (4分)
(4分)
[说明:若(1)中加速度不用逐差法表示,而(2)中用了(1)的结果,则(2)不扣分]
(Ⅱ).(10分)
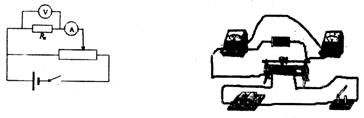 (1)图 (3分)
(1)图 (3分)
(2) 0-3V(2分)
Rl(2分)
(3) (3分)
23.(16分) 解:(1)0.6s。最长的反应时间,对应杀车之前最大可能运动距离。(4分)
(2)0.32最小的动摩擦因数,对应最大的可能运动距离。(4分)
(3)s=vt+![]() (6分)
(6分)
s=197.2m≈200m,因此200m的安全距离是必要的。(2分)
24.(18分)解:(1)由图象可知,![]() ………………………(1分)
………………………(1分)
此时电路中的电流(即通过金属杆的电流)![]() (2分)
(2分)
用右手定则判断出,此时电流的方向由b指向a…………………………(1分)
(2)金属杆产生的感应电动势![]() …………………………(3分)
…………………………(3分)
因![]() ……(3分)
……(3分)
(3)金属杆速度为v时,电压表的示数应为 ![]() (2分)
(2分)
由图象可知,U与t成正比,由于R、r、B及L均与不变量,所以v与t成正比,即金属杆应沿水平方向向右做初速度为零的匀加速直线运动…………………(1分)
金属杆运动的加速度![]() (2分)
(2分)
根据牛顿第二定律,在5.0s末时对金属杆有F―BIL=ma,解得F=0.20N……(2分)
此时F的瞬时功率P=Fv=1.0W…………………………(1分)
25.(20分)解:
(1)质子射入磁场后做匀速圆周运动,有
evB=mv2/r,可得v=eBr/m (2分)
(2)质子沿x轴正向射入磁场后经1/4圆弧后以速度v垂直于电场方向进入电场,
![]()
![]() (2分)
(2分)
在磁场中运动的时间t1=T/4=πm/2eB (2分)
进入电场后做抛物线运动,沿电场方向运动r后到达y轴,因此有
t2=![]() (2分)
(2分)
所求时间为t= t1+
t2= ![]() (2分)
(2分)
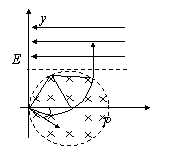 (3)质子在磁场中转过120°角后从P点垂直电场线进入电场,如图所示
(3)质子在磁场中转过120°角后从P点垂直电场线进入电场,如图所示
P点距y轴的距离x1=r+rsin30°=1.5r (2分)
因此可得质子到达y轴所需时间为
![]() (2分)
(2分)
t2=![]() (2分)
(2分)
在y方向质子做匀速直线运动,因此有
y’=vt2=![]() (2分)
(2分)
质子到达y轴的位置坐标为(0,r+![]() ) (2分)
) (2分)