天津一中高三理科综合能力测试第一套
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。第I卷1至8页,第II卷9至16页,共16页。满分300分。考试时间150分钟。
第I卷(选择题共132分)
本卷共22题,每题6分,共132分。在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5
1.反应式ADP+Pi+能量 ATP是在所有生活细胞中均发生的反应,下列与反应式中“能量”相关的叙述正确的是 ( )
A.向右反应需要的能量可以来自细胞内蛋白质水解为氨基酸的过程
B.向右反应需要的能量可以来自乳酸的氧化分解
C.向左反应产生的能量可以用于叶绿体中H2O的分解或CO2的固定
D.向左反应产生的能量可以用于人体肺泡内的气体交换过程
2.北京地区种植的大白菜于秋末冬初收获(在立冬日砍收白菜)。人们发现,收获的大白菜外部叶片的钙元素含量大大高于菜心,菜心的氮元素含量却远远高于外部叶片,而肥沃的菜园土富含各种矿质营养。对此现象可能合理的解释是 ( )
A.大白菜生长后期的气温偏低
B.北方的土壤氮元素含量比钙元素多
C.钙在植物体内可被不同器官重复利用
D.氮在植物体内形成的化合物比较稳定
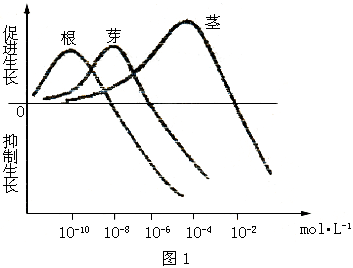
3.经实验检测出某一植株的不同器官对不同生长素浓度的反应如图1所示,横坐标表示生长素物质的量浓度。根据实验结果,可以获得的结论之一是 ( )
A.当生长素浓度为10-9mol・L-1时,抑制根的生长,促进芽的生长
B.若解除顶端优势,应确保侧芽的生长素浓度低于10-6 mol・L-1
C.低浓度生长素促进根、芽的生长,高浓度生长素则促进茎的生长
D.根向地生长的原因是其背地侧生长素浓度高于10-8 mol・L-1
 |
4.用纯种的黑色长毛狗与白色短毛狗杂交,F1全是黑色短毛。F1代的雌雄个体相互交配,F2的表现如下表所示。据此可判断控制这两对相对性状的两对基因位于 ( )
|
| 黑色短毛 | 黑色长毛 | 白色短毛 | 白色长毛 |
| ♀ | 42 | 19 | 14 | 6 |
| ♂ | 47 | 12 | 15 | 5 |
A.一对同源染色体上
B.一对姐妹染色单体上
C.两对常染色体上
D.一对常染色体和X染色体上
5.某国家妇女的生育年龄大都在20~35岁,如果这个年龄段的人口增长得比35岁以上年龄段慢,且每位妇女生育孩子的数目长期保持现在的水平,那么该国家的人口将( )
A.出生率不变,人口数量基本稳定
B.出生率下降,人口数量下降
C.出生率不变,人口数量下降
D.出生率下降,但人口数量基本稳定
6.大雪过后,融雪剂成为清除道路积雪的有力武器。过去使用的融雪剂以氯化钠等无机盐为主要成分,如向100g冰或雪中加入33g氯化钠可以使冰点降低到-21.20C,但它对路面和桥梁中钢筋的腐蚀作用相当强,对植物也会产生相当大的危害。现在所用的环保型融雪剂则大量使用有机盐和缓蚀剂,有的还添加了尿素,但它的融雪原理与以前相同。则下列说法不正确的是 ( )
A.环保型融雪剂的融雪原理为盐溶于水后,使冰点降低
B.使用环保型融雪剂可以减缓对路面和桥梁中钢筋的腐蚀
C.使用环保型融雪剂可以减少对植物的危害
D.使用环保型融雪剂主要是给植物补充养分
7.下列各组离子在溶液中能够大量共存的是 ( )
A.Mg2+、NH4+、OH-、HCO3-
B.K+、Fe3+、Cl-、SO42-
C.Al3+、H+、S2-、SiO32-
D.Fe2+、H+、Na+、NO3-
8.白磷在高压下隔绝空气加热后急速冷却,可得钢灰色固体――黑磷,其转化过程如
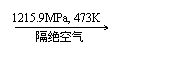 |
下:白磷 黑磷,黑磷性质稳定,结构与石墨相似。下列叙述正确的是( )
A.黑磷与白磷互为同分异构体
B.黑磷能导电
C.白磷转化为黑磷是物理变化
D.黑磷能在空气中自燃
9.香兰素的结构简式如图2所示,有宜人的气味,存在于香草豆、香脂、安息香、丁子油和香茅油中,是制作巧克力的辅助原料。下列关于香兰素的判断不正确的是 ( )
A.可与银氨溶液反应
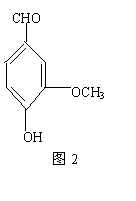 B.可与氢氧化钠溶液反应
B.可与氢氧化钠溶液反应
C.分子中所有原子都在同一平面上
D.分子式为C8H8O3
10.X、Y属于短周期元素,元素X的原子最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层有6个电子,则X与Y形成化合物的化学式可表示为( )
A.X2Y B.XY2
C.XY3 D.X2Y3
11.石榴石是石榴石族矿物的总称,颜色随成分的不同而变化,其组成可以表示为A3B2(SiO4)3,式中A、B均为金属元素,则A、B对应的化合价依次为 ( )
A.+2,+3 B.+3,+2
C.+2,+2 D.+3,+3
12.下列叙述正确的是 ( )
A.附着银的试管可先用少量稀氨水溶解,再用水洗净
B.苯酚的浓溶液不慎沾到皮肤上,应立即用氢氧化钠溶液擦洗
C.应将浓硝酸盛放在带橡胶塞的试剂瓶中,置于冷暗处保存
D.除去乙酸乙酯中的乙酸可加入饱和碳酸钠溶液,然后分液
![]() 13.在一定条件下,可逆反应2A(气)+B(气) nC(固)+D(气)达平衡。若维持温度不变,增大压强,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是 ( )
13.在一定条件下,可逆反应2A(气)+B(气) nC(固)+D(气)达平衡。若维持温度不变,增大压强,测得混合气体的平均相对分子质量不发生改变,则下列判断正确的是 ( )
A.其它条件不变,增大压强,平衡不发生移动
B.其它条件不变,增大压强,混合气体的总质量不变
C.该反应式中n值一定为2
D.原混合气中A与B的物质的量之比为2:1,且![]()
(其中M表示物质的摩尔质量)
14.常温下,将pH=5的硫酸溶液稀释到原来的500倍,则稀释后溶液中[SO42-]与[H+]之比约为 ( )
A.1:1 B.1:2
C.1:10 D.10:1
15.用中子轰击氧原子核的核反应方程式为 816O+01n→7aN+b0X,对式中X、a、b的判断正确的是 ( )
A.X代表中子,a=17, b=1
B.X代表电子,a=17,b=-1
C.X代表正电子,a=17,b=1
D.X代表质子,a=17,b=1
16.下面的叙述中正确的是 ( )
A.物体的温度升高,物体中分子热运动加剧,所有分子的热运动动能都会增大
B.对气体加热,气体的内能一定增大
C.物质内部分子间吸引力随着分子间距离增大而减小,排斥力随着分子间距离增大而增大
D.布朗运动是液体分子对悬浮颗粒碰撞作用不平衡造成的
17.如图3所示,从点光源S发出的一细束白光以一定的角度入射到三棱镜的表面,经过三棱镜的折射后发生色散现象,在光屏的ab间形成一条彩色光带。下面的说法中正确的是 ( )
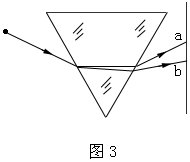 A.a侧是红色光,b侧是紫色光
A.a侧是红色光,b侧是紫色光
B.在真空中a侧光的波长小于b侧光的波长
C.三棱镜对a侧光的折射率小于对b侧光的折射率
D.在三棱镜中a侧光的传播速率大于b侧光的传播速率
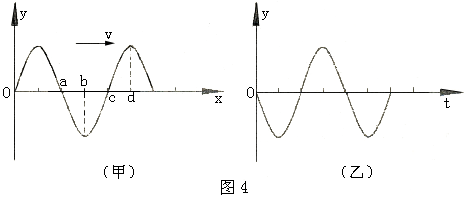
18.一列沿x轴正向传播的横波在某时刻的波形图如图4甲所示。a、b、c、d为介质中沿波的传播方向上四个质点的平衡位置,若从该时刻开始计时,则图4乙是下面哪个质点在经过3个周期后的振动图象? ( )
A.a处质点 B. b处质点
C.c处质点 D. d处质点
 |
19.有一种硬气功表演,表演者平卧地面,将一大石板置于他的身体上,另一人将重锤举到高处并砸向石板,石板被砸碎,而表演者却安然无恙。假设重锤与石板撞击后二者具有相同的速度。表演者在表演时尽量挑选质量较大的石板。对这一现象,下面的说法中正确的是 ( )
A.重锤在与石板撞击的过程中,重锤与石板的总机械能守恒
B.石板的质量越大,石板获得的动量就越小
C.石板的质量越大,石板所受到的打击力就越小
D.石板的质量越大,石板获得的速度就越小
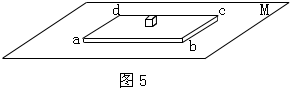
20.在水平桌面M上放置一块正方形薄木板abcd,在木板的正中点放置一个质量为m的木块,如图5所示。先以木板的ad边为轴,将木板向上缓慢转动,使木板的ab边与桌面的夹角为θ;再接着以木板的ab边为轴,将木板向上缓慢转动,使木板的ad边与桌面的夹角也为θ(ab边与桌面的夹角θ不变)。在转动过程中木块在木板上没有滑动。则转动以后木块受到的摩擦力的大小为 ( )

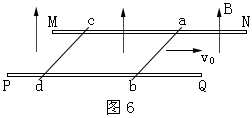
21.如图6所示,两根相互平行、间距为L的金属轨道MN和PQ固定在水平面内,轨道所在空间存在竖直向上的匀强磁场,磁感强度为B。在该轨道上垂直轨道方向放置两根金属杆ab和cd,它们的电阻分别为R1和R2,质量分别为m1和m2。开始时两金属杆静止在轨道上。某一时刻ab杆受到瞬间水平向右冲量作用,以初速度v0沿轨道滑动,这个瞬间cd杆的速度仍可视为零。已知金属杆ab和cd在轨道上滑动时所受到的摩擦力可忽略不计,金属轨道足够长且电阻不计,金属杆与轨道接触良好。以下说法中正确的是 ( )
A.当ab杆以水平初速度v0 开始在轨道上滑动瞬间,cd杆两端电势差为BLv0
B.当ab杆以水平初速度v0 开始在轨道上滑动瞬间,cd杆所受到磁场力方向与初速度v0方向相同,大小为![]()
C.在两杆都滑动的过程中,金属杆ab和cd总动量不变,大小总是m1v0
D.在两杆都滑动的过程中,金属杆ab动量减小,cd动量增大,ab和cd的总动量减小
 |
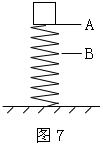
22.如图7所示,物体放在轻弹簧上,沿竖直方向在A、B之间做简谐运动。在物体沿DC方向由D点运动到C点(D、C两点未在图上标出)的过程中,弹簧的弹性势能减少了3.0J,物体的重力势能增加了1.0J。则这段过程中 ( )
 A.物体经过D点时的运动方向是指向平衡位置的
A.物体经过D点时的运动方向是指向平衡位置的
B.物体的动能增加了4.0J
C.D点的位置一定在平衡位置以上
D.物体的运动方向可能是向下的
理科综合能力测试
| 科目 | 第I卷 | 第II卷 | 总分 | ||||||||||||
| 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | ||||
| 生物 | ― | ― | ― | ― | ― | ― | ― | ― | ― | ||||||
| 化学 | ― | ― | ― | ― | ― | ― | ― | ||||||||
| 物理 | ― | ― | ― | ― | ― | ― | ― | ― | |||||||
第II卷(非选择题共168分)
本卷共12道题
以下数据可供解题时参考:
相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5
23.(8分)已知唾液中含有淀粉酶,淀粉酶可以催化淀粉的水解;又知鸡蛋被加热到650C后会“变熟”,但不知唾液淀粉酶被加热到650C后是否会影响其生物活性。为探究此问题,请你依据所给材料和用品设计出相应的实验方案,并预测可能的实验结果及可获得的相应结论。
材料和用品:经过稀释的唾液、经过稀释并煮熟的淀粉糊两份(一份保持在370C环境中,另一份保持在650C环境中)、碘酒、酒精灯或其它的加热设备、试管若干、量筒、滴管、大烧杯、温度计等。
实验方案:
(1)
(2)将一支试管放入370C左右的温水中,将另一支试管放入650C温水中,两试管均保持温度5min后取出。
(3)
可能的实验结果及相应的结论“
24.(12分)下面①~⑤列举了五种育种方法,请回答相关问题:
①甲品种×乙品种→F1→F1自交→F2→人工选择→自交→F3→人工选择→自交→性状稳定遗传(新品种)。
②甲品种×乙品种→F1→F1花药离体培养→若干幼苗→秋水仙素处理芽尖→若干植株→人工选择→新品种。
③正常的幼苗→秋水仙素处理→人工选择→新品种。
④人造卫星搭载种子→返回地面种植→发生多种变异→人工选择→新品种。
⑤获取甲种生物的某基因→通过某种载体将该基因携带入乙种生物→新生物个体
(1)第①种方法属常规育种,一般从F2代开始选种,这是因为______________
________________________________________________。
(2)在第②种方法中,我们若只考虑F1分别位于n对同源染色体上的n对等位基因,则利用其花药离体培育成的小苗应有_____________种类型(理论数据)。
(3)第③种育种方法中使用秋水仙素的作用是促使染色体加倍,其作用机理是
__________________________________________________________________________。
(4)第④种方法中发生的变异一般是基因突变,卫星搭载的种子应当选用萌动的(而非休眠的)种子,试阐述原因____________________________________________________。
(5)第⑤种方法培育的新生物个体可以表达出甲种生物的遗传信息,该表达过程包括遗传信息的__________________________。此遗传工程得以实现的重要理论基础之一是所有生物在合成蛋白质的过程中,决定氨基酸的_____________是相同的。
请依据下面的情景回答第25、26题:
碳元素及其化合和与生物生命活动、人类生产生活密切相关。在无机物中碳元素以二氧化碳、一氧化碳和碳酸盐等形式存在,同时碳原子又是组成有机物的主要骨架,与其它原子通过不同形式的结合形成多种化合物。在生物体内碳元素约占干重的49%,碳素营养是生物的生命基础。
25.(10分)请回答下列与碳素有关的问题:
(1)下面是发生在紫硫细菌体内的生化反应,据此判断其同化作用方式为_____________。
CO2+2H2S→(CH2O)+2S+H2O
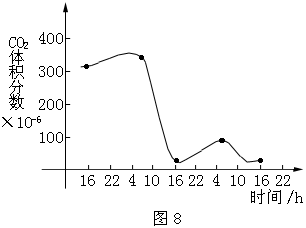 (2)北方农村常建造塑料薄膜温室在冬季栽培蔬菜。某温室从下午4点开始持续密封48小时,测得温室内CO2体积分数的变化情况(如图8所示)。试分析:
(2)北方农村常建造塑料薄膜温室在冬季栽培蔬菜。某温室从下午4点开始持续密封48小时,测得温室内CO2体积分数的变化情况(如图8所示)。试分析:
曲线b-c段大幅度下降的原因是__________________________,c-d的成因是__________________________。
检测结果表明,要提高温室的产量必须适时通风,你认为每天通风的时间最好选在曲线_____________区段相对应的时间内进行。
(3)温室生产过程中施用有机肥比单纯施用化肥具有明显的增产效果,试从碳素营养的角度分析其中的原因:__________________________。
26.(10分)在石油化工的加氢操作中,如果氢气中混有CO和CO2等杂质,会引起催化剂中毒,因此必须除去。
(1)在常温下,可以用银氨溶液来检测微量的CO,其原理与银镜反应相似,有银析出。写出银氨溶液与CO反应的化学方程式_______________________________________
_________________________________________________________________;
(2)工业上常采用甲烷化法除去少量碳的氧化物(CO、CO2)。其方法是:一定温度时,在催化剂的作用下,向碳的氧化物中通入氢气,使之转化为甲烷和易于除去的水。写出CO发生甲烷化反应的化学方程式__________________________________________;
(3)在上述两个反应中,CO依次作_____________________、_____________________(多选不得分)。
A.氧化剂 B. 既是氧化剂,又是还原剂
C.还原剂 D. 既不是氧化剂,又不是还原剂
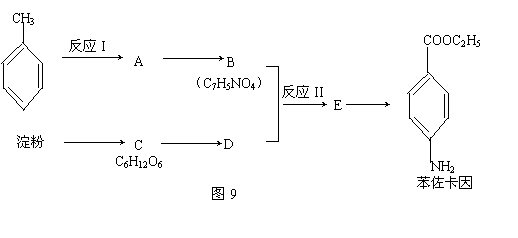 27.(18分)苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂使用。其合成路线如图9所示,其中有机物B具有酸性。
27.(18分)苯佐卡因是一种局部麻醉剂,可用于粘膜溃疡、创面及痔疮的镇痛,一般制成软膏或栓剂使用。其合成路线如图9所示,其中有机物B具有酸性。
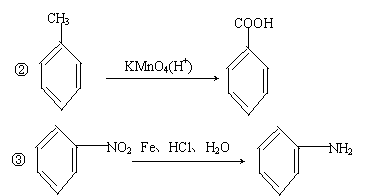
已知:
①苯环上的取代有如下定位规律:当苯环上的碳原子连有甲基时,可在其邻位或对位上引入官能团;当苯环上的碳原子连有羧基时,可在其间位上引入官能团。
 |
请写出:
(1)反应类型 反应I__________________,反应II_______________;
(2)化合物A、C的结构简式A_______________,C_______________;
(3)下列转化的化学方程式
C→D_____________________________________________,
B+D→E_____________________________________________;
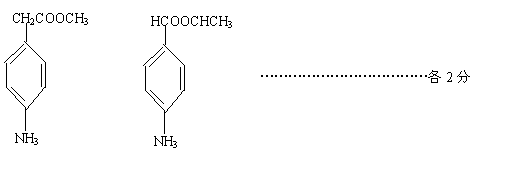
![]() (4)苯佐卡因有多种同分异构体,其中―NH2直接连在苯环上,分子结构中含有
(4)苯佐卡因有多种同分异构体,其中―NH2直接连在苯环上,分子结构中含有
―C―O―R官能团,且苯环上的一氯取代物只有两种的同分异构体共有6种,除苯佐卡因外,其中3种的结构简式是:
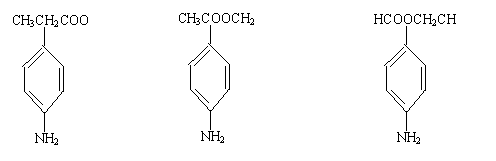 |
则剩余两种同分异构体的结构简式为
__________________________、__________________________。
28.(12分)实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲、乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取25.00mL甲溶液,向其中缓慢滴加乙溶液15.00mL,共收集到二氧化碳气体224mL。
②另取15.00mL乙溶液,向其中缓慢滴加甲溶液25.00mL,共收集到二氧化碳气体112mL。
上述气体体积均已换算为标准状况,则根据上述操作及实验数据填空:
(1)写出上述过程所涉及反应的离子方程式__________________________ __________________________;
(2)甲是_______________,甲溶液的物质的量浓度为________________,乙溶液的物质的量浓度为________________;(二氧化碳在溶液中的少量溶解忽略不计)
(3)将nmL的甲溶液与等体积的乙溶液按各种可能的方式混合,产生的气体体积为VmL(标准状况),则V的取值范围为________________________________。
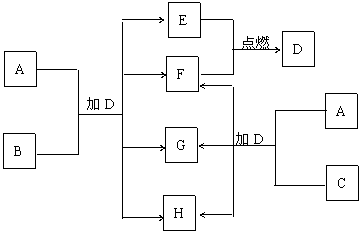 29.(12分)下列框图中的A-H是中学化学中常见的八种物质,所有物质均由短周期元素组成,其中B、C、G都含有同一种元素。B、E、F为单质。常温、常压下D为液体,E、F为气体,F是空气的主要成分之一。C由两种元素组成,其晶体熔点高、硬度大,闪烁着晶莹的光泽。A~H有可能发生如下转化,其反应关系如框图10所示:
29.(12分)下列框图中的A-H是中学化学中常见的八种物质,所有物质均由短周期元素组成,其中B、C、G都含有同一种元素。B、E、F为单质。常温、常压下D为液体,E、F为气体,F是空气的主要成分之一。C由两种元素组成,其晶体熔点高、硬度大,闪烁着晶莹的光泽。A~H有可能发生如下转化,其反应关系如框图10所示:
请填写下列空白:
(1)写出E+F→D的化学反应方程式________________________________;
(2)B的化学式________________,A的电子式________________;
(3)如图10所示A与C两种固体混合后,加入液体D,可能发生反应的化学方程式为____________________________________________________________________________。
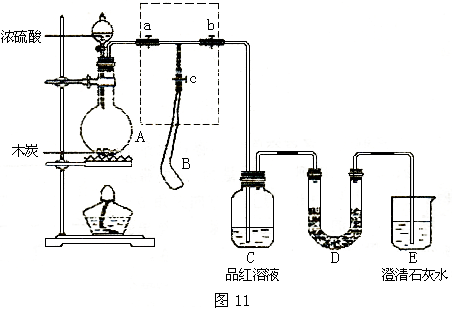 30.(14分)为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图11所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
30.(14分)为检验浓硫酸与木炭在加热条件下反应产生SO2和CO2气体,设计了如图11所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
请回答下列问题:
(1)实验前欲检查装置A的气密性,可以采取的操作是___________________________
________________________________________________________________________________________________________________________________________________;
(2)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是________________(用操作编号填写);
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(3)实验时,装置C中的现象为________________________________;
(4)当D中产生____________(多选不得分)现象时,可以说明使E中澄清石灰水变浑的是CO2,而不是SO2;
A.进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
B.脱脂棉上蓝色均变浅
C.脱脂棉上蓝色褪去
则装置D的作用为________________________________________________。
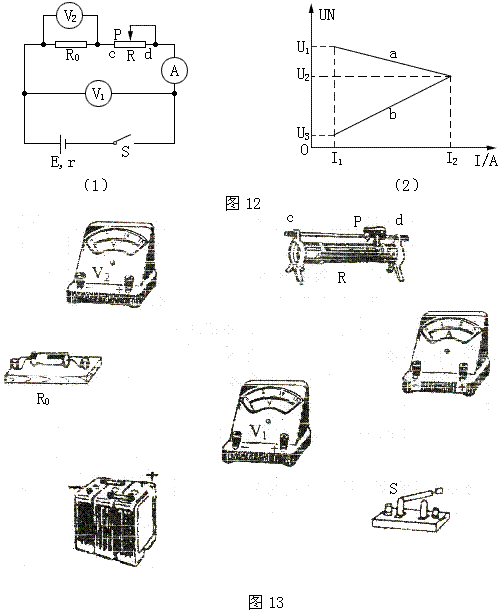
31.(17分)某同学利用如图12(1)所示电路测定电源的电动势和内电阻。实验中电表内电阻对实验结果的影响很小,均可以忽略不计。闭合电键S后,变阻器的滑动触头p由变阻器的一端滑到另一端的过程中,两电压表示数随电流表示数变化情况分别如图(2)的U-I图象中直线a、b所示。
(1)若滑动触头p由变阻器的一端滑到另一端的过程中,电压表V2的示数一直增大,可知滑动触头p由__________端滑到___________端;(用电路图中的字母表示)
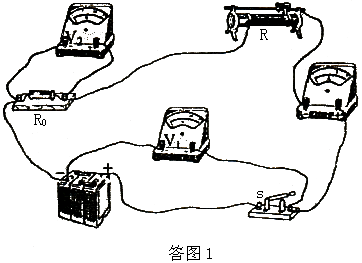
(2)用画线代表导线,将图13的实物图中各元件按图12(1)连接成实验电路;
(3)通过分析可知,其中图12(2)中图线__________(填“a”或“b”)表示电压表V1示数随电流表A示数变化的关系;
(4)根据U-I图象中坐标轴所标出的数据,可以求出电源电动势E=________________,内电阻r=________________(用图中给出的坐标值表示)。
 |
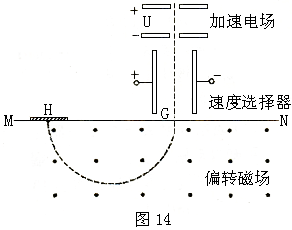
32.(15)如图14所示为质谱仪的原理示意图,电荷量为q、质量为m的带正电的粒子从静止开始经过电势差为U的加速电场后进入粒子速度选择器,选择器中存在相互垂直的匀强电场和匀强磁场,匀强电场的场强为E、方向水平向右。已知带电粒子能够沿直线穿过速度选择器,从G点垂直MN进入偏转磁场,该偏转磁场是一个以直线MN为边界、方向垂直纸面向外的匀强磁场。带电粒子经偏转磁场后,最终到达照相底片的H点。可测量出G、H间的距离为l。带电粒子的重力可忽略不计。求:(1)粒子从加速电场射出时速度v的大小。(2)粒子速度选择器中匀强磁场的磁感强度B1的大小和方向。(3)偏转磁场的磁感强度B2的大小。
 |
33.(18分)一位同学的家住在一座25层的高楼内,他每天乘电梯上楼,经过多次仔细观察和反复测量,他发现电梯启动后的运动速度符合如图15所示的规律,他就根据这一特点在电梯内用台秤、重物和停表测量这座楼房的高度。他将台秤放在电梯内,将重物放在台秤的托盘上,电梯从第一层开始启动,经过不间断地运行,最后停在最高层。在整个过程中,他记录了台秤在不同时间段内的示数,记录的数据如下表所示。但由于0~3.0s段的时间太短,他没有来得及将台秤的示数记录下来。假设在每个时间段内台秤的示数都是稳定的,重力加速度g取10m/s2.
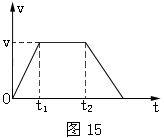 (1)电梯在0~3.0s时间段内台秤的示数应该是多少?
(1)电梯在0~3.0s时间段内台秤的示数应该是多少?
(2)根据测量的数据,计算该座楼房每一层的平均高度。
| 时间/s | 台秤示数/kg |
| 电梯启动前 | 5.0 |
| 0~3.0 | |
| 3.0~13.0 | 5.0 |
| 13.0~19.0 | 4.6 |
| 19.0以后 | 5.0 |
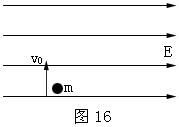
34.(22分)在足够大的真空空间中,存在水平向右方向的匀强电场,若用绝缘细线将质量为m的带正电小球悬挂在电场中,静止时细线与竖直方向夹角θ=370。现将该小球从电场中的某点竖直向上抛出,抛出的初速度大小为v0,如图16所示。求:(1)小球在电场内运动过程中的最小速率。(2)小球从抛出至达到最小速率的过程中,电场力对小球做的功。(sin370=0.6, cos370=0.8)
 |
高三理科综合能力测试第二学期期中练习参考答案及评分标准
第I卷(共132分)
本卷共22题,每题6分
1. B 2. A 3. B 4. C 5. B 7. D 7. B 8. B 9. C 10. B 11. A 12. D
13. D 14. C 15. C 16. D 17. B 18. C 19. D 20. B 21.C 22.A
第II卷(共168分)
本卷共12道题
23.(8分)
实验方案:
(1)取甲、乙两支试管分别作标记,一支注入370C的淀粉糊3mL,另一支注入650C的淀粉糊3mL,再向两试管各注入2mL唾液。两试管均振荡。
注:本题要求答出两个要点:①试管要做标记;②每种液体在两支试管内加入的量要相等……………………………………………………………………………………………2分
(3)冷却后,分别向两试管内滴入等量的碘酒,观察并比较两试管中液体的颜色。
注:本题要求答出两个要点:①加等量的碘酒(可以不强调等量)②比较颜色
……………………………………………………………………………………………2分
可能的实验结果及相应的结论:
(1)若两试管中液体的颜色相同(或均无颜色反应、或均为碘酒的颜色),则证明唾液淀粉酶在被加热到650C后并未丧失其生物活性。……………………………………2分
(2)若经370C处理的试管内液体无颜色反应,而经650C处理的试管中液体呈现蓝色反应,则证明唾液淀粉酶被加热到650C后丧失了生物活性。(或经370C处理的试管内液体无颜色反应,而经650C处理的试管中液体的颜色比前者略深,则证明唾液淀粉酶被加热到650C后生物活性减弱)。(答出两种可能之一即给满分)………………………………2分
24.(12分)
(1)从F2代开始发生性状分离
注:①若答案指向对基因型的选择不给分;②除参考答案外,若再增加其它不正确的表述不得分,如回答“F2代出现符合育种目标的纯合体”不得分。…………………2分
(2)2n…………………………………………………………………………………2分
(3)秋水仙素抑制纺锤体的形成………………………………………………………2分
注:答案的核心是影响纺锤体或纺锤丝的形成过程,而非破坏已形成的纺锤体或纺锤丝。
(4)答案要点:①种子萌动后进行细胞分裂;②DNA在复制过程中可能由于某种因素的影响发生基因突变…………………………………………………………………………2分
注:以上两要点各占1分;若答出“间期细胞易发生基因突变”给2分。
(5)转录和翻译(答案不全不给分)密码子(其它答案如“遗传密码”不给分)
……………………………………………………………………………………………2分
25.(10分)
(1)自养型或光合自养型(答案不得扩展)…………………………………………2分
(2)光合作用合成有机物利用了室内大量的CO2……………………………………2分
进行呼吸作用释放CO2……………………………………………………………………2分
b―c(或d―e) ……………………………………………………………………………2分
(3)土壤微生物分解有机肥,释放CO2。(与碳素营养无关的多余答案若正确不扣分,若有错误则必须扣分)………………………………………………………………………2分
26.(共10分)
(1)CO+2[Ag(NH3)2]OH=NH4HCO3+3NH3+2Ag↓(原理正确均给分)……………
……………………………………………………………………………………………3分
 |
(2)CO+3H2 CH4+H2O(条件1分,下同)…………………………………3分
(3)C A …………………………………………………………………………各2分
27.(共18分)
(1)硝化反应(或取代反应)酯化反应(或从形式上也可看作是取代反应)………
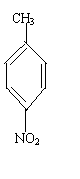 …………………………………………………………………………………………各2分
…………………………………………………………………………………………各2分
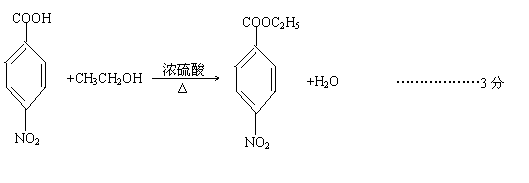
(2) CH2OH(CHOH)4CHO ……………………………………………各2分
 |
(3)C6H12O6 2C2H5OH+2CO2↑…………………………………………3分
 |
 (4)
(4)
28.(共12分)
(1)CO32-+2H+=CO2↑+H2O, CO32-+H4=HCO3-, HCO3-+H+=CO2↑+H2O(不按上述顺序书写或未写CO32-+2H+=CO2↑+H2O也给4分)……………………………………共4分
(2)盐酸(或HCl) 0.8mol・L-1 1.0mol・L-1(不要求有效数字位数)…………
………………………………………………………………………………………各2分
(3)0≤V≤8.96n 或[0, 8.96n]…………………………………………………2分
第(2)题提示:根据两种不同操作中,Na2CO3与HCl量分别相同,产生CO2量却不同,说明盐酸不足。
由操作①:n1(CO2)=224mL÷22400mL・mol-1=0.01mol
据反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O
0.02mol 0.01mol
c(HCl)=0.02mol÷0.025L=0.8mol・L-1
由操作②:n2(CO2)=112mL÷22400mL・mol-1=0.005mol
设:15mLNa2CO3溶液中Na2CO3的物质的量为x
据反应:NaCO3+HCl=NaCl+NaHCO3
x x
NaHCO3+HCl=NaCl+CO2↑+H2O
0.005mol 0.005mol
0.005mol+x=0.02mol
x=0.015mol
c(Na2CO3)=0.015mol÷0.015L=1mol・L-1
第(3)题提示:据反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O
![]()
n(CO2)=1/2n(HCl)=1/2×0.8mol・L-1×n×10-3L=4n×10-4mol
则CO2最大生成量为V(CO2)=22400mL・mol-1×4n×10-4mol=8.96nmL
据反应:Na2CO3+HCl=NaCl+NaHCO3
![]()
则CO2最小生成量为V(CO2)=0mL
则0≤V≤8.96n
![]() 29.(共12分)
29.(共12分)
(1)2H2+O2 2H2O………………………………………………………………2分
(2)Al(或Si) Na+[:O:O:]2-Na+………………………………………………各2分
(3)2Na2O2+2H2O=4NaOH+O2↑, Al2O3+2NaOH=2NaAlO3+H2O
(或SiO2+2NaOH=Na2SiO3+H2O)(答案合理均给分)………………………………共6分
30.(共14分)
(1)关闭分液漏斗的活塞,打开止水夹a和b,关闭止水夹c,用手捂热(或微热)圆底烧瓶A,若C中有气泡冒出,移开手掌(或热源)后,C处导管内有水上升,则证明A装置的气密性良好(答案合理均给分)……………………………………………………3分
(2)③①②……………………………………………………………………………3分
(3)品红溶液褪色……………………………………………………………………2分
(4)A……………………………………………………………………………………2分
除去SO2并检验SO2已被除净…………………………………………………………4分
31.(17分)
(1)d c ………………………………………………………………………………3分
(2)如答图1连接……………………………………………………………………3分
(3)a……………………………………………………………………………………3分
 |
![]() …………………………………………………………………4分
…………………………………………………………………4分
![]() …………………………………………………………………………4分
…………………………………………………………………………4分
32.(共15分)
解:(1)设带电粒子被加速电场加速后的速度为v,根据动能定理
![]()
解得:![]() ……………………………………………………………………5分
……………………………………………………………………5分
(2)带正电粒子以速度v进入相互垂直的电、磁场做直线运动,受到水平向右的电场力qE,水平向左的洛伦兹力qvB1,用左手定则可判断磁场B1方向垂直纸面向外……2分
且 ![]()
可解得:![]() ………………………………………………………………3分
………………………………………………………………3分
(3)粒子以速度v从G进入偏转磁场,受到洛伦兹力做匀速圆周运动,到达照相底片的H点,圆周运动的半径R=1/2
洛伦兹力提供了粒子运动的向心力,根据牛顿第二定律,可得
![]() ……………………………………………………………………………2分
……………………………………………………………………………2分
将(1)的v代入,解得![]() ………………………………………………3分
………………………………………………3分
33.(共18分)
解:(1)电梯启动前,台秤示数为5.0kg,则物体重力G=mg=50N.………………1分
由于表中各段时间内台秤示数恒定,所以在时间t1(0~3.0s)内,物体做匀加速运动,在时间t2(3.0s~13.0s)内物体做匀速直线运动,在时间t3(13.0s~19.0s)内物体做匀减速直线运动,19.0s末速度减为零。
在13.0s~19.0s内,物体所受的支持力N3=46N,根据牛顿第二定律
mg-N3=ma3
得在时间t3内物体的加速度![]() ……………………………3分
……………………………3分
13.0s末物体的速度v2=a3t3=4.8m/s。…………………………………………………2分
而由于电梯在13.0s末的速度与3.0s末的速度相同。因此根据匀变速运动规律,物体在0~3.0s内的加速度
![]() ……………………………………………………………………2分
……………………………………………………………………2分
根据牛顿第二定律N1-mg=ma1
解得:N1=58N。即台秤的示数为5.8kg………………………………………………2分
(2)0~3.0s内物体的位移![]() ………………………………………2分
………………………………………2分
3.0s~13.0s内物体的位移![]() ……………………………………………1分
……………………………………………1分
13.0s~19.0s内物体的位移![]() ………………………………………2分
………………………………………2分
则电梯上升的总高度,实际为24层的总高度
s=s1+s2+s3=69.6m…………………………………………………………………………2分
平均每层楼高 ![]() ………………………………………………………2分
………………………………………………………2分
34.(22分)
解:(1)小球静止在电场中时,根据力的平衡条件
![]() ………………………………………………………………2分
………………………………………………………………2分
小球被抛出以后,受到重力和电场力的共同作用,沿重力方向的分运动是匀减速运动,加速度为g,设t时刻的速度为v1,沿电场方向的分运动是初速度为0的匀加速运动,设加速度为a,t时刻的速度为v2,则有
![]() ………………………………………………5分
………………………………………………5分
小球t时刻的速度大小为 ![]()
由以上各式得出:![]()
解得v的最小值为:![]() ………………………………………………………7分
………………………………………………………7分
vmin的方向与电场力和重力的合力方向垂直,即与电场的方向夹角为370。
说明:如果将速度按照合力方向和垂直合力方向分解,当沿合力方向的速度减为零时其速度达到最小值,也可以解出最小速度。该问也同样给分。
如果运用速度矢量合成的三角形法则解此问,用文字叙述清楚,该问也同样给分。
(2)小球沿电场方向的位移为![]()
而小球在到达最小速度时,沿电场方向的速度为![]() ………4分
………4分
得小球沿电场方向的位移为![]()
电场力做功为![]() ……………………………………4分
……………………………………4分