试卷类型:A
2003年MAM高考理综仿真试题(七)
MAM: M-March A-April M-May
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。第Ⅰ卷第1至5页,第Ⅱ卷第6至12页。满分为300分,考试时间为150分钟。
第Ⅰ卷(选择题 共132分)
注意事项:
1.答第Ⅰ卷前,考生务必将自己的姓名、准考证号、考试科目、试卷类型用铅笔涂写在答题卡上。
2.每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号。不能答在试卷上。
3.考试结束后,考生将本试卷和答题卡一并交回。
一、选择题(本题共22小题,每小题6分,共132分,每小题的四个选项中只有一项符
合题意)
1.我国农业因遭受酸雨而造成的损失每年高达15亿元,为了有效控制酸雨,国务院已批准《酸雨控制区和二氧化碳污染控制区方案》等法规,你认为减少酸雨产生的有效途径是
①减少煤炭燃烧②把工厂烟囱造高③燃烧脱硫④在已酸化的土壤中加石灰⑤开发新能源
A.①②③ B.②③④⑤ C.①③⑤ D.①③④⑤
2.在正常情况下,叶肉细胞中细胞液的浓度与根毛细胞细胞液浓度相比较
A.大 B.小 C.相等 D.不确定
3.玉米的胚乳细胞内共有染色体30个,由此可知其卵细胞、极核和精子内的染色体数目为
A.10、10、10 B.10、15、15
C.15、15、15 D.10、20、10
4.以下是果蝇产生眼色素B和D的反应
底物A 酶X 色素B
![]()
底物C 酶Y 色素D
![]()
野生的果蝇有两种色素,眼睛为红褐色,缺乏色素B表现为鲜红色眼,缺乏色素D为褐色眼,两色素都没有表现为白色眼。现将一纯合的白眼果蝇同一只野生型果蝇交配,则子一代酶的存在情况是
A.只有一种酶X
B.只有一种酶Y
C.酶X和酶Y都有
D.酶X和酶Y都无
5.有一种昆虫酷似黄蜂,腹部也有清晰的明暗相间的横纹,当这种昆虫迁移到一个没有黄蜂的环境中,你预测
A.这种昆虫在没有黄蜂的新环境中很快被淘汰
B.这种昆虫在与捕食者的斗争中逐渐形成有毒或有恶臭的特征
C.这种昆虫的拟态在没有黄蜂的环境中也能很好的生存
D.这种昆虫在没有黄蜂的环境中,通过与捕食者之间的激烈斗争,逐渐由拟态转变成保护色而生存下来
6.为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成分都是
A.碳水化合物 B.碳氢化合物
C.氢气 D.醇类
7.飘尘是物质燃烧时产生的粒状漂浮物,其颗粒很小,不易沉降,它与空气中的SO2接触时,SO2会部分转化为SO3。飘尘所起的作用是
A.催化剂 B.还原剂 C.氧化剂 D.供氧剂
8.宣传科学,介绍高新技术,揭露伪科学,是教育者的义务,下列各项中属于伪科学的是
①用催化剂将水变成油
②稻草可变成酒精
③在异地“发功”给人治病
④用碘化银人工降雨
A.①②③④ B.②③④
C.①③ D.③④
9.若在宇宙飞船的太空实验室(失重条件下)进行以下实验,其中最难完成的是
A.将金粉和铜粉混合
B.将牛奶加入水中混合
C.蒸发食盐水制取食盐晶体
D.用漏斗、滤纸过滤除去水中的泥沙
10.科学家致力于二氧化碳的“组合转化”技术研究,把过多的二氧化碳转化为有益于人类的物质。如将CO2与H2混合,在一定条件下以1∶3的比例发生反应,生成某种重要的化工原料和水。该化工原料可能是
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
11.电解制铝工厂的一指标是:电解得到1.0 t Al,阳极(C)损耗0.6 t,则阳极上生成的产物可能是
A.只有CO2 B.只有CO
C.CO(多)和CO2(少) D.CO(少)和CO2(多)
12.某条件可以进行反应2CH4![]() C2H2+3H2。在1 L真空容器中充入1 mol CH4,达到平衡后,测得CH4含量为m%。若相同条件下往此容器中充入2 mol CH4,平衡后CH4的含量
C2H2+3H2。在1 L真空容器中充入1 mol CH4,达到平衡后,测得CH4含量为m%。若相同条件下往此容器中充入2 mol CH4,平衡后CH4的含量
A.大于m% B.等于m%
C.小于m% D.无法判断
13.若200 mL c(H+)=1×10-3 mol/L的某一元酸和100 mL c(OH-)=1×10-3 mol/L的某一元碱相混合后,溶液呈碱性。所用的酸和碱应是
A.等浓度的弱酸和强碱
B.稀的强酸和稀的强碱
C.稀的弱酸和浓的强碱
D.稀的强酸和浓的弱碱
14.瑞典皇家科学院2001年10月10日宣布,2001年诺贝尔化学奖授予“手性催化氢化、氧化反应”研究领域做出贡献的美、日三位科学家。在有机物中,若碳原子上连接的四个原子或原子团不同,则这个碳原子称为手性碳原子。下列分子中含有“手性碳原子”的是
A.CBr2F2 B.CH3CH2OH C.CH3CH2CH3 D.CH3CH(OH)COOH
15.天然放射物质的放射线包含三种成分,下列说法中正确的是
①一张厚的黑纸可以挡住α射线,但不能挡住β射线和γ射线
②某原子核在放出γ粒子后,会变成另一种元素的原子核
③三种射线中对气体电离作用最强的是α射线
④β粒子是电子,但不是原来绕核旋转的核外电子
A.①② B.①③④ C.②④ D.②③④
16.如图,一质量为M各面均光滑的劈形物体,放在固定的斜面上,劈形物体的上表面呈水平,其上放一质量为m的光滑小球,劈形物体从静止释放,不计空气阻力,小球在碰到斜面前的运动轨迹是
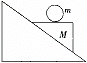 A.平行于斜面的直线
A.平行于斜面的直线
B.抛物线
C.竖直的直线
D.水平的直线
17.由上海飞往美国洛杉矶的飞机在飞越太平洋上空的过程中,如果保持飞行速度的大小和距海面的高度均不变,则以下说法中正确的是
A.飞机做的是匀速直线运动
B.飞机上的乘客对座椅的压力略大于地球对乘客的引力
C.飞机上的乘客对座椅的压力略小于地球对乘客的引力
D.飞机上的乘客对座椅的压力为0
18.市场上有种灯具俗称“冷光灯”,用它照射物品时能使被照物品处产生的热效应大大降低,从而广泛地应用于博物馆、商店等处。这种灯降低热效应的原因之一是在灯泡后面放置的反光镜玻璃表面上镀一层薄膜(例如氟化镁),这种膜能消除不镀膜时玻璃表面反射回来的热效应最显著的红外线,以λ表示此红外线的波长,则所镀薄膜的厚度最小应为
A.![]() B.
B. ![]() λ
C.
λ
C. ![]() λ
D.λ
λ
D.λ
19.S1、S2是振动情况完全相同的两个机械波波源,振幅为A,a、b、c三点分别位于S1、S2连线的中垂线上,且ab=bc,某时刻a是两列波的波峰相遇点,c是两列波的波谷相遇点,则
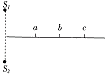 A.a处质点的位移始终为2A
A.a处质点的位移始终为2A
B.c处质点的位移始终为-2A
C.b处质点的振幅为2A
D.c处质点的振幅为0
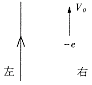 20.初速度为V0的电子,沿平行于通电长直导线的方向射出,直导线中电流方向与电子的初始运动方向如图,则
20.初速度为V0的电子,沿平行于通电长直导线的方向射出,直导线中电流方向与电子的初始运动方向如图,则
A.电子将向右偏转,速率不变
B.电子将向左偏转,速率改变
C.电子将向左偏转,速率不变
D.电子将向右偏转,速率改变
21.有一种高速磁悬浮列车的设计方案是在每节车厢底部安装磁铁(磁场方向向下),并在两条铁轨之间沿途平放一系列线圈。下列说法中不正确的是
A.当列车运动时,通过线圈的磁通量会发生变化
B.列车速度越快,通过线圈的磁通量变化越快
C.列车运行时,线圈中会产生感应电流
D.线圈中感应电流的大小与车速无关
22.某农村水力发电站的发电机的输出电压稳定,它发出的电先通过电站附近的升压变压器升压,然后用输电线路把电能输送到远处村寨附近的降压变压器,经降低电压后,再用线路接到各用户,设两变压器都是理想变压器,那么在用电高峰期,白炽灯不够亮,但用电总功率增加,这时
A.升压变压器的副线圈的电压变大
B.高压输电线路的电压损失变大
C.降压气压器的副线圈上的电压变大
D.降压变压器到各用户的输电线上的电压损失变大
第Ⅱ卷(非选择题 共168分)
注意事项:
1.第Ⅱ卷共7页,用钢笔或圆珠笔直接答在试题卷上。
2.答卷前将密封线内的项目填写清楚。
23.(11分)4000多年前的巴比伦王国是一个经济繁荣、显赫一时的大国,其森林繁多,
资源丰富,自然生态环境优越,但由于人口剧增,森林被砍,耕地扩大,结果造成水土流失,河道阻塞,连年洪水成灾,终于使土壤沙漠化、盐渍化,致使该国变成一片废墟。请根据以下资料回答下列问题:
(1)该国的灭亡,主要是由于失去了森林的哪些作用?
___ ________
(2)造成生态平衡被破坏的主要原因是
A.自然因素
B.生态系统的调节能力有限
C.人口剧增导致对自然资源的不合理利用
D.人口剧增造成环境污染
(3)这个事实告诉我们,对于任何生产活动都要在遵循___________的前提下进行。
(4)要使一个国家的生态环境比较优越,农牧业生产比较稳定,森林覆盖率要达到______________________且分布均匀。
24.(8分)随着科学技术的发展,化学农药的产量和品种逐年增加。但害虫的抗药性也不断增强,对农作物危害仍然很严重,如近年来,棉铃虫在
我国大面积暴发成灾,造成经济损失每年达100亿元以上,针对这种情况,江苏农科院开展“转基因抗虫棉”的科技攻关研究,成功地将抗虫基因导入棉花细胞中,得到的棉花新品种对棉铃虫的毒杀效果高达80%以上。请回答下列问题:
(1)害虫抗药性的增强是___________的结果。
(2)“转基因抗虫棉”抗害虫的遗传信息传递过程可以表示为:
___________
(3)该项科技成果在环境保护上的重要作用是___________。
(4)科学家们预言,此种“转基因抗虫棉”独立种植若干代以后,也将出现不抗虫的植株,此现象来源于___________。
25.(20分)据图回答下列问题:
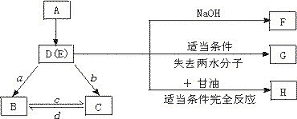
其中A、B、C是生物物质代谢常见的三种重要物质,A水解生成D。化合物E是D类的一种,它的相对分子量为75,元素百分比组成为碳32%,氢6.67%,氮18.79%,其余是氧,其中G属A类,H属于C类。
(1)写出下列物质的结构简式
E___________F___________G___________H___________
(2)写出下列物质的名称
A___________B___________C___________D___________
(3)用谷物喂养鸭子,能迅速育肥,其过程可表示为途径a、b、c、d中的___________。冬眠的熊能保持血糖相对稳定,是通过___________。
(4)对A、B、C三种物质,胃所分泌的酶能消化的是___________
26.(14分)用右图所示装置进行实验,将A逐滴加入B中。
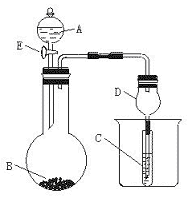
(1)若A为浓硫酸;B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到溶液褪色,则B是___________然后往烧杯中加入沸水,又可观察到的现象是___________。
(2)若B为Na2CO3;C为C6H5ONa溶液,实验中观察到小试管内溶液变浑浊,则酸A应具备的性质是___________。然后往烧杯中加入沸水,可观察到的现象是___________。
(3)若B是生石灰,实验中观察到C溶液中先形成沉淀,尔后沉淀溶解,当溶液恰好澄清时,关闭E,然后往烧杯中加入热水,静置片刻,观察到试管壁上出现光亮的银镜。则A是___________,C是___________与葡萄糖的混合液。仪器D在此实验中的作用是___________。
27.(16分)A是淡黄色的固体,其焰色反应呈黄色;B是100 mL AlCl3溶液,A与B恰好完全反应且只生成O2与C溶液。
(1)A的名称是___________。
(2)将B蒸干、灼烧,所发生反应的化学方程式为:
___________;___________。
(3)将C溶液也蒸干,可得到NaCl与___________的固态混合物。
(4)若生成的O2在标准状况下体积为V L,则AlCl3溶液物质的量浓度C(用含V的关系式表示)为___________。
28.(18分)碘缺乏症遍及全球,多发生于山区,南美的安第斯山区、欧洲的阿尔卑斯山区和亚洲的喜马拉雅山区是高发病地区。我国云南、河南等10余省的山区发病率也较高。据估计我国患者大约有100万人。为控制该病的发生,较为有效的方法是食用含碘食盐。我国政府以国家标准的方式规定在食盐中添加碘酸钾(KIO3)。据此回答下列问题:
(1)碘是合成下列哪种激素的主要原料之一
A.胰岛素 B.甲状腺激素 C.生长激素 D.雄性激素
(2)长期生活在缺碘山区,又得不到碘盐的供应,易患
A.甲状腺亢进 B.佝偻病 C.地方性甲状腺肿 D.糖尿病
(3)可用盐酸酸化的碘化钾和淀粉检验食盐中的碘酸钾。反应的化学方程式为___________,氧化产物与还原产物的物质的量之比为___________,能观察到的明显现象是___________。
(4)已知KIO3可用电解方法制得。原理是:以石墨为阳极,以不锈钢为阴极,在一定电流强度和温度下电解KI溶液。总反应化学方程式为:KI+3H2O======KIO3+3H2↑,则两极反应式分别为:阳极___________,阴极___________。
(5)在某温度下,若以12 A的电流强度电解KI溶液10 min,理论上可得到标况下氢气___________L。
29.(24分)某工厂废液经测定得知主要含有乙醇,其中还溶有丙醇、乙酸和乙酸乙酯。现欲从废液中回收乙醇和乙酸,根据各物质的沸点,补充下列实验步骤,模拟实现这一过程,并回答有关问题。
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
可供选择的实验用品:
1 mol·L-1烧碱溶液;18.4 mol·L-1硫酸;蒸馏水和冰;400 mL烧杯;250 mL烧杯;
250 mL蒸馏烧瓶;温度计;冷凝器;接受器;玻璃棒以及中学化学实验的常用仪器。
(1)补充下列实验步骤:
①组装蒸馏装置,检查气密性;
②取100 mL废液注入250 mL蒸馏烧瓶中,滴入1 mol·L-1烧碱溶液,调废液pH=10;
③___________; ④___________;
⑤___________; ⑥___________。
(2)滴入1 mol·L-1烧碱溶液,使溶液的pH=10的目的是___________。
(3)用18.4 mol·L-1硫酸的目的是(用化学方程式表示):___________。
(4)最后蒸馏烧瓶内残留液中的溶质的主要成分是___________。
30.(16分)(1)在“测定金属的电阻率”的实验中,电阻丝的电阻约为4~6 Ω,可供选择的主要器材如下:
A.电压表(量程0~3 V,内阻15 kΩ)B.电流表(量程0~0.6 A,内阻2 Ω)
C.电流表(量程0~1 A,内阻0.5 Ω)D.滑动变阻器(额定电流1 A,内阻20 Ω)
E.滑动变阻器(额定电流0.5 A,阻值为1 000 Ω)
F.电池组(电动势为4 V,内阻为0.5 Ω)
要求测量时误差小,电压从0开始调节,滑动变阻器向左滑动时电压变大。
①电流表应选___________,滑动变阻器应选___________。
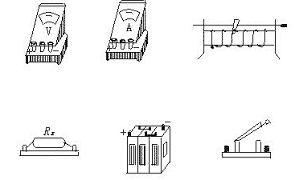
②把下图所示的器件,连接成测量电路。
(2)如图为一个理想变压器的示意图,输出端有两组线圈。现在三个小灯泡L1:“6 V、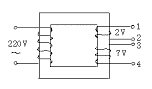 0.9 W”,L2:“6 V、0.9 W”,L3:“3 V、0.9 W”。要使它们接在同一电路上都能正常发光,在答题纸上画出它们的接线图,这时初级线圈中电流的最大值Im=___________A。
0.9 W”,L2:“6 V、0.9 W”,L3:“3 V、0.9 W”。要使它们接在同一电路上都能正常发光,在答题纸上画出它们的接线图,这时初级线圈中电流的最大值Im=___________A。
31.(12分)对宇宙的分析研究中,一个最有趣的宇宙物体就是所谓的“黑洞”,它是某些类型星体(设质量为M的均匀球)的最后演变期。研究证明,黑洞确实存在,设星体表面发出频率为ν的光子,其能量为hν,由爱因斯坦质能方程,光子的质量可以描述为m=hν/c2;已知质量为m的粒子,离星体中心为r0处的引力势能为Ep=-GMm/r0,此处h为普朗克常数,c为光速,G为万有引力恒量。根据黑洞的性质,我们可以用能量守恒原理近似地求解黑洞临界半径R的数量级。
(1)简述“黑洞”最主要的一个物理性质。
(2)试求解黑洞临界半径R。
 (3)据分析,太阳演变的最后阶段,很可能变成所谓的“黑洞”,如已知太阳的质量为6×1030 kg,估算太阳变成黑洞时的半径R。
(3)据分析,太阳演变的最后阶段,很可能变成所谓的“黑洞”,如已知太阳的质量为6×1030 kg,估算太阳变成黑洞时的半径R。
32.(17分)如图所示,一个带电小物块P,沿一个绝缘的倾斜轨道向上运动,设运动过程中P的带电量保持不变,空间存在着匀强电场(未在图中画出)。
已知P经过A点时动能30 J,经过B点时动能减少了10 J,机械能增加了20 J,电势能减少了35 J,P运动到C点时速度刚好减为零。(设小物块P所受滑动摩擦力的大小不变)
(1)求小物块P从A到C的运动过程中,克服摩擦力所做的功。
(2)小物块P到达C点后会不会沿轨道向下运动?为什么?
33.(12分)(1)如图所示是利用高频交流电焊接自行车零件的原理示意图,其中外圈A是通高频交流电的线圈,B是自行车的零件,a是待焊接的接口,接口两端接触在一起。
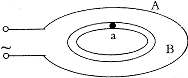
当A中通有交变电流时,B中会产生感应电流,便使接口处金属熔化而焊接起来。为什么在其他条件不变的情况下,交变电流的频率越高,焊接越快?
(2)分析为什么焊接过程中,接口a处已被熔化而零件的其他部分并不很热?
(3)NH4Cl常用在金属焊接上,以除去金属表面上的氧化物薄层,请用方程式表示除锈的过程。
(4)高频焊接时线圈中通过高频交流电,金属工件的焊缝中就产生大量焦耳热,要使焊接处产生的热量较大,可采用
A.增大交变电流的电压
B.增大交变电流的频率
C.增大焊接缝的接触电阻
D.减少焊接缝的接触电阻