2006届永嘉二中高三第二次周考
理科综合能力测试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分300分。考试时间150分钟。
第I卷(选择题,共21题,共126分)
一、选择题(本题包括13小题。每小题只有一个选项最符合题意)
1.N和P是组成生物体的重要元素,下列相关叙述中正确的是
①N、P不仅是生物膜的重要部分,也是ATP、DNA、RNA等细胞内重要化合物不可缺少的成分。
②花盆中正常生长的米兰转移到缺乏N、P的培养液一段时间后,幼嫩叶片首先表现出相应的缺乏症。
③大气中的N2必须经固氮作用才能被生物所利用,固氮作用包括生物固氮、工业固氮、高能固氮三种方式。
④健康成年男子和重创伤恢复期病人在一段时间内,机体摄入的氮量均大于排出的氮量。
A.①② B.③④ C.①③ D.④②
2.荠菜传粉受精,一段时间后,胚珠中大型泡状细胞、胚乳核的数量以及有机物的含量变化依次为
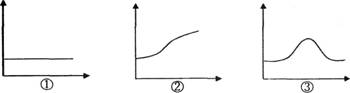 |
A.①②③ B.②③② C.①③② D.①③③
3.水稻(基因型为AaBb)的花药通过无菌操作,接入试管,经过如下过程培育试管苗。以下选项中正确的是
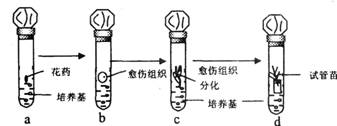 |
A.a:用花药离体培养法获得单倍体植株;b:通过有丝分裂产生愈伤组织;c:培养基中至少应有乙烯和脱落酸;d:试管苗的生长发育不需要光照
B.a:用花药离体培养法获得二培体植株;b:通过减数分裂产生愈伤组织;c:培养基中至少应有生长素和细胞分裂素;d:试管苗的生长发育不需光照
C.a:用花药离体培养法获得单体植株;b:通过有丝分裂产生愈伤组织;c:培养基中至少应有生长素和细胞分裂素;d:试管苗的生长发育需要光照
D.a:用花药离体培养法获得二倍体植株;b:通过有丝分裂产生愈伤组织;c:培养基中至少应有乙烯和脱落酸;d:试管苗的生长发育需要光照
4.D、d与T、t都是同源染色体上的等位基因,在不同情况下,符合叙述中因果关系的选项为
A.进行独立遗传的DDTT与ddtt杂交,F2中得到具双显性性状且稳定遗传的个体比例为9/16
B.D与t连锁,d与T连锁,两个具相对性状的纯合体杂交,其F2表现型比为1:2:1
C.将基因型为DDtt的桃树枝条嫁接到基因型为ddTT的植株上,自花传粉后,所结果实的基因型为DdTt
D.后代表现型比为1:1:1:1的两个亲本,基因型一定为DdTt和ddtt
5.1987年,美国科学家将萤火虫的萤光素基因转入烟草植物细胞,获得高水平的表达。长成的植物通体光亮,堪称自然界的奇迹。这一研究成果表明:
①萤火虫与烟草植物的DNA结构基本相同 ②萤火虫与烟草植物共用一套遗传密码
③烟草植物体内合成了萤光素 ④萤火虫和烟草植物合成蛋白质的方式基本相同
A.①和③ B.②和③ C.①和④ D.①②③④
6.NA表示阿伏加德罗常数,下列说法正确的是:
①标准状况下,NA个水分子所占体积约为22.4升 ②常温、常压下,22·4升N2所含的分子数小于NA个 ③在1mol Fe3O4中加入足量硝酸,反应中电子转移的总数为8/3 NA个 ④在标准状况下,Cl2和H2的混合气22·4升,光照后原子总数约为2NA个
A.①②③ B.②③④ C.①③④ D.②④
7、下列反应的离子方程式正确的是
A.次氯酸钙溶液中通入过量二氧化碳 Ca2++2ClO-+H2O+CO2 CaCO3↓+2HClO
B.硫酸亚铁溶液中加过氧化氢溶液 Fe2++2H2O2+4H+
Fe 3++4H2O
C.用氨水吸收少量二氧化硫NH3·H2O+SO2
NH4++HSO3—
D.将1mL~2mL氯化铁饱和溶液加到20mL沸水中:Fe3++3H2O Fe(OH)3(胶体)+3H+
8.X、Y、Z为短周期元素,X原子最外层只有一个电子,Y原子的最外层电子数比内层电子总数少4,Z的最外层电子数是内层电子总数的3倍。有关下列叙述正确的是
A.X肯定为碱金属元素
B.稳定性:Y的氢化物>Z的氢化物
C.X、Y两元素形成的化合物可能为离子晶体
D.Y、Z两元素形成的化合物熔点较高
9.2004年10月13日有关媒体报道天津巨能化学有限公司生产的巨能钙含有双氧水,经农业部产品质量监督检验测试中心检测,部分送检品种不同程度地含双氧水。双氧水属于危险化学品及有毒有害物质,以前也曾作为漂白剂、杀菌剂、防腐剂广泛用于食品中。下列有关H2O2的叙述中正确的是
A.H2O2是二元弱酸,将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失,一定是因为发生了酸碱中和反应
B.H2O2分子中含有非极性键,因此H2O2是非极性分子
C.H2O2的自然分解过程非常缓慢,一般不易察觉,但正因为如此,一般药用的双氧水在贮存期间也会逐渐失效
D.人体中含有过氧化氢酶,过氧化氢酶可以使H2O2分解,因此人体即使吸收多量的H2O2也没有关系,可以被过氧化氢酶分解为无毒物质
10.进行化学实验时必须要有安全意识。下列做法错误的是
A.被玻璃割伤手后,先取出伤口里的碎玻璃片,再用稀双氧水擦洗,然后敷药包扎
B.苯酚沾在皮肤上应立即用酒精擦洗
C.温度计摔坏导致水银散落到地面上,应立即用水冲洗水银
D.酒精灯碰倒洒出酒精着火,迅速用湿抹布扑盖
11.下列说法正确的是
A.淀粉和纤维素均可以有(C6H10O5)n表示,因此它们互为同分异构体
B.17g羟基中所含电子的物质的量为9mol
C.铁位于元素周期表中第四周期第ⅧB族
D.氨、塑料和橡胶都是以石油化工为基础的三大合成材料
12.2003年10月15日我国成功发射了第一艘载人航天飞船-“神州五号”。从此我国进入了航天大国和航天强国行列。发射“神五”用肼(N2H4)作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。
 已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7 kJ/mol。
已知:N2(g)+2O2(g)=2NO2(g);△H=+67.7 kJ/mol。
N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-534 kJ/mol。下列关于肼和NO2反应的热化学方程式中,正确的是
A.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l);△H=-1135.7 kJ/mol
B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1000.3 kJ/mol
C.N2H4(g)+NO2(g)=3/2N2(g)+2H2O(l);△H=-1135.7 kJ/mol
D.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g);△H=-1135.7 kJ/mol
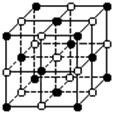
13.KO2的晶体结构与NaCl相似,可以看作是Na+的位置用K+代替,Cl-的位置用O2-代替,下列对KO2晶体结构的描述正确的是
A.和K+距离相同且最近的O2-共有8个
B.和K+距离相同且最近的K+共有12个
C.和K+距离相同且最近的O2-构成的多面体是正八面体
D.和K+距离相同且最近的O2-构成的多面体是正六面
二、本题共8小题,每小题6分,共48分.在每小题给出的四个选项中,有的小题只有一个选项正确,有的小题有多个选项正确.全部选对的得6分,选不全的得3分,有选错或不答的得0分.
14.原子核A发生![]() 衰变后变为原子核
衰变后变为原子核![]() X,原子核B发生
X,原子核B发生![]() 衰变后变为原子核
衰变后变为原子核![]() Y,已知原子核A和原子核B的中子数相同,则两个生成核X和Y的中子数以及a、b、c、d的关系可能是
Y,已知原子核A和原子核B的中子数相同,则两个生成核X和Y的中子数以及a、b、c、d的关系可能是
A.X的中子数比Y少1
B.X的中子数比Y少3
C.如果a – d = 2,则b – c = 3
D.如果a – d = 2,则b – c = 1
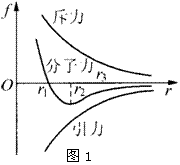
15.如图1所示.甲分子固定在坐标原点O,乙分子位于r轴上,甲、乙两分子间作用力与距离关系的函数图象如右图。现把乙分子从r3处由静止释放.则
A.乙分子从r3到r1,加速
B.乙分子从r3到r2加速,从r2到r1减速
C.乙分子从r3到r1过程中.两分子间的分子势能先减小后增加
D.乙分子从r3到r1过程中,两分子间的分子势能一直增大
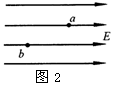
16.如图2所示,在沿水平方向的匀强电场中有a、b两点,已知a、b两点在同一竖直平面但在不同的电场线上。一个带电小球在重力和电场力作用下由a点运动到b点,在这一运动过程中,以下判断中正确的是
A.该带电小球的动能可能不变
B.该带电小球运动的轨迹一定是直线
C.该带小球做的一定是匀变速运动
D.该带电小球在a 点的速度可能为零
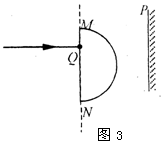
17.如图3所示,半圆形玻璃砖的半径为R,直线MN,一细束白光从Q点垂直于直径MN的方向射入半圆形玻璃砖,从玻璃砖的圆弧面射出后,打到光屏上得到由红到紫的彩色光带。已知QM =![]() 。如果保持入射光线和光屏的位置不变,只使半圆形玻璃砖沿直径方向向上或向下移动,移动的距离小于
。如果保持入射光线和光屏的位置不变,只使半圆形玻璃砖沿直径方向向上或向下移动,移动的距离小于![]() ,则有
,则有
A.半圆形玻璃砖向上移动的过程中,屏上红光最先消失
B.半圆形玻璃砖向上移动的过程中,屏上紫光最先消失
C.半圆形玻璃砖向下移动的过程中,屏上红光最先消失
D.半圆形玻璃砖向下移动的过程中,屏上紫光最先消失
18.在A地用物体m1、B地用物体m2做同样的实验:用竖直向上的力F拉物体,测量物体的加速度a与拉力F间的关系.然后把在两地测得的结果画在同一个a-F图象中,得到如图4所示的加速度a与拉力F的关系图线(A)和(B).若A、B两地的重力加速度分别为g1和g2,由图象可知
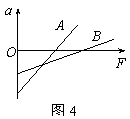 A.m1 > m2 B.m1 < m2
A.m1 > m2 B.m1 < m2
C.g1 > g2 D.g1 < g2
19.神舟六号飞船飞行到第5圈时,在地面指挥控制中心的控制下,由椭圆轨道转变为圆轨道。轨道的示意图如图5所示,O为地心,轨道1是变轨前的椭圆轨道。轨道2是变轨后的圆轨道。飞船沿椭圆轨道通过Q点的速度和加速度的大小分别设为v1和a1,飞船沿圆轨道通过Q点的速度和加速度的大小分别设为v2和a2,比较v2和v2、a1和a2的大小,有
A.v1 > v2,a1 = a2 B.v1 < v2,a1 = a2
C.v1 < v2,a1≠a2 D.v1 > v2,a1≠a2
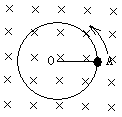
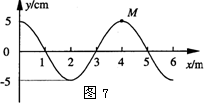
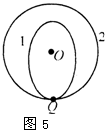
图6
20.在光滑绝缘水平面上,一轻绳拉着一个带电小球绕竖直方向的轴,在匀强磁场中做逆时针的匀速圆周运动,磁场方向竖直向下,其俯视图如图6所示,若小球运动到A点,绳子突然断裂,关于小球在绳断后可能的运动情况是
A.小球仍做逆时针匀速圆周运动,半径不变
B.小球仍做逆时针匀速圆周运动,半径减小
C.小球做顺时针匀速圆周运动,半径不变
D.小球做顺时针匀速圆周运动,半径减小
21.如图7所示是一列简谐横波t = 0时刻的图象,质点M位于波峰位置.经过Δt = 0.4 s时间,第一次重复出现图示的波形.根据以上信息,下列说法正确的是
A.t = 0.2 s时刻质点M的速度最大
B.波的传播速度的大小v = 10 m/s
C.Δt = 1 s时间内质点M经过的路程是25 cm
D.Δt = 1 s时间内质点M经过的路程是10 cm
第II卷(非选择题10题,共174分)
22、(17分)(1)(7分)在“利用单摆测重力加速度”的实验中,测得单摆的摆角小于5O,完成![]() 次全振动的时间为
次全振动的时间为![]() ,用毫米刻度尺测得的摆线长为
,用毫米刻度尺测得的摆线长为![]() ,用螺旋测微器测得摆球的直径为
,用螺旋测微器测得摆球的直径为![]() 。
。
①用上述物理量的符号写出求重力加速度的一般表达式![]() ____________。
____________。
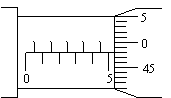
②从图中可知,摆球的直径![]() 的读数为_______
的读数为_______![]() 。
。
 ③实验中有个同学发现他测得的重力加速度的
③实验中有个同学发现他测得的重力加速度的
值总是偏大,其原因可能是下述原因中的______。
A.悬点未固定紧,振动中出现松动,使摆线增长了
B.单摆所用的摆球质量太大
C.把![]() 次全振动的时间误作为
次全振动的时间误作为![]() 次全振动的时间
次全振动的时间
D.以摆线长作为摆长来计算
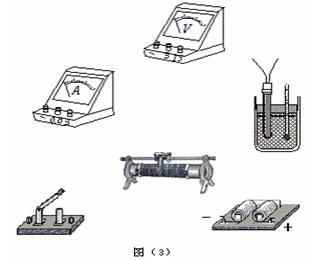
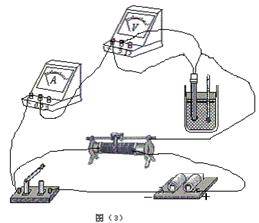
(2)(10分)热敏电阻是传感电路中常用的电子元件.现用伏安法研究热敏电阻在不同温度下的伏安特性曲线,要求特性曲线尽可能完整.已知常温下待测热敏电阻的阻值约40~50Ω.热敏电阻和温度计插入带塞的保温杯中,杯内有一定量的冷水,其它备用的仪表和器具有:盛有热水的热水瓶(图中未画出)、电源(3V、内阻可忽略)、直流电流表(内阻约1Ω)、直流电压表(内阻约5kΩ)、滑动变阻器(0~10Ω)、开关、导线若干.
⑴图(1)中a、b、c三条图线能反映出热敏电阻伏安特性曲线的是 .
⑵在图(2)的方框中画出实验电路图,要求测量误差尽可能小.
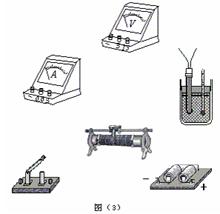 ⑶根据电路图,在图(3)的实物图上连线.
⑶根据电路图,在图(3)的实物图上连线.

23.(17分)一列货车以8m/s的速度在铁路上行驶,由于调度事故,在大雾中后面600m处有一列快车以20m/s的速度在同一轨道上行驶,快车司机赶快合上制动器,但快车要滑行2000m才停下来,请判断两车会不会相撞?
 24.(20分)如图17所示,光滑水平地面上停着一辆平板车,其质量为2m,长为L,车右端(A点)有一块静止的质量为m的小金属块.金属块与车间有摩擦,与中点C为界, AC段与CB段摩擦因数不同.现给车施加一个向右的水平恒力,使车向右运动,同时金属块在车上开始滑动,当金属块滑到中点C时,即撤去这个力.已知撤去力的瞬间,金属块的速度为v0,车的速度为2v0,最后金属块恰停在车的左端(B点)。如果金属块与车的AC段间的动摩擦因数为
24.(20分)如图17所示,光滑水平地面上停着一辆平板车,其质量为2m,长为L,车右端(A点)有一块静止的质量为m的小金属块.金属块与车间有摩擦,与中点C为界, AC段与CB段摩擦因数不同.现给车施加一个向右的水平恒力,使车向右运动,同时金属块在车上开始滑动,当金属块滑到中点C时,即撤去这个力.已知撤去力的瞬间,金属块的速度为v0,车的速度为2v0,最后金属块恰停在车的左端(B点)。如果金属块与车的AC段间的动摩擦因数为![]() ,与CB段间的动摩擦因数为
,与CB段间的动摩擦因数为![]() ,求
,求![]() 与
与![]() 的比值.
的比值.
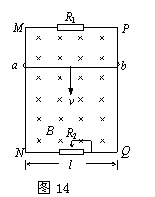 25.(18分)图14中MN和PQ为竖直方向的两平行长直金属导轨,间距l为0.40m,电阻不计。导轨所在平面与磁感应强度B为0.50T的匀强磁场垂直。质量m为6.0×10-3kg.电阻为1.0Ω的金属杆ab始终垂直于导轨,并与其保持光滑接触。导轨两端分别接有滑动变阻器和阻值为3.0Ω的电阻R1。当杆ab达到稳定状态时以速率v匀速下滑,整个电路消耗的电功率P为0.27W,重力加速度取10m/s2,试求速率v和滑动变阻器接入电路部分的阻值R2。
25.(18分)图14中MN和PQ为竖直方向的两平行长直金属导轨,间距l为0.40m,电阻不计。导轨所在平面与磁感应强度B为0.50T的匀强磁场垂直。质量m为6.0×10-3kg.电阻为1.0Ω的金属杆ab始终垂直于导轨,并与其保持光滑接触。导轨两端分别接有滑动变阻器和阻值为3.0Ω的电阻R1。当杆ab达到稳定状态时以速率v匀速下滑,整个电路消耗的电功率P为0.27W,重力加速度取10m/s2,试求速率v和滑动变阻器接入电路部分的阻值R2。
26.(15分) t℃时,将3molA和1molB气体通入容积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g)![]() xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol·L-1。请填写下列空白:
xc(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol·L-1。请填写下列空白:
⑴从反应开始到平衡状态,生成C的平均速率为: ;
⑵x== ;
⑶若向原平衡混合物的容器中再充入amolC,在t℃时达到新的平衡,此时B的物质的量为n(B)== mol;
⑷保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡向右移动的是 。
A. 均减半 B. 均加倍 C. 均增加0.4mol D. 均减少0.4mol
⑸如果上述反应在相同温度和容积的容器中进行,起始加入3molA和3molB,达到平衡时A的体积分数为a%,其它条件不变时,按下列配比作为起始物质,平衡时A的体积分数大于a%的是 (填字母)。
A. 2mol B. 1molA、3molB和4molC
C. 1molB和4molC D. 6molA和2molB
27.(15分)根据实验室中测定硫酸铜晶体结晶水含量的实验,填写下列空白。
(1)从下列仪器选出所需仪器(用标号字母填写)
A.托盘天平(带砝码) B.研钵 C.试管夹 D.酒精灯 E.蒸发皿
F.玻璃棒 G.坩埚 H.干燥器 I.石棉网 L三脚架
除上述仪器外,还需要的仪器是_____________
(2)加热前应将晶体放在__________中研碎,加热是放在__________中进行,加热失水后,应放在__________中冷却。
(3)判断是否完全失水的方法是_________________________________。
(4)做此实验,最少应进行称量操作_________次
(5)下面是某学生一次实验的数据,请完成计算,填入下面的表中。
| 坩埚质量 | 坩埚与晶体 总质量 | 加热后坩埚与 固体总质量 | 测得晶体中 结晶水个数 |
| 11.7g | 22.7g | 18.6g |
(6)这次实验中产生误差的原因可能是________(填写字母)所造成。
(A)硫酸铜晶体中含有不挥发性杂质 (B)实验前晶体表面有湿存水
(C)加热时有晶体飞溅出去 (D)加热失水后露置在空气中冷却
28.(14分) 2005年诺贝尔化学奖由法国科学家YvesChauvin、美国科学家RobertH.Orubbs、 RichardR.Schrock共同获得。以表彰他们在烯烃复分解反应方面研究与应用所作出的贡献。已知烯烃的交叉复分解反应机理为双键断裂,换位连接。可表示为:
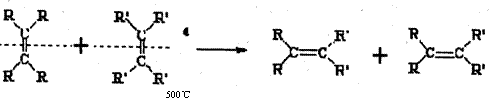 |
![]() 又已知:R-CH2-CH=CH2+Cl2
R-CH Cl –CH=CH2+HCl
又已知:R-CH2-CH=CH2+Cl2
R-CH Cl –CH=CH2+HCl
有机物R是烃的含氧衍生物,分子式为C9H14O6,常用作纤维的增塑剂以及化妆品等,F也可由油脂水解得到,有机物R的合成路线如下:
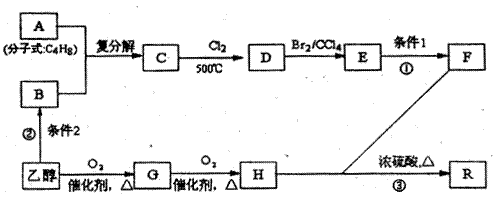
试回答下列问题
⑴写出反应①、②的反应条件:条件1 ;条件2 。
⑵写出结构简式,A: ;E: 。
⑶写出反应③的化学方程式: 。
29.(16分)已知C、D、F、I均为常见气体,E为常见金属,G溶液蒸干并灼热得红棕色粉末H,I是一种能导致温室效应的气体,B由三种元素组成三它们有如下框图关系:
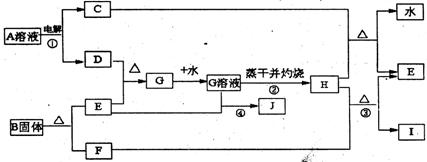
试回答下列问题
⑴反应①阳极的电极反应式 。
⑵反应③的化学方程式 。
⑶反应④的离子方程式 。
 ⑷反应②蒸发至于并灼烧最终得H而不是无水的G,试用文字和方程式简述其理由:
⑷反应②蒸发至于并灼烧最终得H而不是无水的G,试用文字和方程式简述其理由:
。
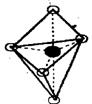
⑸已知B的结构为三角双锥(如右图示),图中○代表F分子,● 代表E原子,写出B的化学式 。
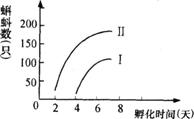
30.(18分)以下图表是某校生物课外科技活动小组人工孵化蛙卵的实验记录。
| 项目 组别 | 水源 | 水量 | 水温 | 水深 |
|
| I | 自来水 | 500ml | 13℃ | 10cm | 300 |
| Ⅱ | 池塘水 | 500ml | 25℃ | 5cm | 300 |
分析以上图表中的数据,回答下列问题:
(1)孵化率相对较低的一组是 。你认为该组
孵化率较低的三条原因是:
①
②
③
(2)利用所孵化的蝌蚪,再提供玻璃缸两只、甲状腺激素制剂少量、池水及蝌蚪饲料,请你设计一个实验,说明甲状腺激素具有促进幼小动物发育的作用。
第一步:将两个玻璃缸分别贴上标签甲、乙,分别放入等量的池水和蝌蚪。
第二步:
……
(3)在(2)所述实验中,你认为对蝌蚪的选择应注意哪些问题?
31.(24分)(1)资料显示,近10年来,PCR技术(聚合酶链反应)成为分子生物学实验室的一种常规实验手段,其原理是利用DNA半保留复制的特性,在试管中进行DNA的人工复制(如下图),在很短的时间内,将DNA扩增几百万倍甚至几十亿倍,使实验室所需的遗传物质不再受限于活的生物体。请据图回答:
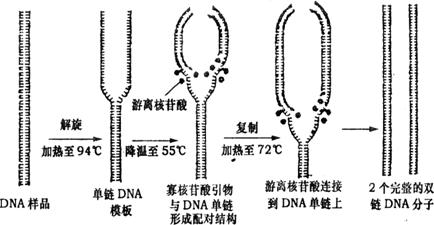
①加热至94℃的目的是使DNA中的 键断裂,这一过程在细胞内是通过
的作用来完成的。
②综合PCR技术与人体细胞内DNA合成过程可知,二者的必需条件中,除了模板、原料、ATP、酶以外,至少还有3个是 。
③PCR技术不仅为遗传病的诊断带来了便利,而且改进了检测细菌和病毒的方法。若要检测一个人是否感染了艾滋病毒,你认为可用PCR技术扩增他血液中的( )
A.白细胞DNA B.病毒的蛋白质 C.血浆中的抗体 D.病毒的核酸
(2)工业上常用发酵罐生产淀粉酶,现用发酵罐研究不同糖类对于微生物产生淀粉酶的影响,实验中,pH值维持在7—8之间,其它条件保持稳定,测定淀粉酶的产量(相对值),
结果如下表
| 糖的来源 | 淀粉酶产量(相对值) |
| 玉米淀粉 | 235 |
| 麦芽糖 | 179 |
| 葡萄糖 | 52 |
| 蔗糖 | 17 |
| 乳糖 | 0 |
| 不含糖 | O |
①关于糖类的种类对微生物产生淀粉酶影响,根据上述结果,你能得出什么结论?
②进一步研究酸碱度对于微生物淀粉酶产量的影响,只用一种糖类进行实验,结果如下表
| pH | 淀粉酶产量(相对值) |
| 6.0 | 0 |
| 6.5 | 4 |
| 7.0 | 13 |
| 7.5 | 18 |
| 8.0 | 14 |
| 8.5 | 11 |
你认为本实验中使用哪种糖类最合适?酸碱度又是如何影响微生物产生淀粉酶的?
2006届永嘉二中高三第二次周考
理科综合能力测试答题卷
第I卷(选择题,共21题,共126分)
一、 本题共13小题,每小题6分,共78分.
| 1 | 2 | 3 | 4 | 5 |
|
|
|
|
|
|
|
|
|
|
|
|
| 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
|
|
|
|
|
|
|
|
|
二、本题共8小题,每小题6分,共48分
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 |
|
|
|
|
|
|
|
|
|
第II卷(非选择题10题,共174分)
22(17分)(1)① 、② 、③
 (2) ①
(2) ①
② ③

23、(17分
24(20分
25、(18分
26、(15分⑴、 ⑵、
⑶、 ⑷、
⑸、
27、(14分(1) (2)
(3) (4)
(5)
(6)
28、(15分(1) 、
(2) 、
(3)
29、(16分)(1)
(2)
(3)
(4)
(5)
30、(18分)(1)
①
②
③
(2)
(3)
31.(24分)(1)① ;
② 。 ③
(2)①
②
2006届永嘉二中高三第二次周考
理科综合能力测试答参考答案
第I卷(选择题,共21题,共126分)
二、 本题共13小题,每小题6分,共78分.
| 1 | 2 | 3 | 4 | 5 |
|
|
|
| C | C | C | B | D |
|
|
|
| 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 |
| D | D | C | C | C | B | D | C |
二、本题共8小题,每小题6分,共48分
| 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 |
| AC | A | AC | D | BC | B | ACD | B |
第II卷(非选择题10题,共174分)
22(1)①![]() (3分)、②
(3分)、②![]() (2分)、③C(2分)
(2分)、③C(2分)
 (2) ① c (2分)
(2) ① c (2分)
②如答图2 (4分)
|
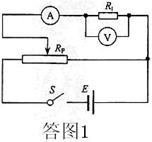
(3)如答图3所示.(4分)
23.快车刹车后的加速度大小为![]() ①
①
当两车速度相等时,![]() ②
②
快车多走距离为
![]() ③
③
或![]()
故两车将相撞。
参考评分:①4分②5分③8分
24.解析:设水平恒力F作用时间为t1.
对金属块使用动量定理Fμt1=mv0-0即: μ1mgt1=mv0 ①
得t1=![]() ②
②
对小车有(F-Fμ)t1=2m×2v0-0,得恒力F=5μ1mg ③
金属块由A→C过程中做匀加速运动,加速度a1=![]() =
=![]() ④
④
小车加速度![]() ⑤
⑤
金属块与小车位移之差![]() ⑥
⑥
而![]() ,∴
,∴![]() ⑦
⑦
从小金属块滑至车中点C开始到小金属块停在车的左端的过程中,系统外力为零,动量守恒,设共同速度为v,由2m×2v0+mv0=(2m+m)v,得v=![]() v0. ⑧
v0. ⑧
由能量守恒有![]() ⑨
⑨
得![]() ⑩
⑩
∴![]()
参考评分:各式1分、结果错扣2分
25、解析:对ab棒由能量守恒定律得: mgv=P ①
代入数据得:v=4.5m/s ②
又 E=BLv ③
设电阻R![]() 与R
与R![]() 的并联电阻为R
的并联电阻为R![]() ,ab棒的电阻为r,有
,ab棒的电阻为r,有
![]() ④
④
![]() ⑤
⑤
P=IE ⑥
由②③④⑤ 代入数据得:![]() =6.0Ω.
=6.0Ω.
参考评分:各式3分,结果错扣2分
26.①0.2mol/l*min② 4 ③0.8+0.2a④ n(A): (B)=3:1 n(C)≧0
27. (1)A、B、D、F、G、H、L,坩埚钳、泥三角、药匙
(2)研钵;坩埚;干燥器。 (3)最后一次加热前后两次质量数据差不超过0.1g。
(4)4 (5)5.3 (6)B、C
28.⑴氢氧化钠水溶液,加热;浓硫酸,170℃(加热)
⑵CH3CH=CHCH3;CH2C1CHBrH2Br
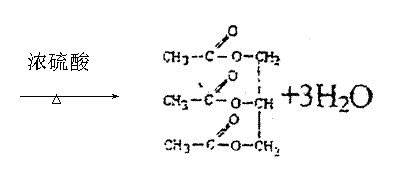 ⑶3CH3COOH+CH2OHCHOHCH2OH
⑶3CH3COOH+CH2OHCHOHCH2OH
29.
|
⑶2Fe3++Fe=3Fe2+
|
⑸Fe(CO)5或者FeC5O5
30.(1)1 ①自来水中的Cl2、HClO对蛙胚有毒害作用 ②温度太低导致酶活性降低 ③水太深,氧供应不足
(2)(第二步)在甲缸中加入少量甲状腺激素制剂,乙缸中不加,作为对照(第三步)每天投喂适量饲料,做好观祭和记录
(3)所选蝌蚪应是同一批孵化出来的,且个体大小相近,健康活泼
31.(1)①氢;解旋酶 ②一定温度、适宜的pH、水环境 ③D
(2)①在以多糖为原料的情况下,产生的淀粉酶多,单糖和二糖都不理想。②淀粉;在微碱性环境中(如表中pH=7.5时)产生淀粉酶最多;酸性环境下产生的淀粉酶相对较少;碱性环境下产生的淀粉酶相对较多。
 蛙卵数
蛙卵数