九年级科学第二学期中考模拟卷
考生须知:
1、 全卷满分为200分,考试时间120分钟。有4大题,38小题。
2、 本卷答案必须做在答题卷的相应的位置上,做在试题卷上无效。
温馨提示:请仔细审题,细心答题,相信你一定会有出色的表现!
(可能用到的相对原子质量:H 1;C 12 ;O 16;S 32;N 14; Li 7;K39)
试卷I
一、 选择题(本题20小题,每小题4分,共80分。请选出各题中一个符合题意的正确选项,不选、多选、错选,均不给分)
1.2008年的北京奥运会倡导“绿色奥运”,绿化城市、绿色生活、绿色消费、人与自然和谐发展。下列不符合“绿色”理念的是( )
A、人走不忘关灯;手洗不忘关水龙头 B、用电子贺卡代替纸质贺卡
C、尽量少用一次性筷子、塑料袋等物品 D、废旧电池没用扔掉
2.嘉兴市城区有些小区已开始使用“西气东输”工程送来的天然气。天然气的主要成分是CH4。下列四位同学在讨论化学式CH4的意义,其中错误的是 ( )

3.“小时不识月,呼作白玉盘”中描述的月相是( )
A、新月 B、上弦月 C、满月 D、下弦月
4.我国于2006年1月1日开始实施《可再生能源法》。这部法律不仅向人们显示了可再生能源对于未来社会生活的重大意义,同时,也为可再生能源未来的发展指出了更明确的方向.下列不属于“可再生能源”的是 ( )
A、风能 B、海洋能 C、太阳能 D、石油
5.在一座小山上,生长着许多草、树木、鸟、昆虫、蛇、细菌等生物,它们与其生存环境组成了( )
A、生物群落 B、生态因素 C、生态系统 D、生物种群
6.同学们放学骑自行车回家,下坡时即使停止蹬车,车速也会越来越快,这是因为人和自行车的( )
A、机械能越来越大 B、惯性越来越大
C、重力越来越大 D、重力势能转化为动能
7.下列关于ABO血型系统中的叙述错误的是( )
A、ABO血型系统的血型由红细胞上的凝集原决定的
B、一个人的血型是由遗传决定的,且终生不变
C、红细胞上的凝集原有两类∶A凝集原和B凝集原
D、在O型血的血清中没有抗A;抗B凝集素
8.下列实验操作中,不正确的是( )

9.学习了自然科学的知识后,小林同学对与人身体相关的科学知识很关注,并进行了估测,以下估测中合理的是 ( )
A、他自身所受的重力为50牛 B、步行速度约为10米/秒
C、吃饭后半小时,血糖浓度约为0.11% D、人体电阻值约为几十欧
10.人类认识黑洞,最有可能了解到的事实是( )
A、 黑洞附近的恒星可能会受黑洞引力的影响而有特别的分布
B、 用射电望远镜看到黑洞
C、 航天探测器近距离接近黑洞
D、黑洞发出的光被我们接受收到
11.我国西北一些地区,如内蒙古,过去是“天苍苍,野茫茫,风吹草低见牛羊”,现在是“天苍苍,野茫茫,老鼠跑过露脊梁”,其主要原因是( )
A、水资源利用不合理 B、全球气温升高 C、过度放牧、盲目开垦 D、酸雨
12.现有六种物品:铁钉、玻璃、铅笔心、水银、橡胶棒、陶瓷片.小明将它们分成两类,如下表所示.则小明是按照物质的哪种物理特性进行分类的 ( )
| 第一类 | 第二类 |
| 铁钉 铅笔芯 水银 | 玻璃 橡胶棒 陶瓷片 |
A、密度 B、磁性 C、硬度 D、导电性
 13.在探究凸透镜成像规律的实验中,当烛焰、凸透镜、光屏
13.在探究凸透镜成像规律的实验中,当烛焰、凸透镜、光屏
处于如图所示的位置时,恰能在光屏上得到一个清晰的像。
利用这一成像原理可以制成( )
A、照相机 B、幻灯机 C、放大镜 D、望远镜
14 .下表为某地在一次连续四天降水中,测得空气中二氧化硫浓度和降水pH值的数据。
析表中数据可知,这次降水中遭受酸雨污染较重的是
| 日期 | 第一天 | 第二天 | 第三天 | 第四天 |
| SO2(mg/m3) | 0.009 | 0.013 | 0.015 | 0.018 |
| pH | 5.55 | 5.36 | 4.78 | 4.42 |
A.、第一天 B、.第二天 C、第三天 D.、第四天
15.近年来,禽流感作为一种高致病性传染病,对人类产生很大的威胁。在尚未研制出相关疫苗和特效药的情况下,下面做法中最合理的是( )
A、放弃遍布各地的农村散养方式,改为大规模的工业化养殖方式。
B、善待家禽,尊重动物的生命权,与其和谐相处。
C、消灭所有的通过本市的迁徙候鸟,并禁止养殖家禽和观赏鸟。
D、加强卫生管理,强化家禽检疫及疫点扑杀、消毒。
16.以下是被媒体暴光的一些商家的不法欺诈行为,其中涉及化学变化的是( )
A、工业石蜡给水果上蜡美容 B、淀粉掺人奶粉制造劣质奶粉
C、工业酒精兑水制假酒 D、用硫磺熏白木耳
 17.如图所示是奥运会赛艇比赛的场景,赛艇的桨可看成一个杠杆。若把杠杆按省力杠杆、等臂杠杆和费力杠杆进行分类,赛艇的桨属于( )
17.如图所示是奥运会赛艇比赛的场景,赛艇的桨可看成一个杠杆。若把杠杆按省力杠杆、等臂杠杆和费力杠杆进行分类,赛艇的桨属于( )
A.省力杠杆 B.费力杠杆
C.等臂杠杆 D.无法确定
18.下列某物质在氧气中充分燃烧后,将生成物依次通过浓硫酸和氢氧化钠固体,经测定,它们增重的质量之比为9∶11。则该物质是( )
A、C2H5OH B、CH4 C、H2 D、CO
19 .AB导体作如图所示的运动,下述各种情况会产生感应电流的是 ( )
 |
20.甲、乙、丙、丁四位同学设计了下列有关物质鉴别的方案:
甲:利用CO2气体就能区分NaOH、Ca(OH)2和稀盐酸三种溶液;
乙:若有BaCl2溶液,就有办法鉴别NaOH、Na2C03、Na2S04和硫酸四种溶液;
丙:有酚酞和BaCl2溶液,就能鉴别盐酸、硫酸、Na2C03、NaOH和KN03五种溶液;
丁:不用其它任何试剂就能将HCl、BaCl2、Na2C03、NaCl四种溶液鉴别出来。
下列有关这些方案的评价正确的是( )
A、只有甲的可行 B、只有乙和丁的可行
C、只有乙的不可行 D、都可行
试卷II
二、简答题(本大题有20个空格,每空3分,共60分)
21.“月落乌啼霜满天,江枫渔火对愁眠.姑苏城外寒山寺,夜半钟声到客船”.从科学角度看.诗中的“月落”是以________作为参照物的,“钟声”是由钟的________所产生的.
22.下表中列出了空气、NH3(氨气)、CH4、HCl四种气体在标准状况下的密度和溶解度,回答下列问题:
| 空气 | NH3 | CH4 | HCl气体 | |
| 密度(g/mL) | 1.293 | 0.771 | 0.717 | 1.629 |
| 溶解性 | — | 极易溶 | 极难溶 | 极易溶 |

(1)其中,既可用排水法收集,又可用向下排空气法收集的气体是 ;
(2)若用右上图装置除去氢气中混有的HCl气体,则装置内应装的试剂为 。
23.下图所示曲线分别表示人体血液中O2和CO2含量的变化情况。请据图回答:
(1) ![]()
 血液流过B段毛细血管时,血液中氧气分子
血液流过B段毛细血管时,血液中氧气分子
与血 红蛋白迅速_________(分离或结合)。
(2) 你认为B段毛细管是肺泡毛细血管还是组织
内的毛细血管?_________ 。
24.蛋白质的机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应,生成氨基酸。蛋氨酸(化学式为C5H11O2NS)就是其中的一种。请回答下列问题。
⑴蛋氨酸中各元素的质量比C∶H∶O∶N∶S = ;
⑵蛋氨酸中氮元素的质量分数为 ;
⑶合格奶粉每100克含蛋白质约18克,蛋白质中氮元素的平均质量分数为16%,则每100克合格奶粉中氮元素的质量为 克;现测定某奶粉每100克中含有氮元素0.5克。则这种奶粉属于 (填“合格”或“不合格”)奶粉。
25.嘉兴地处浙东沿海夏天,由于海洋上的水的比热比内陆砂土比热大,海洋上空的气温比内陆上空的气温______,海洋上空的气压比内陆上空的气压_________,风从海洋吹向陆地,形成东南季风。
 26.某同学将在黑暗中放置了24小时的两盆植物,分别移置在透明、密闭的玻璃装置中(如图甲、乙示),再放在阳光下照射4小时。然后各取一张叶子,
26.某同学将在黑暗中放置了24小时的两盆植物,分别移置在透明、密闭的玻璃装置中(如图甲、乙示),再放在阳光下照射4小时。然后各取一张叶子,
经酒精煮沸脱色后滴碘液检验。
⑴结果 。
⑵此实验可证明 是光合作用所需要的原料。
27.鉴别失去标签的硝酸钡、碳酸钾和稀盐酸三种无色溶液。
(1)学生得知氯化钡溶液显中性,碳酸钾溶液显碱性,稀盐酸显酸性,选用了一种指示剂;学生B选用了一种酸;学生C选用了一种含钠的正盐溶液。三位同学都一次鉴别成功。请你想一想并写出他们选用的试剂:A ,B ,C 。
(2)学生D认为不用其他试剂也可以鉴别。请你根据学生D可能采用的实验方案写出一个有关的化学方程式 。
28.2003年月15日晚02时00分,我国载人航天试验飞船“神舟”五号用“长征二号——运载火箭发射成功。飞船在太空飞行时.各物体处于“失重”(没有受到重力)状态。
(1)载人试验飞船的返回舱中有许多植物种子,将这些物种带上天再回来的目的是决
定生物性状的 发生变化,从而培育出新品种。
(2)在太空舱内,宇航员拟开展下列实验,其中不能完成的是 (填字母)
A、用温度计测温度 B、用显微镜观察叶绿体
C、在水中溶解食盐 D、用漏斗、滤纸过滤除去水中的泥沙
三、实验探究题(本大题有15个空格,每空2分,共30分)
29.右图所示,是某校研究性学习小组的同学模拟池塘生态系统制作的一个封闭生态瓶(瓶中生物生长良好),请据图回答:
(1)该生态瓶中属于生产者的是 。
(2)该生态瓶放置在明亮的窗台上(天气晴朗并不 采用其它光源),那么生态瓶中早晨时水溶液的PH (填“>”或“=”或“<”)傍晚时水溶液的PH。

30.小明所设计的“估测大气压的值”的实验方法下:
①把注射器的活塞推至注射器筒的底端,然后用—橡皮帽封住注射器的小孔;
②如图所示,用细尼龙绳拴住注射器活塞的颈部,
绳的另一端与固定在墙上的弹簧测力计的挂钩相连,
然后水平向右慢慢地拉动注射器筒. 当注射器中的活塞
刚开始移动时,记下弹簧测力计的示数F;
③观察并记录注射器筒上所标明的容积V,用刻度尺测出
注射器的全部刻度长度L.
(1)根据以上实验方案,用测得和记录的物理量计算大气压强的表达式应为________。
(2)按照上述实验方案测得的大气压强的值,往往会比大气压强的实际值偏小.你认为产生这种现象的原因是: _________________________________________。
31.某同学做了“用双氧水和二氧化锰制氧气”的实验后,展开了下面的思考与探究
双氧水溶液的溶质质量分数对反应速率有没有影响呢?
他做了一组实验:每次均取5ml30%的双氧水溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:(实验均在20℃室温下进行,其他条件相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 双氧水溶液的 溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2 粉末的 质量(克) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集500 ml气体 所用的时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后溶液的温度(℃) | 24 | 34 | 39 | 65 | 70 | 79 | 85 | 90 |
请发现表中的数据回答:
(1)双氧水溶液的溶质质量分数对反应速率有没有影响呢?
如果有,是怎样影响呢? 。
(2)还有哪些因素可能影响该反应速率呢?请你说出一个猜想:
。
(3) 同学在室温中要收集5L,需要多少克30%的双氧水溶液(20℃室温中氧气的密度为1.4 克/升,计算最后结果精确到0.01,)
。
同学在室温中要收集5L,需要多少克30%的双氧水溶液(20℃室温中氧气的密度为1.4 克/升,计算最后结果精确到0.01,)
。
32.如图所示,物体重200牛,物体与地面的摩擦力为50牛
,在力F=30牛的作用下物体在水平地面做匀速直线运动,V=0.2米/秒,
则该装置的机械效率为______;拉力F做功的功率为_______瓦特。
33.以下表格是某同学关于酶的特性的实验操作步骤。碘液滴入后可观察到乙试管内的试剂变蓝色。
| 步骤 | 项 目 | 试 管 | |
| 甲 | 乙 | ||
| l | 注入1%的淀粉溶液 | 4毫升 | 4毫升 |
| 2 | 注入新鲜稀释的唾液 | 2毫升 | 2毫升 |
| 3 | 放置一定温度下保温5分钟 | 37℃ | 60℃ |
| 4 | 滴加碘液 | 2滴 | 2滴 |
(1)甲试管内 发生了化学变化(填“有”或“没有”)
(2)实验说明了唾液淀粉酶的催化活性受 影响。酶是活细胞制造且有催化
能力的 。
(3)本实验 (选填“有”或“没有”)对照组。
34.现有A、B.两个塑料软瓶,A瓶内装有CO和O2的混合气体,B瓶内装有CO2气体。某同学从野外捉来了两只活蝗虫,分别放入两个塑料软瓶中,拧紧瓶盖。结果,两只蝗虫很快都死了。请根据下面所给选项回答,造成蝗虫死亡的主要原因是:
A瓶 B瓶 。
四、分析计算题(本题有4小题,30题6分,31;32;33题均8分,共30分)
35. .一个体重为500N的同学骑自行车上学,在水平路面上以4m/s的速度匀速行驶. 有关数据如右表所示.
(1)
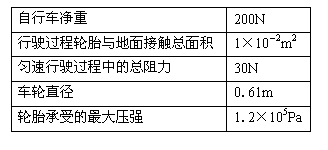 在行驶过程中,车对地面的
在行驶过程中,车对地面的
压强是多大?
(2)该同学骑车沿直线匀速行驶10min
做了多少功?
(3)该同学骑车时的功率多少?
36.汽车电瓶是一种铅蓄电池,在使用一段时间后,常需补充“电瓶水”—30%的硫酸溶液。
(1) 常用的一只蓄电池的电压多少伏?某汽车电瓶由6只铅蓄电池组成,可供汽车灯泡正常工作,已知该灯泡正常工作时的电阻为2.88Ω,则通过小灯泡的电流为多少?
(2)若要配制1kg这种“电瓶水”—30%的硫酸溶液,需要密度为1.84g/ml、98%的浓硫酸多少毫升?需要水多少毫升?
37.当生物体在缺乏空气的条件下腐烂时,会放出一种气体,我们把它称为沼气.沼气通常含有60%的甲烷(CH4),其余的大部分是CO2.沼气是很好的燃料,可用于家庭烹调、取暖和照明,目前我国农村中建造了大量的沼气池产生沼气。据测算,平均每立方米大小的沼气池一天产生沼气量是0.2m3.而每立方米的沼气可以供6口之家三餐的烹调所用,可以使3吨的卡车运行3km,可以点亮60W电灯工作6h.请问:
(1)每立方米的沼气可以产生_____J的能量.
(2)沼气燃烧的主要化学方程是_____.
(3)经研究可知,沼气是甲烷细菌在分解腐烂物质时释放出来的.甲烷细菌属于_____
A、好氧性异养型细菌 B、厌氧性异养型细菌
C、好氧性自养型细菌 D、厌氧性自养型细菌
(4)如果某小山村有30户家庭,生活用电每户平均100W,公共设施及学校用电约1000W.设全村平均每天用电4h.为保证全村的正常用电,至少要建造多大的沼气池才够用?(请通过计算回答,计算过程中不能被整除的,小数点后保留一位小数)。
38.宇宙飞船内,宇航员呼出的气体要通过盛有氢氧化锂的过滤网,以除去所含的二氧化碳,如下式所示:2LiOH(固)+CO2(气)=Li2CO3(固)+H2O(液)
⑴试计算1g氢氧化锂所能吸收的二氧化碳的质量?
⑵若用氢氧化钾来代替氢氧化锂,试计算吸收相同质量的二氧化碳需多少克氢氧化钾?
⑶利用⑴和⑵所得的结果,试解释为什么宇宙飞船选用氢氧化锂来吸收二氧化碳较用氢氧化钾为佳?

(参考答案)
可能用到的相对原子质量:H 1;C 12 ;O 16;S 32;N 14; Li 7;K39
一、 选择题(本题共20小题,每小题4分,共80分。)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| D | C | C | D | C | D | D | B | C | A |
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| C | D | B | D | D | D | B | B | C | D |
二、 简答题(本题有8小题20空格,每空格3分,共60分)
21.地面, 振动。22.CH4,氢氧化钠溶液。
23.(1)结合,(2)肺泡毛细血管。24.(1)60:11:32:14:32,(2)9·4%,(3)3·24(4)合格。
25.底,高 。 26.(1)甲不变蓝;乙变蓝,(2)CO2。
27.(1)石蕊试液,B硫酸,C碳酸钠。(2)BaCl2+K2CO3=Ba CO3+H2O+CO2。
28.(1)基因,(2)D。
三、 实验探究题(本大题有15个空格,每空2分,共30分)
29.(1)绿萍;金鱼藻,(2)<。
30.(1)P=FL/V,(2)针筒中有空气(其他合理答案亦可)。
31.(1)催化剂量相同时,双氧水溶液的溶质质量分数越大反应速率越大,
(2)反应速率可能与双氧水溶液的温度有关,(3)49·58。
32.(1) 83·3%,(2)__12_______。
33.(1)有_____,(2)_温度______ ,____一类蛋白质_____。(3)__有____ _ 。
34.____CO有毒且与血红蛋白结合的速度比氧气快__, CO2不能供给呼吸___________。
四、分析计算题(本题有4小题,30题6分,31;32;33题均8分,共30)
35.
(1)F= G人+G车 = 500N +200N = 700N
P= F/S = 700N/1×10-2m2 = 70000pa
(2)t=10×60s = 600s
S = vt = 4m/s×600s =2400m
W = Fs = 30N×2400m =7.2×104J
P = W/t = 7.2×104J/600s =120W
36.
(1)2v I = U/R = 12V/2.88Ω =4.17A
(2) m×98% = 1000g×30% m = 306.12g
V = 306.12g/1.84g/ml =166.37ml
V水=(1000g-306.12g)/1g/ml =693.88ml
37.
(1) 1.296×106J
(2) CH4 + O2 点燃 CO2 + H2O
(3)B
(4) t = 4×3600s = 1.44×104s
W = Pt = (30×100W+1000W) ×1.44×104 = 5.76×107J
5.76×107J/1.296×106J/ × 5 m3 = 222.2m3
38.
(1) 2LiOH(固)+CO2(气)=Li2CO3(固)+H2O(液)
48 44
1g x
48/1g = 44/x x=1.09g
2KOH(固)+CO2(气)=K2CO3(固)+H2O(液)
112 44
Y 1.09g
112/y = 44/1.09g y =2.77g
吸收一样多的二氧化碳所需氢氧化锂的质量比氢氧化钾少