塘栖中学2006届高三理科综合训练题(八) 2006-5-24
班级 姓名 学号
杭州市塘栖中学 余晓钟
一、选择题(每小题只有一个选项符合题意)
1、近年来,科学家正在探索利用铝粉作为新能源的可能性,以期铝能成为一种石油的取代物。假如铝作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法,你认为哪项是错误的 ( )
A.铝质轻,便于运输、贮存,且安全
B.铝燃烧时放出的热量大,且燃烧后新产物对环境的污染容易得到有效的控制
C.在地球上,铝矿资源比较丰富
D.现代电冶铝的工业技术已为铝作为新能源奠定了重要基础
2、不具有放射性的同位素称之为稳定同位素,近20年来,稳定同位素分析法在植物生理 学、生态学和环境科学研究中获得广泛应用。如在陆地生态系统研究中,2H、13C、15N、18O、34S等常用做环境分析指示物。下列说法中正确的是( )
A.34S原子核内的中子数为16 B.1H216O在相同条件下比1H218O更易蒸发
C.13C和15N原子核内的质子数相差2 D.2H+的酸性比1H+的酸性更强
3、食物中碲的一个来源是装食物的含锡罐头。通常开罐时约有8毫克金属屑落入食物中,其中含碲0.1%(即8微克)。因此,用塑料包装代替罐头可以防止摄入碲,碲具有内在的毒性,碲可能会包含在酶体系中,与蛋白配合,引起肾和肝退化。碲在元素周期表中的位置是( )
A.第四周期IVA族 B.第五周期IVA族 C.第四周期VIA族 D.第五周期VIA族
4、羟胺(NH2OH)是一种还原剂,能将某些氧化剂还原。现用25.00mL0.049mol/L的羟胺的酸性溶液跟足量的硫酸铁溶液在煮沸条件下反应,生成的Fe2+恰好与24.65mL 0.020mol/L的KMnO4酸性溶液完全作用(已知:FeSO4+ KMnO4+ H2SO4= Fe2(SO4)3+ K2SO4+ MnSO4+ H2O(未配平),则在上述反应中,羟胺的氧化产物是( )
A.N2 B. N2O C.NO D.NO2
5、常温下,有甲、乙两份体积均为1 L,浓度均为0.1 mol·L-1的氨水,其pH为11。甲用蒸馏水稀释100倍后,溶液的pH将为a;乙与等体积、浓度为0.2mol·L-1的HCl混合,在混合溶液中:n(NH4+)+n(H+)-n(OH—)=b mol 。a、b正确的答案组合是( )
A.9~11之间;0.1 B.9~11之间;0.2 C.12~13之间;0.2 D.13;0.1
6、可逆反应N2+3H2![]() 2NH3是一个放热反应。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=4Q1,则甲容器中,H2的转化率为( )
2NH3是一个放热反应。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3 molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2 molNH3,达平衡时,吸收的热量为Q2。已知Q2=4Q1,则甲容器中,H2的转化率为( )
A.20% B.25% C.75% D.80%
7、用电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是( )
A.当电池负极消耗![]() 气体时,电解池阴极有
气体时,电解池阴极有![]() 气体生成
气体生成
B.电解池的阳极反应式为:4OH--4e-==2H2O+O2↑
C.电解后,![]() 不变,且溶液中有晶体析出
不变,且溶液中有晶体析出
D.电池中![]() 不变;电解池中溶液
不变;电解池中溶液![]() 变大
变大
8、要求设计实验证明,某种盐的水解是吸热的,有四位学生分别作出如下回答,其中正确的( )
A.丁学生:在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的
B.甲学生:将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的
C.乙学生:在盐酸中加入相同温度的氨水,若实验过程中混和液温度下降,说明盐类
水解是吸热的
D.丙学生:在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的
二、非选择题
26.(15分)甲、乙、丙、丁分别代表中学化学中常见的物质。根据要求回答下列问题。
(1)甲的化学式为RClx。
① 若甲为某短周期金属元素的氯化物,甲中含有的金属元素的原子半径在同周期金属元素中最小,其阳离子与氖原子有相同的电子层结构。则甲中含有的金属元素是____________;
② 若甲为某金属元素的棕色氯化物,将该氯化物水溶液加热蒸干并灼烧,得到的氧化物为红棕色粉末,则甲的化学式为________________,甲中含有的金属元素在周期表中的位置为___________________;
③ 将上述两种金属中活泼性强的金属与另一种金属的最高价氧化物混合,引燃后可发生剧烈反应,其化学方程式为_________________________________,引燃该反应的实验操作是___________________________________________。
(2)若甲、乙、丙、丁为单质或化合物,均含有某短周期中的同一种元素,常温下甲为气体,将甲通入常温下的KOH溶液中得到乙和丙,丙的水溶液具有强氧化性。
① 电解乙溶液得到甲,该反应的化学方程式为____________________________;
② 在一定条件下1 mol甲与2 mol KOH在溶液中反应得到乙和丁,n(乙) :n(丁)
=5:1,该反应的离子方程式为_____________________________________。
27.(15分)图中A~J分别代表一种反应物或生成物,已知A受热分解得到等物质的量的B、C、D气态物质,图中部分生成物未列出

请回答
(1)B的电子式________,C是__ ___(极性、非极性)分子,D分子的空间构型为__ __。
(2)写出反应①、②的化学方程式
①______________________________________;②_______ ____________________
(3)写出反应③的离子方程式______________________________________________
28、I、下表是如东某超市出售的“淮牌”加碘精制盐的有关说明:
| 产 品 标 准 号 | Q/320000JYJ03-2004 |
| 许 可 证 号 | 食盐批字第100070号 |
| 配 料 表 | 精制盐、碘酸钾 |
| 含 碘 量 | 35±15mg/kg |
| 卫生许可证号 | 东卫食字(2005)第00015号 |
| 分 装 日 期 | 见封口 |
| 储 藏 方 法 | 通风、防潮 |
| 食 用 方 法 | 根据烹调所需适量加入 |
| 食品标签认可号 | 苏食签(2002)007号 |
II、下面是某网站上刊出的有关碘及碘的化合物的有关信息:
自然界中碘主要以碘化物和碘酸盐的形式存在。碘在海水中的含量甚微(5×10-8%),但海洋中某些生物如海带、海藻等具有选择性吸收和聚积碘的能力,因而干海藻是碘的一个重要来源。目前世界上碘主要来自智利硝石,其中含碘0.02%~1%,智利硝石中碘主要以碘酸钠(NaIO3)的形式存在。通常情况下碘是一种紫黑色固体,易升华,只能少量溶于水得棕黄色的碘水溶液,但易溶于苯、四氯化碳等有机溶剂,紫色的碘蒸气有刺激性气味,能强烈刺激眼、耳、鼻、气管等粘膜,吸入较多的碘蒸气会发生中毒,甚至造成死亡。碘遇淀粉(面粉的主要成分)会出现明显的蓝色。碘离子(I-)具有明显的还原性,而高价态的碘则具有较强的氧化性:
2NaI+3H2SO4+MnO2=2NaHSO4+MnSO4+2H2O+I2 …………⑴
2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2 …………⑵
反应⑴是自海藻灰中提取碘的主要反应,反应⑵是自智利硝石中提取碘的主要反应。
根据以上信息,回答下列问题:
⑴反应⑴、反应⑵的离子方程式是(亚硫酸氢钠的电离方程式是:NaHSO3=Na++HSO3-)
反应⑴: ;反应⑵: ;
I2在反应⑴中是 (填“氧化”或“还原”,下同)产物,在反应⑵中是 产物;
⑵请你设计实验探究上述 “淮牌”精制盐中是否真的含有碘元素。
实验名称:探究“淮牌”精制盐中是否含有碘元素
实验目的:1.认识碘酸钾中的碘元素转变成碘单质的化学反应;
2. 。
实验原理:(提示:结合题中信息和实验目的进行分析) 。
实验用品:(提示:实验用品通常包括仪器和药品,根据你设计的实验填写)
。
实验步骤:(用准确、简洁的语言填写下表)
| 实 验 步 骤 | 实验现象 | 化 学 方 程 式 或 实 验 结 论 |
| 固体在水中 溶 解 | ||
| 溶液出现棕 黄 色 | 2IO3-+5HSO3-=3H++5SO42-+H2O+I2 | |
| “淮”牌精制盐中含有碘元素。 |
问题讨论:如东有100多km的海岸线,海产品丰富,海产品中或多或少的含有碘元素,而海产品又是如东人的主要副食品,如东人的食用盐中需要加碘吗?说明你的理由
。
29、(15分)松节油是生产高级香料的重要原料,是绿色可再生资源。
(1)月桂烯是松节油中的常见组分,月桂烯的结构简式为![]() ,也可简写为
,也可简写为![]() ,其分子式是
,可以发生的化学反应有
(选填序号)。
,其分子式是
,可以发生的化学反应有
(选填序号)。
①加成反应 ②消去反应 ③酯化反应 ④氧化反应
(2)下列物质也是松节油中的常见组分。
![]()
![]()
![]()
![]()
柠檬烯 双戊烯 α—水芹烯 对伞花烃
① ② ③ ④
这些物质中,与月桂烯互为同分异构体的是 (选填序号)。
(3)有机物C10H18O是无色油状液体,具有铃兰香气。它的一种合成路线如下所示:
 |
1 mol C2H4O2与适量的碳酸氢钠溶液反应生成二氧化碳22.4 L(标准状况); C10H18O能够使溴的四氯化碳溶液褪色。经测定,C10H18O分子中含有三个甲基(-CH3),其中一个甲基不在分子碳链的两端;C10H18O分子中有一个碳原子连接着四个不同的原子或原子团。请回答下列问题:
①C2H4O2与碳酸氢钠溶液反应的离子方程式是 。
②C10H18O分子所含官能团的名称是 、 。
③有机物C10H17Cl的结构简式是 。
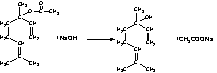
④C12H20O2在氢氧化钠存在条件下水解的化学方程式是
。
6-13 D B D B B A D A
26、
|
③ 2Al+Fe2O3=== 2Fe + Al2O3 (3分,仅条件错得2分)
|
(2)① 2KCl+2H2O====Cl2↑+H2↑+2KOH
(2分,写“电解”可得分,缺条件不得分)
② 3Cl2+6OH—==5Cl—+ClO3—+3H2O (2分)
27、(1)![]() (2分);极性(2分);三角锥形(2分)
(2分);极性(2分);三角锥形(2分)
(2)①![]() (3分)
(3分)
②![]() (3分)
(3分)
(3)![]() (3分)
(3分)
28、⑴2I-+4H++MnO2=Mn2++2H2O+I2
2IO3-+5HSO3-=3H++5SO42-+H2O+I2 氧化 还原
实验目的:2.认识碘单质的检验方法。
实验原理:⑵用NaHSO3还原KIO3生成单质碘,再用淀粉检验碘单质的存在
实验用品:试管、滴管,“淮”牌精制盐、亚硫酸氢钠溶液、淀粉溶液
| 实 验 步 骤 | 实验现象 | 化 学 方 程 式 或 实 验 结 论 |
| 1.取食盐少许于一支试管中,加入适量的水,振荡,使食盐全部溶解 | 食盐及碘酸钾能溶于水 | |
| 2.向上述溶液中滴加适量的亚硫酸钠溶液,振荡 | ||
| 3.再向上述溶液中滴加淀粉溶液。振荡,观察现象 | 溶液变成蓝色 |
问题讨论(只要阐述的理由和得出的结论不矛盾即给分)
29.(1)C10H16 ①④ (2)①③
(3)①CH3COOH+HCO3-===CH3COO-+CO2↑+H2O
②碳碳双键 羟基
③![]() 或
或 ![]()
④ 或
或