新教材化学高考模拟题精编详解第十五套试题
| 题号 | 一 | 二 | 三 | 四 | 总分 |
| 分数 |
说明:本套试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,满分120分.考试时间:90分钟.
可能用到的相对原子质量:Na:23 H:1 O:16 Al:27 Mg:24 Si:28 Ag:108
第Ⅰ卷(选择题,共64分)
一、选择题(本题包括16小题,每小题4分,共64分.每小题只有一个选项符合题意.)
1.调查发现,经过装修的居室中装修材料会缓慢释放出某些化学物质,这些物质浓度过高,会危害人的身体.这些污染物中最常见的是( )
A.甲醛 B.一氧化碳 C.二氧化硫 D.臭氧
2.![]() 元素是X的一种同位素,元素X在周期表中的位置是( )
元素是X的一种同位素,元素X在周期表中的位置是( )
A.第4周期第VA族 B.第4周期第ⅦA族 C.第3周期第ⅦA族 D.第5周期第ⅠA族
3.下列离子在溶液中可以大量共存,且加入过量氨水后也不产生沉淀的是( )
A.![]() 、
、![]() 、
、![]() ;、
;、![]() B.
B.![]() 、
、![]() 、
、![]() 、
、![]()
C.![]() 、
、![]() 、
、![]() 、
、![]() 7
D.
7
D.![]() 、
、![]() 、
、![]() 、
、![]()
4.设![]() 为阿伏加德罗常数,下列说法中不正确的是( )
为阿伏加德罗常数,下列说法中不正确的是( )
A.质子总数为5![]() 的重水(
的重水(![]() )是0.5mol
)是0.5mol
B.在标准状况下,11.2L甲烷和乙烯的混合物所含氢原子的数目为2![]()
C.2.4g Mg与过量盐酸反应,失去的电子数目为0.2![]()
D.6g![]() 所含的共价键的数目为0.2
所含的共价键的数目为0.2![]()
5.某同学想用实验证明高锰酸钾溶液的紫红色是![]() 离子的颜色而不是
离子的颜色而不是![]() 的颜色,他设计的下列实验步骤中对实验结论没有意义的是( )
的颜色,他设计的下列实验步骤中对实验结论没有意义的是( )
A.将高锰酸钾晶体加热分解,所得固体质量减少
B.观察氯化钾溶液没有颜色,表明溶液中![]() 无色
无色
C.在氯化钾溶液中加入适量锌粉振荡,静置未见变化,表示锌与![]() 无反应
无反应
D.在高锰酸钾溶液中加入适量锌粉振荡,静置后见紫红色褪去,表明![]() 为紫红色
为紫红色
6.将a mol钠和a mol铝一同投入m g足量的水中,所得溶液的密度为dg・![]() 该溶液的质量分数为( )
该溶液的质量分数为( )
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
7.历史上最早使用的还原性染料是靛蓝,其结构式为: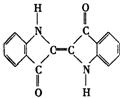 ,下列关于它的性质的叙述中错误的是( )
,下列关于它的性质的叙述中错误的是( )
A.它的苯环上的一氯取代物有4种
B.它的分子式是![]()
C.它是高分子化合物 D.它可使溴水褪色
8.在一密闭容器中用等物质的量的A和B发生如下反应A(g)4+2B(g)![]() 2C(g) 反应达到平衡时,若混合物中A和B的物质的量之和等于C的物质的量.则这时A的转化率为( )
2C(g) 反应达到平衡时,若混合物中A和B的物质的量之和等于C的物质的量.则这时A的转化率为( )
A.40% B.50% C.60% D.70%
9.有些固体药品长期存放时,若因密封不严,瓶内会逐渐积聚一定量的液体.以下各组中的每种药品都可能会出现这种现象的是( )
A.硫磺、生石灰、无水硫酸铜 B.红磷、氯化铁晶体、无水硝酸镁
C.白磷、明矾、无水氯化镁 D.碘片、氯化钠、无水氯化钙
10.纳米材料是当今世界的一种新型材料,广泛地应用于建筑、医学、电子等方面,纳米材料是指( )
A.尺度为米粒大小的颗粒制成的材料 B.尺度为![]() m数量级的小颗粒制成的材料
m数量级的小颗粒制成的材料
C.尺度为![]() m数量级的小颗粒制成的材料 D.尺度为
m数量级的小颗粒制成的材料 D.尺度为![]() m数量级的小颗粒制成的材料
m数量级的小颗粒制成的材料
11.下列叙述正确的是( )
A.久置于空气中的氢氧化钠溶液,加盐酸时有气体产生
B.50mL 12mol/L的浓盐酸与足量的二氧化锰反应,能生成氯气0.15mol
C.常温下,浓硫酸不与铜反应,是因为铜被钝化
D.少量二氧化碳通入浓的氯化钙溶液能生成白色沉淀
12.下列仪器:①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦烧瓶,能用酒精灯加热的是( )
A.②③⑤ B.③⑥⑦ C.①③④ D.③⑤⑦
13.下列叙述肯定正确的是( )
A.构成分子晶体的微粒一定含有共价键 B.较不活泼的金属单质不能还原较活泼的金属阳离子
C.酸和碱之间的反应都是复分解反应 D.熔化时无需破坏化学键的晶体一定是分子晶体
14.中小学生经常使用的涂改液中含有挥发性的有毒溶剂,应告诫学生尽量不要使用,以减少对身体的毒害及对环境的污染,该溶剂是( )
A.乙醇 B.乙酸 C.甘油 D.三氯乙烯
15.邻甲基苯甲酸(![]() )有多种同分异构体,其中属于酯类,且分子结构中含有甲基和苯环的异构体有( )
)有多种同分异构体,其中属于酯类,且分子结构中含有甲基和苯环的异构体有( )
A.6种 B.5种 C.4种 D.3种
16.按装置图进行实验,若图的x轴表示流入阴极的电子的量,则y轴不可能表示的是( )
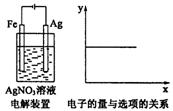
A.![]() 物质的量浓度 B.
物质的量浓度 B.![]() 物质的量浓度 C.溶液的pH D.银棒的质量
物质的量浓度 C.溶液的pH D.银棒的质量
第Ⅱ卷(非选择题,共56分)
二、(本题包括两小题,共20分)
17.(8分)(1)指出使用下列仪器或用品时的第一步操作.
①托盘天平______________________________________________________
②淀粉KI试纸___________________________________________________
③滴定管________________________________________________________
(2)实验室用无水酒精和浓![]() 制取乙烯,应选用的温度计是________
制取乙烯,应选用的温度计是________
A.体温计 B.酒精温度计
C.最大刻度为150℃的水银温度计 D.最大刻度为200℃的水银温度计
18.(12分)根据下述实验装置和操作,回答有关问题.
(1)按图中所示装置,用两种不同操作分别进行实验,观察B管中现象.
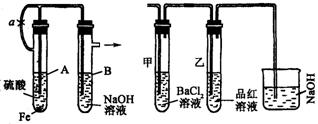
操作1:先夹紧止水夹a,再使A管开始反应.实验中在B管中观察到的现象是:__________________
_______________________________________________________________________________________________
B管中发生反应的离子方程式是:_____________________________________________________
操作2:打开止水夹a,使A管开始反应一段时间后再来夹紧止水夹a.实验中在B管中观察到的现象是:_______________________________________________________________________________________.
B管中发生反应的离子方程式是:_____________________________________________________
(2)上述装置的实验结束后,取A管内反应所得溶液,隔绝空气小心蒸干后再高温煅烧(有关装置及操作均已略去),最后留下红色固体.将分解时产生的气体按图所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内溶液红色褪去.回答:
问题1:用化学方程式说明试管甲产生白色沉淀的原因(不用文字说明).
问题2:根据实验现象,写出图中A管内溶液蒸干后,在高温煅烧分解时所产生的氧化还原反应的化学方程式_____________________.这个反应的氧化剂是________,还原剂是________.
三、(本题包括两小题,共20分)
19.(10分)![]() 和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为:
和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为:![]()
(1)请完成该化学方程式,并配平.
(2)浓盐酸在反应中显示出来的性质是________(填写编号,多选倒扣).
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)产生0.1mol![]() ,则转移的电子的物质的量为________mol.
,则转移的电子的物质的量为________mol.
(4)![]() 具有很强的氧化性.因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是
具有很强的氧化性.因此,常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是![]() 的□倍.
的□倍.
20.(10分)图中①~⑩分别代表有关反应中的一种物质,它们均为中学化学中的常见物质.已知①~⑤和⑥~⑩中分别含有同一种元素.反应⑤→①+
![]() 的条件未标出.请填写以下空白:
的条件未标出.请填写以下空白:
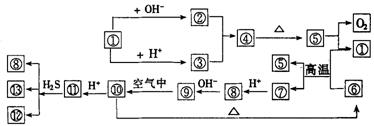
(1)①、⑤、⑥的化学式分别是_______________________________________________.
(2)②、③反应的离子方程式是__________________________________________________________________
(3)![]() 和
和![]() 反应的离子方程式是_____________________________________________________________
反应的离子方程式是_____________________________________________________________
四、(本题包括两小题,共16分)
21.(8分)有一种广泛用于汽车家电产品上的高分子涂料是按下列流程图生产的.图中有机化合物M(化学式为![]() )和A都可以发生银镜反应,N和M的分子中碳原子数相等.A的烃基上一氯取代位置有3种.
)和A都可以发生银镜反应,N和M的分子中碳原子数相等.A的烃基上一氯取代位置有3种.
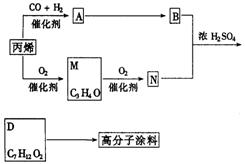
(1)写出物质的结构简式: A________________ B___________________ N:___________________ (2)用化学方程式表示下列转化过程:
①丙烯→M ②N+B→D
22.(8分)将某温度下的![]() 溶液200g蒸发掉10g水,恢复到原温度,或向其中加入10g
溶液200g蒸发掉10g水,恢复到原温度,或向其中加入10g![]() 固体,均可使溶液达到饱和.试计算该温度下
固体,均可使溶液达到饱和.试计算该温度下![]() 的溶解度.
的溶解度.
参考答案
一、
1.A 为装修材料中的高分子钾化合物的产物.
2.D 该元素为37号元素,在元素的下方.
3.C A中![]() 和
和![]() ;D中
;D中![]() 和
和![]() 不能大量共存,B项加入
不能大量共存,B项加入![]() 有沉淀产生.
有沉淀产生.
4.D 所含共价键数目为![]() .
.
5.A B项验证![]() ,C、D项验证
,C、D项验证![]() .
.
6.C 溶质为![]() ,质量为82a,溶液质量为23a+27a+m-4a=46a+m.
,质量为82a,溶液质量为23a+27a+m-4a=46a+m.
7.C 结构对称,且含有双键.
8.A A(g)+2B(g)![]() 2C(g)
2C(g)
始 a a 0
变 x 2x 2x
平 a-x a-2x 2x
a-x+a-2x=2x
![]()
A的转化率为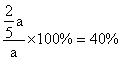
9.B 红磷氧化为![]() 、吸水.
、吸水.![]() 可吸水潮解、
可吸水潮解、![]() 可吸水潮解.
可吸水潮解.
10.D 1纳米=![]() m
m
11.A B项中盐酸变稀后不与![]() 反应.C项中反应缓慢.D项不能反应.
反应.C项中反应缓慢.D项不能反应.
12.D 集气瓶、量筒、容量瓶不能加热
13.D A项中如Ar.B项如![]() .C项如
.C项如![]() 和HI.
和HI.
14.D A、B、C三项中的物质无毒.
15.C 分别为
16.D 由图像知x变化y不变,故为![]() 、
、![]() 、溶液的pH.而Ag棒溶解.Fe棒析出Ag.
、溶液的pH.而Ag棒溶解.Fe棒析出Ag.
二、
17.(1)①调节零点 ②用水润湿 ③检查是否漏水 (2)D
18.(1)操作1:先出现白色絮状沉淀,然后沉淀迅速变灰绿色,最后变为红褐色.
方程式:![]()
![]()
操作2:溶液中有气泡产生,夹好夹子a后,溶液中出现白色絮状沉淀,一段时间内不变色.
方程式:![]()
(2)问题1:![]()
![]()
问题2:![]() ;
;![]() ,
,![]()
三、
19.(1)2 4 2 2 1 ![]() (2)② (3)0.2 (4)2.63
(2)② (3)0.2 (4)2.63
20.(1)①Al;⑤![]() ;⑥
;⑥![]() (2)
(2)![]()
(3)![]()
四、
21.(1)A:![]() ―
―![]() ―
―![]() ―CHO
―CHO
B:![]() ―
―![]() ―
―![]() ―
―![]()
N:![]() CH―COOH
CH―COOH
(2)①
②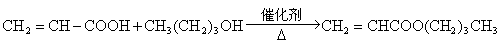
![]()
22.![]()