选择题强化训练(7)
一、单选题(每小题3分,共8×4=32分)
1、某物质经分析,只含一种元素,则此物质
A、一定是一种单质; B、一定是纯净物;
C、一定是混合物; D、可能是纯净物,也可能是混合物
2、微量元素是指在人体内总含量不到万分之一,质量总和不到人体质量的千分之一的二十多种元素,这些元素对人体正常代谢和健康有重要作用,下列元素不是微量元素的是
A、I B、F C、H D、Fe
3、雷雨时,某含氮物质随雨水降落地面,可使土壤中氮元素含量增加,这种含氮物质是
A、氨 B、氯化铵 C、硝酸 D、硝酸铵
4、某温度下,150g水中溶解100gNa2SO3・7H2O晶体(Na2SO3式量:126),恰好配成饱和溶液。则该温度下,Na2SO3的溶解度为
A、45.45g B、25g C、16g D、11.25g
5、某碱式碳酸镁[Mg(OH)2・xMgCO3]固体31克恰好跟100mL8mol/L的盐酸反应后成MgCl2溶液,则x为
A、1 B、2 C、3 D、4
6、下列反应中,调节反应物用量或浓度,不会改变反应产物的是
A、硝酸中加铜片; B、二氧化硫通入石灰水
C、烧碱溶液加放氯化铝溶液中; D、铁在硫蒸气中燃烧
7、下列实验中:1)配制一定物质的量浓度的溶液;2)pH试纸的使用;3)过滤,蒸发,均用到的仪器是
A、试管 B、胶头滴管 C、玻璃棒 D、漏斗
8、为同时施用分别含N、P、K三种元素的化肥,对于给定的化肥:①K2CO3 ②KCl ③Ca(H2PO4)2④(NH4)2SO4 ⑤氨水,最适宜的组合是
A、①③④ B、①③⑤ C、②③④ D、②③⑤
二、选择题(每小题有1~2个正确答案,共4×10=40分)
9、下列离子方程式正确的是
A、在氢氧化钡溶液中加入过量小苏打: Ba2+ + 2OH- + 2HCO3- = BaCO3↓+ CO32- + 2H2O
B、在氢氧化钾的稀溶液中通入过量SO2: SO2 + OH- = HSO3-
C、氯化铁水解: Fe3+ +3H2O = Fe(OH)3↓+ 3H+
D、氯气通入水中:Cl2 + H2O = 2H+ + Cl- + ClO-
10、FeS2的结构类似于Na2O2,是一种过硫化物,与酸反应生成H2S2,H2S2类似于H2O2,易分解:H2S2 = H2S + S↓。实验室制取H2S时,某学生误将FeS2颗粒当作FeS使用,当FeS2反应完后,不可能生成的物质是
A、FeS B、H2S C、S D、FeCl3
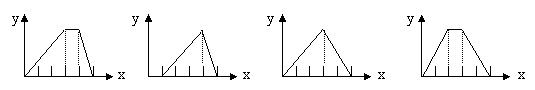 11、将物质的量相等的硫酸铝和硫酸铵溶于水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是
11、将物质的量相等的硫酸铝和硫酸铵溶于水形成VmL混合溶液,向混合溶液中逐滴加入某氢氧化钠的溶液(其物质的量浓度为混合溶液中两溶质的物质的量浓度之和),直至过量。下列表示氢氧化钠溶液加入的体积(x)与溶液中沉淀物的量(y)的关系示意图中正确的是
![]() A、
B
C
D
A、
B
C
D
12、下列各组离子在溶液中能大量共存的、且此溶液既能与盐酸反应又能与烧碱反应的是
A、Na+、K+、SO42-、HCO3- B、AlO2-、OH-、Na+、K+
C、K+、NH4+、NO3-、Cl- D、NH4+、Fe2+、HSO4-、OH-
 13、目前人们正在研究一种高能电池――钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na + xS Na2Sx,以下说法正确的是:
13、目前人们正在研究一种高能电池――钠硫电池,它是以熔融的钠、硫为两极,以Na+导电的β-Al2O3陶瓷作固体电解质,反应式如下:2Na + xS Na2Sx,以下说法正确的是:
A、放电时钠作正极,硫作负极;
B、充电时钠极与外电源的正极相连,硫与外电源的负极相连
C、充电时,阳极发生的反应为:Sx2- - 2e = x S
D、放电时钠极发生氧化反应
![]() 14、在一定条件下,可逆反应 X(g) +3Y(g)
2Z(g)达到平衡时,测得Y的转化率为37.5%,X的转化率为25%,则反应开始时充入容器中的X和Y的物质的量之比是
14、在一定条件下,可逆反应 X(g) +3Y(g)
2Z(g)达到平衡时,测得Y的转化率为37.5%,X的转化率为25%,则反应开始时充入容器中的X和Y的物质的量之比是
A、1:3 B、3:1 C、3:2 D、1:2
15、某氧原子的质量为a g,12C原子的质量为b g,且NA表示阿氏常数,下列说法中正确的是:
A、氧元素的相对原子质量为12a/b B、1mol该原子质量为aNAg
C、x g该氧原子所含的电子数为8x/a D、y g 该氧原子的中子数一定为8y/a
16、有Xn+、Ym+、Zn-,已知它们各自带有的电荷数值m>n,且X、Y、Z三种原子的M电子层中的电子数均为奇数。若按X→Y→Z的顺序,下列说法中正确的是]
A、它们的最高价氧化物的相应水化物的碱性依次减弱,酸性依次增强
B、它们的原子半径依次增大;
C、它们的单质在常温、常压下的密度依次减小
D、它们的最高价氧化物的水化物都是强电解质
![]() 17、金属卤化物与卤素化合可生成多卤化物,如KI + I2 KI3,有关KI3的叙述中错误的是
17、金属卤化物与卤素化合可生成多卤化物,如KI + I2 KI3,有关KI3的叙述中错误的是
![]() A、I2在KI溶液中溶解度增大是由于生成了I3-; B、I3-在溶液中存在平衡:I3- I2 + I-;
A、I2在KI溶液中溶解度增大是由于生成了I3-; B、I3-在溶液中存在平衡:I3- I2 + I-;
C、KI3溶液遇淀粉不呈蓝色; D、将氯气通入KI3溶液中,I3-浓度减小。
 18、如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距离为a cm,氯化铯的式量为M,NA为阿氏常数,则氯化铯晶体的密度为
18、如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距离为a cm,氯化铯的式量为M,NA为阿氏常数,则氯化铯晶体的密度为
|
|
| ||||||||
| ||||||||||
A、―― g/cm3 B、―― g/cm3 C、―― g/cm3 D、―― g/cm3
![]() 19、氢叠氮酸(HN3与醋酸酸性相近,基其盐稳定,但撞击发生爆炸生成氮气,有关氢叠氮酸的叙述有①NaN3的水溶液呈碱性;②HN3的固体属于分子晶体;③NaN3的固体属于离子晶体;
④NaN3可用于小汽车防撞保护气囊。其中正确的是
19、氢叠氮酸(HN3与醋酸酸性相近,基其盐稳定,但撞击发生爆炸生成氮气,有关氢叠氮酸的叙述有①NaN3的水溶液呈碱性;②HN3的固体属于分子晶体;③NaN3的固体属于离子晶体;
④NaN3可用于小汽车防撞保护气囊。其中正确的是
A、①②③ B、②③④ C、①③④ D、全部
|
![]()
![]()
![]() R1-C=CH-R2
R1-C=O + R2CHO。现有化学式为C7H14的烯烃,它与H2加成反应后生
R1-C=CH-R2
R1-C=O + R2CHO。现有化学式为C7H14的烯烃,它与H2加成反应后生
R R 成2,3-二甲基戊烷,它经臭氧氧化后在Zn存在下
水解成乙醛和一种酮,由此可推断该有机物的结构简式为
![]()
![]()
![]()
![]()
![]()
![]()
![]() A、CH3-C=CH-CH-CH3 B、CH3CH=C-CH2-CH2-CH3 C、CH3-CH=C-CH-CH3 D、CH3-C
=C-CH2-CH3
A、CH3-C=CH-CH-CH3 B、CH3CH=C-CH2-CH2-CH3 C、CH3-CH=C-CH-CH3 D、CH3-C
=C-CH2-CH3
CH3 CH3 CH3 H3C CH3 H3C CH3