北大附中(海淀区) 2004年第二学期期末练习
高二化学
2004.6
可能用到的相对原子质量:H 1 O 16 C 12 N 14 Na 23
Cu 64 Fe 56 Al 27 Cl 35.5
第Ⅰ卷(选择题 共50分)
请将第Ⅱ卷中各小题正确答案前的字母,填到第4页首的表格中相应的位置上.
一、选择题(下列各题只有一个选项符合题意.每小题2分,共50分)
1.环境污染已经成为人类社会面临的重大威胁,下列情况下不会造成大气污染的是
A.汽车尾气的排放 B.工业上大量燃烧含硫燃料
C.燃放烟花爆竹 D.新能源氢气的燃烧
2.下列元素原子半径最小的是
A.Na B.Mg C.Al D.H
3.下列气体可以用排水法收集的是
A.HCl
B.![]() C.
C.![]() D.
D.![]()
4.下列含氧酸中,酸性最强的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
5.下列仪器中,可以直接加热的是
A.烧杯 B.容量瓶 C.试管 D.量筒
6.下列物质中,属于强电解质的是
A.NaCl
B.![]() C.
C.![]() D.
D.![]()
7.下列金属中,常温下能在浓硫酸或浓硝酸中发生钝化的是
A.Cu B.Mg C.Zn D.Fe
8.下列反应中,属于取代反应的是
A.甲烷和氯气混合后光照
B.用乙烯制取聚乙烯
C.用镍做催化剂和加热的条件下,苯和氢气反应
D.用乙醇和浓硫酸制乙烯
9.在一个2L的密闭容器中,某一反应物的物质的量为1.0 mol,经过20s后,它的物质的量变成了0.6 mol,在这20 s内它的反应速率为
A.0.4mol/L B.0.02mol/(L・s)
C.0.01mol/L D.0.O1mol/(L・s)
10.下列各组中的两种物质,互为同素异形体的是
A.![]() 和
和![]() B.
B.![]() 和
和![]()
C.金刚石和石墨 D.乙酸和乙酸乙酯
11.下列通式中,表示烯烃的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
12.下列物质中,跟水反应有气体生成的是
A.CaO
B.Na
C.![]() D.
D.![]()
13.下列物质中,既能使溴的四氯化碳溶液褪色,又能使酸性高锰酸钾溶液褪色的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
14.下列试剂中,能将![]() 、
、![]() 、
、![]() 、
、![]() 四种溶液一一区分开的是
四种溶液一一区分开的是
A.NaOH
B.![]() C.
C.![]() D.
D.![]()
15.化学与生活密切相关,运用你所学的化学知识判断下列说法中不正确的是
A.明矾可用于净水 B.制药皂时可以掺入少量的苯酚
C.铝锅可以用来蒸煮酸性食物 D.甲醛的水溶液可用于杀菌和防腐
16.下列有机物的命名中,正确的是
A.1-甲基丙烷 B.2-甲基丙烷
C.2,3-甲基丁烷 D.2甲基丙烷
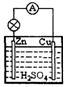
17.如图,在锌、铜和稀硫酸组成的原电池中,正极发生的反应是
A.![]() B.
B.![]()
C.![]() D.
D.![]()
18.下列物质中既能跟盐酸反应又能跟氢氧化钠溶液反应的是
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
19.下列各组离子中,能大量共存于同一水溶液中的是
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
20.下列物质中,可以发生银镜反应的是
A.葡萄糖 B.淀粉 C.蛋白质 D.纤维素
21.在下列各用途中,利用了物质的氧化性的是
A.用食盐腌渍食物 B.用盐酸除去铁钉表面的铁锈
C.用汽油擦洗衣料上的油污 D.用臭氧对自来水进行消毒
22.相同物质的量的Fe和Al分别和足量的稀盐酸反应,产生![]() 的质量比是
的质量比是
A.1∶3 B.2∶3 C.1∶1 D.3∶2
23.下列离子方程式中正确的是
A.碳酸钙溶于盐酸中:![]()
B.氢氧化钡溶液与稀硫酸发生中和反应:![]()
C.稀硝酸滴在铜片上:![]()
D.氯化铝溶液跟过量氨水反应:![]()
24.常温下,1
mol/L ![]() 溶液中存在着电离平衡
溶液中存在着电离平衡![]()
![]()
![]() ,若使c(
,若使c(![]() )减小,可加入的物质是
)减小,可加入的物质是
A.![]() B.
B.![]() C.NaOH
D.HCl
C.NaOH
D.HCl
25.下列说法中正确的是
A.1mol氢气的体积是22.4 L
B.58.5gNaCl溶于1 L水中,所得溶液的物质的量浓度为1 mol/L
C.![]() 的摩尔质量为44 g
的摩尔质量为44 g
D.17g氨气中所含原子的物质的量为4mol
第Ⅱ卷(非选择题 共50分)
二、填空题(共 23分)
26.(共3分)在①![]() ②
②![]() ③KOH三种物质中,只含离子键的是(填写序号,下同),只含共价键的是______________,既含共价键又含离子键的是______________.
③KOH三种物质中,只含离子键的是(填写序号,下同),只含共价键的是______________,既含共价键又含离子键的是______________.
27.(共3分)在元素周期表中,同主族、同周期元素的性质呈周期性变化.请判断碳、氮、磷元素中,非金属性最强的元素是__________(用元素名称表示),组成自然界物质最多的元素是______(用元素符号表示).氮元素的原子结构示意图为___________________.
28.(共3分)用已经准确量取过的浓硫酸来配制100 mL某浓度的稀硫酸,所要用到的仪器是烧杯、胶头滴管、_____________和_____________;若要用该稀硫酸滴定锥形瓶中的某碱溶液,则稀硫酸应放置在(填仪器名称)_______________中.
29.(共8分)2004年4月16日,重庆市天原化工总厂发生有毒气体的泄露事件,导致15万人大转移.该有毒气体为中学常见的有色气体![]() ;已知A与B、C、D均为短周期非金属元素,其中B元素的原子最外层电子数是次外层的3倍,B、C可形成两种液态化合物,其分子式分别为
;已知A与B、C、D均为短周期非金属元素,其中B元素的原子最外层电子数是次外层的3倍,B、C可形成两种液态化合物,其分子式分别为![]() 和
和![]() ;C、D可形成一种极易溶于水的气体,该气体能使湿润的红色石蕊试纸变蓝.请回答:
;C、D可形成一种极易溶于水的气体,该气体能使湿润的红色石蕊试纸变蓝.请回答:
(1)为防止有毒气体的危害,消防队员喷洒了大量溶液,用于吸收![]() ,写出该反应的离子方程式______________________________________________.
,写出该反应的离子方程式______________________________________________.
(2)实验室制取气体![]() 的化学方程式是 ____________________________.若采用瓶口向上排空气法收集
的化学方程式是 ____________________________.若采用瓶口向上排空气法收集![]() ,用一种化学方法验满
,用一种化学方法验满![]() 的实验操作及现象是___________.
的实验操作及现象是___________.
(3)由B、C、D可组成既能做肥料又能做炸药的化合物,该化合物与NaOH浓溶液共热的离子反应方程式为_______________________________________.
30.(共6分)要除去下列物质中的杂质(括号内为杂质),写出所用试剂或操作方法并完成有关反应的离子方程式或化学方程式.
(1)碳酸钠固体(碳酸氢钠):操作方法为_________________________,化学方程式为_______________________________________.
(2)NaCl溶液(NaBr):试剂为(写化学式)__________________________,离子方程式为_________________________________.
三、实验题:(共19分)
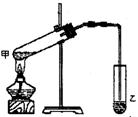
31.(共4分)实验室用下图所示的装置制取乙酸乙酯.在试管甲中加入适量的乙醇、浓硫酸和冰醋酸,加热3~5 min.
(1)写出甲试管中发生反应的化学方程式:____________________________________,
(2)反应后,乙试管中收集到的液体的分离方法是_________________,该分离操作中所用主要仪器的名称是_____________(写1个).
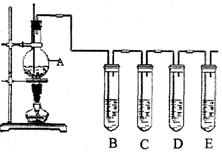
32.(8分)在实验室制取乙烯的实验中常因温度过高而使乙醇炭化,导致生成的乙烯中混有![]() 和
和![]() .已知
.已知![]() 有还原性,能使
有还原性,能使![]() 水、酸性
水、酸性![]() 溶液褪色.现将混合气通入如下图装置中.
溶液褪色.现将混合气通入如下图装置中.
试回答:
(1)A中发生反应的化学方程式______________________________________.
(2)若要验证混合气中含有![]() 和
和![]() ,则B、E装置内应选用的试剂分别是________________和_________________;若要除去
,则B、E装置内应选用的试剂分别是________________和_________________;若要除去![]() 和
和![]() 而验证乙烯的不饱和性,上面的装置可做的改动是:_________________________,可将混合气体依次通入的试剂分别为:___________________________________________________.
而验证乙烯的不饱和性,上面的装置可做的改动是:_________________________,可将混合气体依次通入的试剂分别为:___________________________________________________.
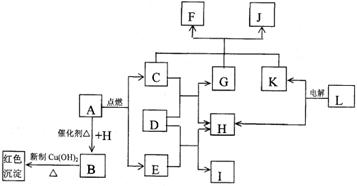
33.(共7分)下图表示中学常见的一些物质之间相互转化的关系.已知B的蒸气密度是同条件下氢气的22倍,F、 H、K均为单质,L是两性氧化物.
回答下列问题:
(1)J的化学式为______________;
(2)写出C+D→G+H的化学反应方程式:
________________________________________________________;
在该反应中D(填序号)_____________________________
①是氧化剂 ②是还原剂
③既是氧化剂又是还原剂 ④既不是氧化剂也不是还原剂
(3)I的水溶液呈__________________性(选填“酸”、“碱”或“中”),发生水解的离子方程式为___________________________________________________.
四、计算题(共8分)
34.(4分)23g乙醇与足量金属钠反应,标准状况下产生氢气的体积是多少?
35.(4分)将Cu与CuO的混合物13.4 g溶于250 mL某浓度的硝酸中,固体全部溶解,产生标准状况下的![]() (x=1、2)气体共2.24 L.取反应后溶液体积的
(x=1、2)气体共2.24 L.取反应后溶液体积的![]() ,往其中慢慢滴加5.00 mol/L的NaOH溶液,当加到38.0 mL时,过量的硝酸被中和,同时
,往其中慢慢滴加5.00 mol/L的NaOH溶液,当加到38.0 mL时,过量的硝酸被中和,同时![]() 恰好完全沉淀.
恰好完全沉淀.
求:
(1)原硝酸溶液的物质的量浓度是多少?
(2)原混合物中Cu单质的质量最少是多少?
参考答案
一、选择题(每小题2分,共50分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 答案 | D | D | B | D | C | A | D | A | D |
| 题号 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 |
| 答案 | C | B | B | D | C | C | B | B | C |
| 题号 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | ||
| 答案 | C | A | D | B | D | C | D |
二、填空题(每个方程式2分,共23分)
26.(3分) ②, ①, ③
27.(3分) 氮
C
![]()
28.(3分)玻璃棒 100 mL容量瓶(或100 mL容量瓶 玻璃棒); 酸式滴定管
29.(8分)(1)![]()
(2)![]()
将湿润的淀粉KI试纸靠近集气瓶口,若试纸变蓝,则气体收集满.
(其它合理答案均给分)
(3)![]()
30.(6分)(1)加热
![]()
(2)![]()
![]()
四、实验题(每个方程式2分,共19分)
31.(共4分)
(1)![]()
(2)分液 分液漏斗
32.(共8分)
(1)![]()
(2)品红溶液 澄清石灰水 去掉B、C、D、E中的任意1个装置(3分)
33.(共7分)
(1)![]() (2)
(2)![]() ③
③
(3)碱 ![]()
![]()
![]() (写一步、两步都给满分)
(写一步、两步都给满分)
五、计算题:(共8分)
34.(4分)解:
![]() (1分)
(1分)
2×46g 22.4 L (1分)
![]() (1分)
(1分)
![]() (1分)
(1分)
答:略.
35.(4分)解:
根据守恒原理:![]() (1分)
(1分)
1 1
依题意:
(1)![]() (1分)
(1分)
(2)生成![]() 时,需铜最少:
时,需铜最少:![]() (1分)
(1分)
64g 2 mol
m(Cu)(2.24÷22.4)mol
m(Cu)=3.2g (1分)
答:略.
(以上合理答案均酌情给分.)