理科综合能力测试[化学部分](一)
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
原子量:H 1,C 12,O 16,Mg 24
1.微量生命元素是指在人体内总含量不到万分之一,总质量不到人体的千分之一的元素,这些元素对人体正常代谢和健康起着重要作用。到目前为止确认的微量生命元素有16种。下列元素不属于微量元素的是
A.I B.F C.H D.Zn
2.甲、乙是同周期的非金属元素,若原子半径甲大于乙,则下列叙述中正确的是
A.最高价氧化物对应水化物的酸性甲比乙强
B.阴离子的还原性甲比乙强
C.气态氢化物的稳定性甲比乙强
D.氢化物水溶液的酸性甲比乙强
3.实验前设法将所用的溶液排尽空气。若将铁屑溶于过量的盐酸中,加入下列溶液后,再加入KSCN溶液,观察到溶液呈血红色的是
A.H2SO4稀溶液 B.Zn(NO3)2 溶液
C.CuCl2溶液 D.Na2S溶液
4.目前使用的塑料(如聚苯乙烯),因难以分解而造成的“白色污染”甚为严重。国家铁道部已下令全国铁路餐车上停上使用聚苯乙烯制造的餐具,改用降解塑料,其结构简式如下:
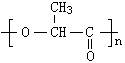
该塑料在乳酸菌作用下会迅速分解为无毒的物质。下列关于这种降解塑料的叙述正确的是
A.它的化学式式量为72 B.它是经加聚反应制得的
C.它的合成单体是![]() D.它是一种无毒的纯净物
D.它是一种无毒的纯净物
5.某二元弱酸(简写为H2A)溶液,按下式发生一级电离和二级电离:
H2A![]() H+
+ HA— 一级电离,电离度为
H+
+ HA— 一级电离,电离度为![]() (H2A)
(H2A)
HA—![]() H+
+ A2— 二级电离,电离度为
H+
+ A2— 二级电离,电离度为![]() (HA—)
(HA—)
已知相同浓度时的电离度![]() (H2A)>
(H2A)>![]() (HA—),则下列四种溶液中[A2— ]最小的是
(HA—),则下列四种溶液中[A2— ]最小的是
A.0.01 mol·L—1的H2A
B.0.01 mol·L—1的NaHA溶液
C.0.02 mol·L—1 的NaOH与0.02 mol·L—1 NaHA溶液等体积混合
D.0.02 mol·L—1 的HCl与0.04 mol·L—1 NaHA溶液等体积混合
6.由环己烷、乙醇与乙醚(C2H5-O-C2H5)组成的混合物,经测定,碳的质量分数为72%。则该混合物中氧的质量分数为
A.14.2% B.16% C.17.8% D.19.6%
7.赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应发生Cu2S+2Cu2O![]() 6Cu+SO2↑,关于该反应的下列说法中,正确的是
6Cu+SO2↑,关于该反应的下列说法中,正确的是
A.该反应的氧化剂中只有Cu2O
B.Cu既是氧化产物,又是还原产物
C.氧化产物与还原产物的物质的量之比为6 :1
D.Cu2S在反应中既是氧化剂,又是还原剂
8.下列液体的pH值大于7的是
A.蔗糖溶液 B.胃液 C.人体血液 D.橙汁
第Ⅱ卷
(非选择题,共3小题,共50分)
9.(18分)a g Mg在充有b L(标准状况)CO2和O2混合气体的密闭容器中燃烧
(1)在密闭容器中可能发生的化学反应有___________________________________。
(2)若反应容器中CO2有剩余,则容器内的固体物质一定含有___________________。
(3)若反应容器中O2 有剩余,则容器内固体物质的质量为________________。此时,在b L CO2和CO2 的混合气体O2 的体积[V(O2)] 必须满足的条件是___________________。
(4)若反应后容器中无气体剩余,则容器内固体物质质量(m)的取值范围为______________________________。
10.(18分)下图中A是一种正盐,D的分子量比C的分子量大16,E是酸。当X是盐酸时,有图1所示转化关系;当X是强碱时,有图2所示转化关系。
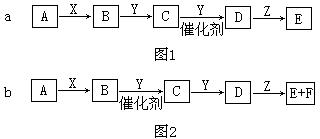
当X是强酸时,A、B、C、D、E均含有同一种元素;当X是强碱时,A、B、C、D、E均含有另一种元素。
(1)A是_________,Y是_________,Z是__________。
(2)当X是强酸时,E是_________________________。
(3)当X是强碱时,E是_____________,F是_____________。
(4)分别写出a、b中A与X反应的离子方程式______________________________、____________________________________。
11.(14分)丙二酸是含有3个碳原子的二元羧酸,在P2O5存在条件下丙二酸脱水生成C3O2,它的化学性活泼,可跟水发生加成反应生成丙二酸,跟HCl加成生成![]() 。
。
(1)C3O2的结构式为________________________。
(2)C3O2跟NH3 的加成产物是_____________________,跟CH3CH2OH 的加成产物是______________________________。
理科综合能力测试(化学部分)参考答案及评分标准
Ⅰ卷 每小题6分,共48分
1.C 2.B 3.B 4.C 5.A 6.A 7.D 8.C
Ⅱ卷 包括3小题,共50分
9.(18分)
(1)2Mg + O2 = 2MgO ,2Mg + CO2 = 2MgO + C,C + O2 = CO2
(每个化学方程式2分)
(2)MgO (3分)
(3)m
= ![]() g,
g,![]() ≤
≤![]() (每空3分)
(每空3分)
(4)![]() (3分)
(3分)
10.(18分)
(1)(NH4)2S,O2,H2O (每空2分)
(2)H2SO4 (2分)
(3)HNO3,NO (每空2分)
(4)NH4+
+OH—=NH3·H2O(或NH4+ +OH—![]() NH3↑+ H2O),S2—+2H+ =H2S↑
NH3↑+ H2O),S2—+2H+ =H2S↑
(每个离子方程式3分)
11.(14分)
(1)O=C=C=C=O (4分)
(2)![]() ,
,![]() (每空5分)
(每空5分)