理科综合能力测试[化学部分](四)
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
原子量:H 1,C 12,O 16,S 32,Cu 64
1.以下说法正确的是
A.石英玻璃是以纯碱、石灰石和二氧化硅为原料制成的
B.氮的固定是指将空气中游离的氮转变为氮的化合物的方法
C.绿色食品是指不含任何化学物质的食品
D.纳米材料是指一种称为“纳米”的新物质制成的材料
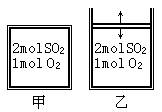 2.向容积固定的容器甲和带有活塞的定压容器乙中分别通入2 mol SO2和1 mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡。则下列说法正确的是
2.向容积固定的容器甲和带有活塞的定压容器乙中分别通入2 mol SO2和1 mol O2(如下图),若开始通气时两容器的体积相同,在相同温度下反应,一段时间后,反应达到平衡。则下列说法正确的是
A.平衡时,两容器内SO3的浓度必定相等
B.平衡时,混合气体中的SO3的体积分数甲比乙高
C.SO2的转化率乙容器内比甲容器内高
D.反应后的相同时间内,甲容器中的反应速率大
3.溶液体积和pH都相同的一元强酸X与一元弱酸溶液Y,已知弱酸的电离度为0.5%,则X和Y溶液分别中和相同浓度的NaOH溶液时,所需Y溶液的体积是X溶液的
A.20倍 B.100倍 C.200倍 D.500倍
4.对重水(D2O)(25℃,D2O离子积为1.6×10—15),可以用和pH一样的定义来规定重氢离子的负对数pD(即—lg[D+])。下列关于pD的叙述中正确的是
A.纯净重水的pD为7
B.在重水中溶解0.01 mol DCl,溶液pD为2
C.溶解0.01 mol NaOD的重水溶液1 L,pD为12
D.100 mL 0.25 mol·L—1的DCl重水溶液与50 mL 0.2 mol·L—1的NaOD重水溶液混合,溶液pD为1
5.已知某溶液中存在OH—、H+、NH4+、Cl— 四种离子,经四位同学测定其浓度大小的关系如下,其中不可能正确的HHH是
A.[Cl— ]>[NH4+]>[H+]>[OH— ] B.[Cl— ]>[H+]>[NH4+]>[OH— ]
C.[NH4+]>[OH— ]>[Cl— ]>[H+] D.[OH— ]>[H+]> [Cl— ]>[NH4+]
6.某温度下,在100 g水中加入m g CuSO4固体或加入n gCuSO4·5H2O晶体,均可使溶液恰好达到饱和,则m与n的关系符合
A.![]() B.
B.![]()
C.![]() D.
D.![]()
7.工业上废气中的氮氧化合物是主要的大气污染物之一,为了保护环境,工业上常通入氨气后发生如下反应:NOx + NH3 → N2 + H2O,使之转化为无毒的氮气,现有NO2和NO的混合气体3 L,同温同压下通入NH3 3 L,恰好使其完全转化为N2,则原混合气体中的NO2和NO的物质的量之比为
A.1:1 B.2:1 C.3:1 D.1:4
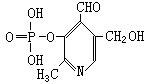 8.磷酸毗醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构如下,下列有关它叙述不正确的是
8.磷酸毗醛素是细胞的重要组成部分,可视为由磷酸形成的酯,其结构如下,下列有关它叙述不正确的是
A.能与金属钠反应
B.能使石蕊试液变红
C.能发生银镜反应
D.1 mol该酯与NaOH溶液反应,消耗3 mol NaOH
第Ⅱ卷
(非选择题,共3小题,共50分)
9.(19分)为证明有关物质的性质,某学生设计了图示的装置。当打开活塞C,使液体A与搁板H上的固体B相遇时,即有气体产生,并发现D中蜡烛(含CnH2n+2,n=20~30)慢慢熄灭;关闭C打开E时,则看到G中蜡烛燃烧得更亮。请写出该学生在装置中有关仪器内盛放的物质:
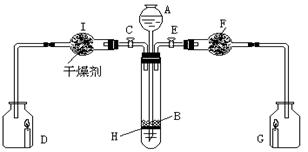
A______________,B______________,F______________。
用化学方程式表示上述实验中发生的有关反应:
___________________________________;__________________________________;
___________________________________;__________________________________。
10.(16分)某化合物A的分子式为C10H10O4,A不能与FeCl3溶液发生显色反应,在稀酸中加热能生成B、C、D三种化合物,化合物B能与FeCl3溶液发生显色反应,化合物C含碳的质量分数为40.0%,化合物D含氧的质量分数为50.0%。
(1)(4分)写出化合物C、D的结构简式
______________________________________________________________
(2)(6分)写出化合物B的结构简式
______________________________________________________________
(3)(6分)写出化合物A的结构简式
______________________________________________________________
11.(15分)三份1 L 1 mol·L—1 Ba(OH)2溶液分别滴加到以下1 L的各溶液中,请将实验过程中产生沉淀的物质的量(y)随所滴加的Ba(OH)2溶液的体积(x)之变化曲线表示在相应的坐标图上(曲线转折点须注明坐标值)。
(1)0.4mol·L—1AlCl3溶液(2)0.5mol·L—1KAl(SO4)2溶液(3)0.8mol·L—1H3PO4溶液



理科综合能力测试(化学部分)参考答案及评分标准
Ⅰ卷 每小题6分,共48分
1.B 2.C 3.C 4.D 5.D 6.B 7.A 8.D
Ⅱ卷 包括3小题,共50分
9.(19分)
A:稀盐酸(2分);B:CaCO3(2分);F:Na2O2(3分)
CaCO3+2HCl=CaCl2+H2O+CO2↑;2Na2O2+2CO2=2Na2CO3+O2;
2Na2O2+2H2O=4NaOH+O2;CxH2x+2 +(![]() )O2
)O2 ![]() xCO2+(x+1)H2O。(每式3分)
xCO2+(x+1)H2O。(每式3分)
10.(16分)
(1)C:CH3COOH D:CH3OH (每式2分,共4分)
(2)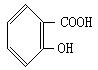

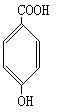 (每式2分,共6分)
(每式2分,共6分)
(3)

![]()
(每式2分,共6分)
11.(15分)
(1)
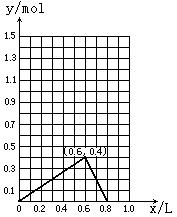 (5分)
(5分)
(2)
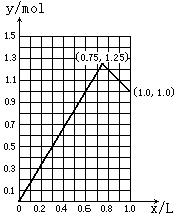 (5分)
(5分)
(3)
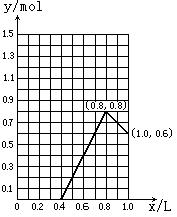 (5分)
(5分)