丽水地区高三理科综合总复习综合练习(二)
能力测试
本卷分第一卷(选择题)和第二卷(非选择题)两部分。满分300分。考试时间150分钟。
第一卷(选择题 共120分)
本卷共24题,每题5分,共120分。在下列各题的选项上,只有一个选项是符合题目要求的。
可能用到的原子量:C:12 Si:28
1. DNA分子的组成分析表明,下列相关比值中的哪一个不是恒定的
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
2. 纳米技术是跨世纪的新技术。如将激光束聚集到纳米范围内,就可以在分子水平上修改细胞的结构从而治疗许多遗传病以及癌症等。这一前景的生物学机理是
A. 激光的高能量使基因突变
B. 激光的单色性使基因互换
C. 激光的方向性使基因重组
D.激光的粒子性使染色体数目改变
3. 破伤风杆菌存在于泥土中,也经常寄居在人和动物的肠道内,但不致端正。当基进入深而狭窄的伤口内部时,则会大量繁殖并致病。由此推测破伤风杆菌的新陈代谢类型属于
A. 自养、厌氧型
B. 自养、需氧型
C. 异养、厌氧型
D.异养、需氧型
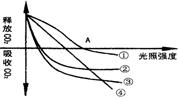
4. 右图中的曲线分别表示四种植物在不同光照强度下释放或吸收CO2的速率的变化情况。据图可知,它们当中,最耐阴的一种是
A.① B.② C.③ D.④
5. 某酒厂库存的啤酒因存放过久而产生沉淀。经化验,沉淀物是蛋白质。为此,提出两种解决方案:甲方案是加入少量蛋白酶;乙方案是加入少量氨基酸氧化酶。你认为
A. 甲方案合理
B. 乙方案合理
C. 两方案都合理
D.两方案都不合理
6. 在下列实例中,通过食物链而引起的生态危机是
A. 酸雨
B. 臭氧减少,臭氧层出现空洞
C. 汞镉等有毒物质的积累和浓缩
D.温室室效应
7. 由两种原子组成的纯净物
A. 一定是化合物
B. 可能是单质,可能是化合物
C. 一定是单质
D.一定是同素异形体
8. 生活中的某些问题,常常涉及到化学知识,下列分析正确的是
A. 氯气和二氧化硫均可作为漂白剂,若同时使用它们去漂白某一润湿的有色物质,漂白效果会明显加强
B. 为了实现中国2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中碘以单质的形式存在
C. 苯酚有杀菌和止痛作用,药皂中也掺有少量苯酚,所以我们可以用苯酚对环境消毒或直接涂抹于皮肤上进行消毒
D.工业酒精不能加水当饮料酒品尝,其原因是它含有甲醇,它虽具有酒香味,但饮后会导致中毒,甚至死亡
9. 日、美三位化学家因发现“传导聚合物”而荣获2000年诺贝尔奖。如在聚乙炔的合成过程 接触某些物质,其导电能力会提高1000万倍。这类化合物在21世纪将制成可折叠电视机屏幕,可穿在计算机,会发光的玻璃纸等,有关生成聚乙炔的反应属于
A. 取代反应
B. 消去反应
C. 缩聚反应
D.加聚反应
10.目前、科学界拟合成一种“双重结构”的球形分子,即把足球烯C60的分子容纳在SI60分子中,外面的硅原子与里面的碳原子以共价键结合,下列叙述不正确的是
A. 反应为置换反应
B. 晶体属分子晶体
C. 物质是一种新化合物
D.该物质的相对分子质量为2400
11.下列反应中,水起氧化剂或还原剂的作用是
A. 氟气通入水中
B. 氯 气通入水中
C. 过氧化钠加入水中
D.二氧化氮加入水中
12.当Naoh与氨水的pH、体积都相同时,下列叙述正确的是
A. 两溶液的物质的量浓度相同
B. 两溶液中的[H+]相同
C. 用同浓度盐酸中和时,消耗酸的体积相同
D.升高温度10℃,两者pH仍相等
13.在无色透明的酸性溶液中,能共存的离子组是
A. na+、 Mg2+、 NO![]() 、 SO
、 SO![]()
B. CO![]() 、NO
、NO![]() 、Al3+ 、Cl-
、Al3+ 、Cl-
C. MnO![]() 、K+、SO
、K+、SO![]() 、 Na+
、 Na+
D.K+ 、SO![]() 、 Fe2+、 NO
、 Fe2+、 NO![]() 、
、
14.现代建筑的门窗框架,常用电解加工成古铜色的硬铝制造。取硬铝样品进行如下实验:(已
知锰化铁活动)
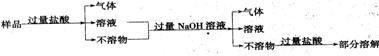
由此推知硬铝的组成是
A. Al 、Mg 、Si 、 Zn
B. Al 、Cu、 Mg 、Si 、Mn
C. Al 、Fe 、C 、Cu
D.Al 、Si 、Zn 、Na
15.只用一种试剂,即可区别NaBr、 NaI 、NaOH 、Na2CO3 、KSCN、H2S 、AgNO3 、C6H5OH 8种无色溶液,该试剂是
A. 硫酸溶液
B. 盐酸
C. 氯化铁溶液
D.氨水
16.水平弹簧振子做简谐运动,轨迹上有A、B两点,已知振子位于A、B两点的动能EA<EB, 且A、B两点的位移方向相同。关于振子通过A、B两点的加速度aA、aB和动量PA、PB一定有
A. aA>aB,且方向相同,
B. aA<aB,且方向相反,
C. PA>PB,且方向相同,
D.PA<PB,且方向相反
17.在电场中,一个带正电的微粒,只受到电场力的作用,沿直线运动,顺序经过直线上A、B、C三点,如图所示。已知带电微粒在A、B、C三点的动能EA=4EB,EC=0,下列说法正确的是
![]()
A. 由A到B所用时间一定小于由B到C所用时间
B. 由A到B所用时间一定等于由B到C所用时间
C. 电场线的方向一定沿CA方向
D.电场线的方向一定沿AC方向
18.如图所示,一细导体杆弯成四个拐角均为直角的平面折线,oabcdo′,oa和do′由轴承支撑着水平放置,整个平面折线在竖直平面内。导体杆中沿oabcdo′方向通有恒一的电流I。若在空间突然施加一个匀强磁场,下列说法正确的是

A. 如果磁场方向竖直向下,则导体杆要偏离竖直平面,随偏离竖直平面的夹角增大,bc段受到的磁场力逐渐减小,对oc′轴的力矩也逐渐减小
B. 如果磁场方向竖直向下,则导体杆要偏离竖直平面,随偏离竖直平面的夹角增大,bc段受到的磁场力不变,对oc′轴的力矩逐渐减小
C. 如果磁场方向垂直纸面向外,则导体杆要偏离竖直平面,随偏离竖直平面的夹角增大,bc段受到的磁场力逐渐减小,对oo′轴的力矩也逐渐减小
D.如果磁场方向垂直纸面向外,则导体杆要偏离竖直平面,随偏离竖直平面的夹角增大,bc段受到的磁场力不变,对oo′轴的力矩逐渐减小
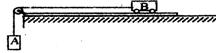
19.重物A和小车B的重分别为GA和GB,用跨过定滑轮的细线将它们连接起来,如图所示。已知GA>GB,不计一切磨擦。则细线对小车B的拉力T的大小是
A. T=GA
B. GA >T ≥GB
C. T <GB
D.GA、GB的大小未知,T不好确定
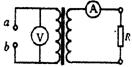
20.如图所示,一个理想变变压器,初级线圈的匝数为n1,a、b接交流电源,次级线圈匝数为n2与负载电阻R相连接,R=40Ω。图中电压表的示数为100V,初级线圈的电流为0.4A。下列说法正确的是
A. 次级线圈中的电流的最大值为1A
B. 初级和次级线圈的匝数比n1:n2=2:5
C. 如果将另一个阻值为R的电阻与负载电阻串联,图中电流表的示数为2A
D.如果将另一个阻值为R的电阻与负载电阻串联,变压器消耗的电功率80W
21.如图所示,凸透镜的主轴上有一个点光源S发出绿光,其中射到凸透镜上的两条光线:SA和SO,经凸镜折射后,是平行光,如图中的2、5。若光源S发出紫光,则SA和SO这两条光线从凸透镜射出后可能是
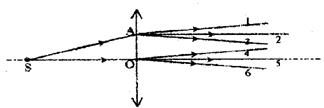
A. 仍是平行光,如图中的2、5
B. 仍是平行光,可能是光线1、4,也可能是3、5
C. 不是平行光,如图中的1、5
D.不是平行光,如图中的3、5
22.一个小物块冲上一个固定的粗糙斜面,经过斜面上A、B两点,到达斜面上最高点后返回时,又通过了B、A两点,如图所示。关于物块上滑时由A到B的过程和下滑时由B到A的过程,动能的变化量的绝对值△E上和△E下,以及所用时间t上和t下相比较,有
A. △E上<△下,t上<t下 B.△E上>△下,t上>t下
C.△E上<△下,t上>t下 D.△E上>△下,t上<t下

23.如图所示一列横波在t1和t2时刻的波形分别如图中的实线和虚线所示,已知波在介质中的传播速度是2m/s。
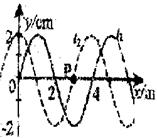
①若t2-t1=1.5s,则波是向右传播的
②若t2-t1=1.5s,则波是向左传播的
③若t2-t1=2.5s,则t2时刻质元P向y轴正方向运动
④若t2-t1=2.5s,则在t2时刻质元P向y轴负方向运动
上述结论正确的是
A.①③ B.②③ C.①④ D.②④
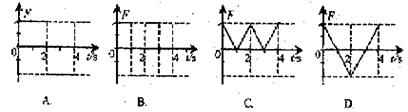
24.矩形导线框abcd放在匀强磁场中,磁感线方向与线圈平面垂直,磁感应强度B随时间变化的图象如图所示。t=0时刻,磁感应强度的方向垂直于纸面向里。在所0―4s时间内,线框的ab边受力随时间变化的图象(力的方向规定以向左为正方向),可能如下图中的:
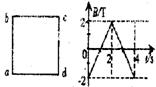
第二卷(共180分)
25.(1)(8分)棉铃虫是一种严重危害棉花的害虫。我国科学工作者发现一种生活在棉铃虫消化道内的苏云金杆菌能分泌一种毒蛋白使棉铃虫致死,而毒蛋白对人畜无害,通过基因工程的方法,我国已将该毒蛋白基因转移到棉花植株内并实现成功表达。由于棉铃虫吃了这种转基因棉花的植株后就会死亡,所以该棉花新品种在1998年推广后,已取得了很好的经济效益。请据上述材料回答下列问题:
(a)毒蛋白对人畜无害,但使棉铃虫致死,从蛋白质的特性看,蛋白质具有______性。
(b)利用苏云金杆菌防治棉铃虫属于生物防治方法,它突出的优点是_______________。
(c)转基因棉花的抗虫变异来源,属于可遗传变异类型中的________________。
(d)题中“毒蛋白基因移入棉花植株内并实现成功表达”中的“成功表达”含义是指
_____________________________________________。
(2)(16分)沼气是一种高效清洁的新能源,农家垃圾在沼气酵即可得到沼气。沼气的主要成分是甲烷,除此还有少量CO、CO2、H2S、H2等。一个10m3左右的沼气池在夏季已足够普通农村家庭使用,在产气量少的冬季也能解决做饭问题。
下面是某课外活动小组在实验室模拟沼气池发酵制沼气并收集甲烷的实验:
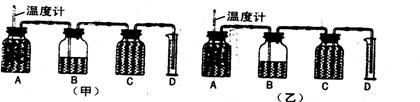
(a)甲、乙两同学分别组装了如图所示两套实验装置,图中瓶A是产生沼气的发酵瓶,瓶B 是洗气瓶(内盛NaOH溶液),瓶C是储气瓶(瓶内盛满水),用于收集甲烷,量筒D用于集水。你认为应该选哪一套装置(填“甲”或“乙”)?_____________。
(b)实验前要首先检查整套装置的_______________。然后,将堆沤过的牛、马粪按比例均匀拦入沼气菌种,放进发酵瓶A内,加满水,B瓶和C瓶也加入试剂或水,连接并密封,几天后即可在瓶C中收集到一瓶较为纯净的甲烷气体。发酵瓶A里微生物的同化作用类型属_______________型,从生态系统的成分看,它们属于_________________________。
(c)洗气瓶B内盛NaOH溶液,作用是______________________。
(d)每天观察并记录,下面是其中三天的实验记录:
| 天 | 温度(℃) | 量筒内收集到的水(mL) |
| 1 | 21 | 30 |
| 2 | 14 | 16 |
| 3 | 11 | 10 |
从上述材料看,影响发酵瓶内产气量的外界因素是――,该因素是通过影响微生物体内的__________的____________能力来影响产气量的。
26.(31分)有A、B、C、D 4种短周期元素。A、B、C为同一周期相邻的3种元素,A和C 的原子序数之比为3:4;A、B、C分别与D形成的化合物的电子总数相等。试回答:
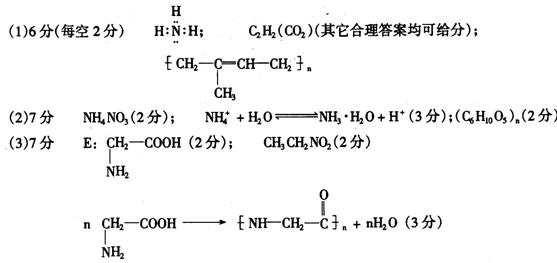
(1)由四种元素中的两种组成的X、Y、Z三种物质,已知X分子的空间构型为三角锥形,该分子的电子式为__________,Y分子的空间构型为直线型,该分子的化学式为__________________________。Z分子为天然高分子化合物(限中学教材范围内),其结构简式为___________________________________________________。
(2)由四种元素中的三种组成的甲、乙两种化合物,甲物质属盐类、其溶液呈酸性,甲物质的化学式为__________,其水溶液呈酸性的原因是__________________;乙物质为常见的天然高分子化合物,其化学式为__________________________________________。
(3)E和F为两种共价化合物,它们均含上述四种元素,且互为同分异构体;它们一个分子中均含有2个A原子。E可发生缩聚反应,F分子中含有40个电子,则E、F的结构简式为
E_________________________ F____________________________
(4)甲物质在农业生产中是为作物提供――元素的主要化肥。植物的根吸收它时要经过_____________和______________两个过程。
由缩聚生成的化合物属于_____________,这类物质是一切生命活动的______________。它在生物体内的合成是受________________控制的。
27.(21分)用下图装置制取和收集气体,根据装置分析后填表(写化学式)
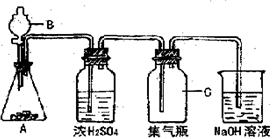
| 编号 | A中物质 | B中物质 | C中气体 |
| (1) | |||
| (2) | |||
| (3) |
写出有关反应的化学方程式
(1)__________________________________________
(2)__________________________________________
(3)__________________________________________
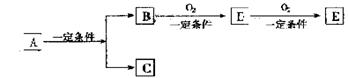
28.(23分)有下列转化关系
(1)若C是可用作自业水消毒的气体,D、E是氧化物,D转化为E时增加氧的质量约是总质量的25.8%,则A是_______________(写化学式),并写出A在一定条件下生成B+C的化学方程式________________________。
(2)若E是酸酐,且为易挥发的晶体,则A是___________________(写化学式),D转化为E的条件是______________________。
(3)若C是水,B是无氧化合物,且在同系物中是分子量最小的化合物;E能使紫色石蕊显红色,则A是_____________________________________(写化学式)。A、B、D、E中易溶于水的是_____________________________________(写化学式)。
写出下列反尖的化学方程式,注明反应类型: 反应类型
①D→E_______________________________________________( )
②B→高分子化合物____________________________________( )
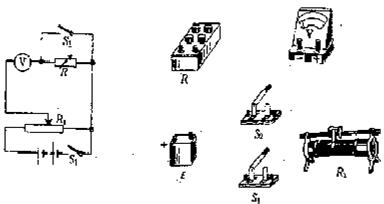
29.(20分)利用如图所示电路测量量程为800mV的电压表的内阻RV,RV给为900Ω。某同学的实验步骤是:
a)按照电路图正确连接好测量电路。将滑动变阻器的滑片移到最右端,电阻箱的阻值调到最大。
b)合上开关S1和S2,调节滑动变阻器R1的滑片位置,使得电压表的指针指到满刻度。
c)合上开关S1,找开开关S2,调节电阻箱R的阻值和滑动变阻器R1的滑片位置,使得电压表指针指到满刻度的一半。
d)读出电阻箱接入电路中的电阻值R,即为电压表内电阻RV的大上。
可供选择的实验器材有
A. 待测电压表:量程为800mV,内阻约900Ω。
B. 滑动变阻器:最大阻值200Ω,额定电流1A
C. 滑动变阻器:最大阻值10Ω,额定电流2A
D.电阻箱:最大阻值999.9Ω,阻值最小改变量为0.1
E. 电阻箱:最大阻值99.9Ω,阻值最小改变量为0.1
F. 电池组:电动势约12V,内阻约1Ω
以及导线和开关等。
按照这位同学设计的实验方法,回答下列问题:
(1)为了使测量比较准确,除了电池组、导线、开关和待测电压表外,从上述器材中还应选用的器材是____________________________(用器材前的序号字母表示)。
(2)在这些器材的实物图上,用铅笔线表示导线,连接成测量电路。
(3)在上述实验步骤中,有遗漏或错误的步骤,请改于下面:
(4)对于用上述方法测出的电压表内阻RV的测量值R测和真实值R真及测量误差,下列说法中正确的是( )
A. R测>R真
B. R测<R真
C. 若RV越大,测量值R测相对于真实值R真的误差就越大
D.若RV越大,测量值R测相对于真实值R真的误差就越小
30.(30分)在磁感应强度为B的匀强磁场中,垂直于磁场的平面上有相距为d的两点P和Q。在Q处有一个质量为M的不带电的液滴,处于静止。质量为m、电量为q的带负电的微粒经电场加速后,从P点垂直于磁感应强度的方向射入匀强磁场后,经过时间![]() ,恰与液滴M相碰。设带电微粒在电场加速前的速度为零。求:
,恰与液滴M相碰。设带电微粒在电场加速前的速度为零。求:
(1) 带电微粒的加速电压是多少?
(2) 若液滴的质量M=3m,带电微粒与液滴撞后即结合成一体,成为带电的液滴,它在碰场中运动轨迹的半径多大?
(3) 要使这个带电微粒从P点射入磁场后,能够在与Q点的液滴相碰,带电微粒的加速电压至少是多大?
31.(31分)燃料电池是将燃料和氧化剂通过电极反应直接将化学能转化电能,它是继水力发电、火力发电、核能发电的第四代发电设备,具有转换效率高,能消除对环境的污染等优点。以氢气作为燃料的电池叫氢燃料电池。美国《时代周刊》将氢燃料电池评为21世纪对人类生活具有重大影响的技术之一。培根电池是一种碱性的氢氧燃料电池,已经应用在“阿波罗六号太空船”上。
(1)在培根电池中,氢氧化钾溶液是电极间的离子带电导体,写出该电池的是电极反应式。
正极:_________________________________________________
负极:_________________________________________________
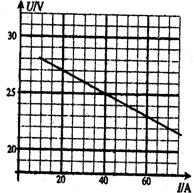
(2)将多个培根电池组合成为电池组,向外供电,电池组工作稳定后,它的电动势和内阻基本保持不变。用实验测出该电池组稳定工作时的路端电压和电流的关系图线如图所示。已知此电池组向外供电的功率是1.2kW。求:电池组的内阻是多大?效率是多少?
丽水地区高三理科综合总复习综合练习(二)
理科综合能力测试参考答案
第一卷(选择题共120分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | C | A | C | C | A | C | B | D | D | A | A | B |
| 题号 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 22 | 23 | 24 |
| 答案 | A | B | C | A | C | B | C | C | D | D | A | D |
第二卷
25.(1)每空2分,共8分
(a) 多样 (b)有利于保护环境(c)基因重组 (d)基因在棉花内成功合成毒蛋白
(2)每空2分,共16分
(a) 乙 (b)气密性;异养;分解者(c)除去沼气中的少量CO2和H2S (d)温度;酶;催化
26.31分
(4)11分 氮(1分);离子交换吸附;主动运输;蛋白质;体现者;基因(每空2分)
27.21分;每空1分,每个化学方程4分(其它合理答案均可给分)
A B C
(1) NaCO3 浓H2SO4 SO2
(2) Cu 浓HNO3 NO2
(3) KmnO4 浓HCl Cl2

(2)列出动量守恒方程得3分,求出半径R1得5分。
(3)求出最小圆半径得4分,求出最小加速电压得4分。
31.(31分)
(1) 正极:O2+2H2O+4e ==== 4OH-
负极:2H2+4OH--4e ==== 4H2O
(2)由图可得输出电流I1=40A,路端电压U1=25V,电流I2=20A时,电压U2=27V。设电池组的电动势为E,内阻为r,有
U1=E-I1r
U2=E-I2r
解得电池组的电动势E=29V,内阻r=0.10Ω。
输出功率为1200W,有
IU=1200
E=U+Ir
解得U=24V(另一根U′=5V舍)
电池组的效率![]()
评分:(1)每个电极反应3分。
(2) 从图中选出两组数据各得2分,列出两个方程得6分,求出电动势和内阻各得3分。共16分。
[另解:应用图象求电动势和内电阻:画出延长图线与纵轴交点得4分,求出电动势得4分;由图象取出两点的坐标各得2分,计算出内阻得4分。]
(3)计算电池组效率,列出方程组给4分,求出路端电压得2分,求出效率再得3分。