高三理综考前热身练
本试卷分第I卷(选择题)和第II卷(非选择题)两部分。第I卷1至4页,第II卷5至10页。考试结束后,将本试题卷和答题卡一并交回。
第I卷
注意事项:
1.答第I卷前,考生务必将自己的姓名、考生号、考试科目涂写在答题卡上。
2.本卷共21题,每题6分,共126分。在每题给出的四个选项中,只有一个选项是最符合题目要求的。
以下数据可供解题时参考:
原子量:H 1 C 12 N 14 O 16 Na 23 P 31 Fe 56 Al 27
一、选择题(本题包括13小题。每小题只有一个选项符合题意,选对的得6分,选错或未选的得0分)
1.某同学在做纤维素消化的实验时,是用刀片将菠菜的叶柄切一小薄片放在载玻片上,滴以蜗牛嗉囊中的消化液,盖上盖玻片;同样制作另一标本,但滴以等量的蒸馏水作为对照组。经过15分钟后,分别观察两标本内的细胞,结果发现两标本内的细胞形态完全一样。他分析了所得的结果与预期不同的原因,下列叙述中,不合理的是
A.实验时温度低,作用时间也不长
B.滴管或实验器皿可能未洗净,残留酸或碱
C.消化液离开蜗牛体内后,不发生作用
 D.取消化液时的蜗牛因温度太低而呈不活动状态,消化液的量很少
D.取消化液时的蜗牛因温度太低而呈不活动状态,消化液的量很少
2.下列四组概念或物质,不能用右图表示其逻辑关系的是
A.免疫系统、T细胞、淋巴细胞
B.酶、胃蛋白酶、蛋白质
C.呼吸作用、无氧呼吸、乳酸发酵
D.有丝分裂、减数分裂、细胞分裂
3、生物学能有今天如此辉煌的成就,离不开众多科学家倾其一生孜孜不倦的研究.下面提及的科学家实验中有精心设置对照实验的是( )
①达尔文提出了以自然选择学说为中心的生物进化理论
②鲁宾和卡门证明了光合作用释放的氧全部来自水
③赫尔希和蔡斯证明了在噬菌体中DNA是遗传物质,而蛋白质不是遗传物质
④艾弗里证明了促使R型菌转化成S型菌的物质是DNA
⑤沃森和克里克提出DNA分子双螺旋结构模型
A、②③④ B、①②③④ C、②③④⑤ D、①③④
4、有人通过观察发现,阴生植物经蒸腾作用散失的水量要比阳生植物经蒸腾作用散失的水量少得多,但阴生植物也没有表现出矿质营养缺乏症。这一现象说明
A、阴生植物需要的水少
B、阴生植物需要的矿质营养少
 C、蒸腾作用对根吸收水分和矿质元素的影响相同
C、蒸腾作用对根吸收水分和矿质元素的影响相同
D根对水分和矿质元素吸收是两个相对独立的过程
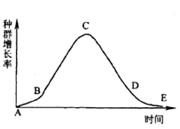
5.根据所给曲线分析,下列描述错误的是
A.在C点是进行海洋捕捞的最佳时期
B.在D点的细菌体内可以形成芽孢
C.在E点种群生长处于稳定期
D.在B―C段内,生存空间没有成为限制种群数量增长的因素
6. NMR(核磁共振)技术已广泛应用于复杂分子结构的的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试推断下列哪组原子均可产生NMR现象
A、元素周期表中第一周期所有元素的原子
B、元素周期表中V A族所有元素的原子
C、18O、31P、119Sn
D、 27Al、19F、12C
7.下列元素一定是主族元素的是
A.原子核外N电子层上只有一个电子的元素
B.原子核外M层电子为偶数的元素
C.原子核外M层电子为小于或等于7的奇数的元素
D.原子核外N层电子为2个的元素
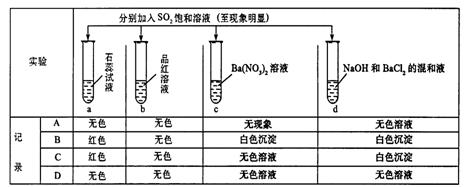
8.下列实验报告记录的实验现象正确的是
 |
9.相对分子质量为a的某物质在室温下的溶解度为b g,此时测得饱和溶液的密度为c g・cm-3,则该饱和溶液的物质的x量浓度是
A.![]() mol・L-1
B.
mol・L-1
B.![]() mol・L-1 C.
mol・L-1 C. ![]() mol・L-1 D.
mol・L-1 D.![]() mol・L-1
mol・L-1
10. 在给定的溶液中,加入对应的一组离子,则该组离子能在原溶液中大量共存的是
A.滴加甲基橙显红色的溶液 I-、NH4+、Cl-、NO3-
B.pH=13的溶液 S2-、SO32-、S2O32-、Na+
C.水电离出来的c(H+)=10-13 mol/L的溶液 K+、HCO3-、Br-、Ba2+
D.含有溶质为NaHSO4的溶液 K+、SiO32-、NO3-、Al3+
11.化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中错误的是
A.电极反应:O2 + 4e- + 2H2O = 4OH-,只能在原电池中发生,不能在电解池中发生
![]() B.硫酸氢钠溶液与等体积等浓度的Ba(OH)2溶液混合的离子方程式:
B.硫酸氢钠溶液与等体积等浓度的Ba(OH)2溶液混合的离子方程式:
2 H+ + SO42-+Ba2+ + 2 OH- =BaSO4 + 2H2O
C.表示中和热的热化学方程式:H+(ag) + OH-(ag) = H2O(l) ;ΔH=-57.3kJ/mol
D.明矾溶于水:Al3+ + 3H2O ![]() Al(OH)3 + 3H+
Al(OH)3 + 3H+
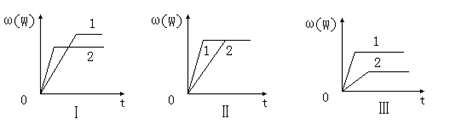 |
12.在一密闭容器中有如下反应:aX(g)+bY(g)
A.图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b> n
B.图Ⅲ可能是不同温度对反应的影响,且T1>T2,ΔH<0
C.图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
D.图Ⅱ可能是在同温同压下催化剂对反应的影响,且1使用的催化剂效果好
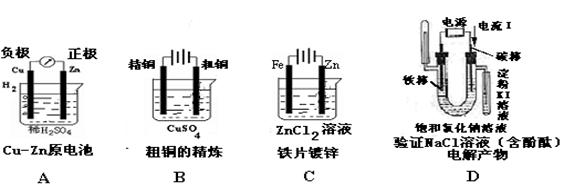
13.下图有关电化学的图示,完全正确的是
二、选择题(本题包括8小题。每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,有错选的得0分)
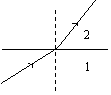 14.光从介质1进入介质2的光路如图所示,由图可知
14.光从介质1进入介质2的光路如图所示,由图可知
A.光在介质1中的波长小于在介质2中的波长
B.在介质1中光子的能量等于在介质2中光子的能量
C.光从介质1射到界面上,只要入射角足够大,就可能发生全反射
D.光在介质1中的传播速度小于光在介质2中的传播速度
15.能源是现代社会生活的物质基础,下列关于能源的论述中错误的是
A.人类消耗常规能源,如煤、石油、天然气等,化学能最终都转化成内能,流散到周围环境中
B.水电站中,水轮机将水流的机械能转化为电能,通过其他装置后,最终又都转化为内能
C.电冰箱消耗了电能才能使热量从低温物体传递到高温物体
D.燃气轮机把燃料燃烧得到的内能全部都转化成机械能
16. 2005年诺贝尔物理学奖授予在光学领域的理论和应用方面作出贡献的美国物理学家格劳伯、霍尔和德国物理学家亨施。霍尔和亨施利用激光进行超精密光谱学测量,完善“光梳”技术做出了重大贡献。所谓的“光梳”是在拥有一系列频率均匀分布的频谱,频谱仿佛一把梳子上的齿或一个尺子上的刻度。下列有关“光梳”的说法正确的是
A.“光梳”是利用光的干涉来测定未知频谱的具体频率
B.“光梳”是利用光的折射来测定未知频谱的具体频率
C.“光梳”是利用原子跃迁光谱来测定未知频谱的具体频率
D.“光梳”是利用一系列频率均匀分布的频谱与未知频谱对比来测定未知频谱的具体频率
 17.质量为m的小物块放在倾角为30º的斜面上,小物块和斜面体一起以速度v沿水平方向向右匀速运动s远,斜面体对于物块的摩擦力和支持力的冲量的大小设为If和IN,和支持力对物块做功的绝对值设为Wf和WN,比较If和IN以及Wf和WN的大小,有
17.质量为m的小物块放在倾角为30º的斜面上,小物块和斜面体一起以速度v沿水平方向向右匀速运动s远,斜面体对于物块的摩擦力和支持力的冲量的大小设为If和IN,和支持力对物块做功的绝对值设为Wf和WN,比较If和IN以及Wf和WN的大小,有
A.If>IN,Wf=WN
B.If<IN,Wf=WN
C.If=IN,Wf>WN
D.If=IN,Wf=WN
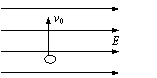 18.如图所示,在水平方向的匀强电场中,将一带正电的小球以初速度v0竖直向上抛出。小球自抛出开始到上升至最大高度的过程中,下列判断不正确的是
18.如图所示,在水平方向的匀强电场中,将一带正电的小球以初速度v0竖直向上抛出。小球自抛出开始到上升至最大高度的过程中,下列判断不正确的是
A.小球的动量的方向不断地变化
B.小球的电势能一直减小
C.小球的重力势能一直增大
D.小球的动能一直减小
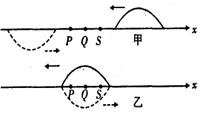 19.如图甲所示,实线和虚线表示两个波长和振幅都相同的简谐横波(各只有半个波形) , 在x轴上分别向左、向右传播。某一时刻两列波的位置如图乙所示, P 、Q、S 表示介质中三个质点的平衡位置,则该时刻
19.如图甲所示,实线和虚线表示两个波长和振幅都相同的简谐横波(各只有半个波形) , 在x轴上分别向左、向右传播。某一时刻两列波的位置如图乙所示, P 、Q、S 表示介质中三个质点的平衡位置,则该时刻
A.P、Q、S都处于各自平衡位置
B.P 、S都处于各自平衡位置, Q 在最大位移处
C. P 的速度向上,Q的速度为零, S 的速度向下
D.P 的速度向下,Q的速度为零, S 的速度向上
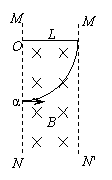 20.如图所示,方向垂直纸面向里的匀强磁场区宽度为L,速率相同的三个粒子分别为质子(
20.如图所示,方向垂直纸面向里的匀强磁场区宽度为L,速率相同的三个粒子分别为质子(![]() ),a粒子(
),a粒子(![]() ),氘核(
),氘核(![]() ),都垂直边界MN飞入匀强磁场区,若a粒子恰能从边界
),都垂直边界MN飞入匀强磁场区,若a粒子恰能从边界![]() 飞出磁场区,那么
飞出磁场区,那么
A.质子和氘核都能从边界![]() 飞出
飞出
B.质子能从边界![]() 飞出,而氘核不能从边界
飞出,而氘核不能从边界![]() 飞出
飞出
C.氘核能从边界![]() 飞出,而质子不能从边界
飞出,而质子不能从边界![]() 飞出
飞出
D.氘核和质子都不能从![]() 边界飞出
边界飞出
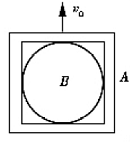 21.如右图所示,小球B刚好放在真空容器A内,将它们以初速度
21.如右图所示,小球B刚好放在真空容器A内,将它们以初速度![]() 竖直向上抛出,下列说法中正确的是
竖直向上抛出,下列说法中正确的是
A.若不计空气阻力,上升过程中,B对A的压力向上
B.若考虑空气阻力,上升过程中,B对A的压力向上
C.若考虑空气阻力,上升过程中,B对A的压力向下
D.若不计空气阻力,上升过程中,B对A的压力向下
第Ⅱ卷
(非选择题 共174分)
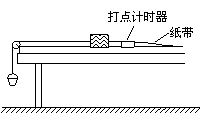 22.⑴(6分)测量木块与长木板间的动摩擦因数的实验装置如图所示,长木板处于水平,装砂的小桶通过细线绕过定滑轮与木块连接,细线的长度大于桌面的高度,木块可以拖动纸带运动,打点计时器在纸带上打下一系列的点。
22.⑴(6分)测量木块与长木板间的动摩擦因数的实验装置如图所示,长木板处于水平,装砂的小桶通过细线绕过定滑轮与木块连接,细线的长度大于桌面的高度,木块可以拖动纸带运动,打点计时器在纸带上打下一系列的点。
实验时接通打点计时器的电源,放手后,装砂小桶带动木块一起运动,小桶与地面接触之后,木块还要在木板上继续运动一段距离后停下,打点计时器在纸带上打下一系列的点,如图所示。纸带的左端与木块相连,并用虚线框标出了A、B两个区域,为了求得木块与长木板间的动摩擦因数,应选取_____区域的数据计算出木块运动的加速度的大小(用a表示),由此计算动摩擦因数的公式是μ=__________。
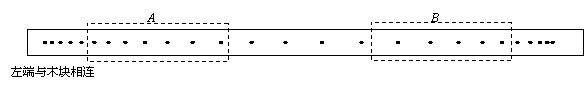 |
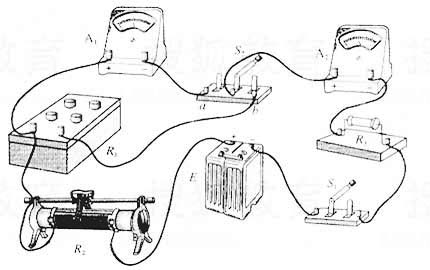
(2)(11分)为了测定电流表A1的内阻,采用如图所示的电路。其中
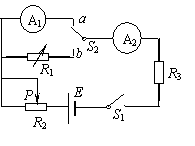 A1是待测电流表,量程为300μA,内组约为100Ω;
A1是待测电流表,量程为300μA,内组约为100Ω;
A2是标准电流表,量程是200μA;
R1是电阻箱,阻值范围0~999.9Ω;
R2是滑动变阻器;
R3是保护电阻;
E是电池组,电动势为4V,内阻不计;
S1是单刀单掷开关,S2是单刀双掷开关。
(1)根据电路图,请在下面实物图中画出连线,将器材连接成实验电路。
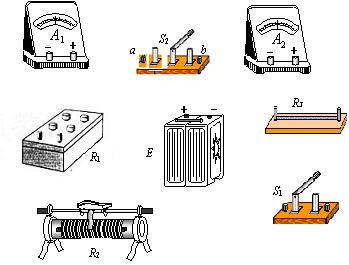
(2)连接好电路,将开关S2扳到接点a处,接通开关S1,调整滑动变阻器R2使电流表A2的读数是150μA;然后将开关S2板到接点b处,保持R2不变,调节电阻箱R1,使A2的读数仍为150μA。若此时电阻箱各旋钮的位置如图3所示,电阻箱R1的阻值是_______Ω,则待测电流表A1的内阻Rg= _______Ω。
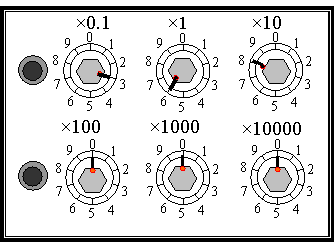 |
(3)上述实验中,无论怎样调整滑动变阻器R2的滑动端位置,都要保证两块电流表的安全。在下面提出来供的四个电阻中,保护电阻R3应选用___________(填写阻值相应的字母)。
A.200kΩ B.30 kΩ C.20 kΩ D.15 kΩ
(4)下面提供最大阻值不同的四个滑动变阻器供选用。既要满足上述实验要求,又要调整方便,滑动变阻器________(填写阻值相应的字母)是最佳选择。
A.25kΩ B.10 kΩ C.5 kΩ D.1 kΩ
23.(16分)2005年10月12日上午9时,“神舟六号”在长征2号F运载火箭的推动下飞向太空,飞船先在距近地点200km、远地点350km的椭圆型轨道上运行5圈后变轨进入到距地面343km的圆形轨道上绕地球飞行。与10月17日凌晨,返回舱顺利着陆。
为使问题简化,现设地球的半径为R,地球表面的重力加速度为g,地球自转周期为T,飞船做圆轨道飞行时距地面高度为H,求:飞船进入圆轨道做匀速圆周运动时的周期为多少?其轨道半径与地球同步卫星轨道半径之比为多少?(用以上字母表示)
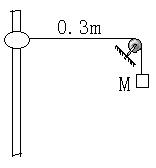 24.(19分)轻绳一端挂一质量为M的物体,另一端系在质量为m的圆环上,圆环套在竖直固定的细杆上,定滑轮与细杆相距0.3m,如图所示,将环由静止释放,圆环沿杆向下滑动的最大位移为0.4m。若不计一切摩擦阻力,求:
24.(19分)轻绳一端挂一质量为M的物体,另一端系在质量为m的圆环上,圆环套在竖直固定的细杆上,定滑轮与细杆相距0.3m,如图所示,将环由静止释放,圆环沿杆向下滑动的最大位移为0.4m。若不计一切摩擦阻力,求:
(1)物体与圆环的质量之比;
(2)圆环下落0.3m时的速度大小(g取10m/s2)
 25. (20分)如图所示,两根不计电阻的倾斜平行导轨与水平面的夹角θ=37o ,底端接电阻R=1.5Ω。金属棒a b的质量为m=0.2kg。电阻r=0.5Ω,垂直搁在导轨上由静止开始下滑,金属棒a b与导轨间的动摩擦因数为μ=0.25,虚线为一曲线方程y=0.8sin(
25. (20分)如图所示,两根不计电阻的倾斜平行导轨与水平面的夹角θ=37o ,底端接电阻R=1.5Ω。金属棒a b的质量为m=0.2kg。电阻r=0.5Ω,垂直搁在导轨上由静止开始下滑,金属棒a b与导轨间的动摩擦因数为μ=0.25,虚线为一曲线方程y=0.8sin(![]() x)m与x轴所围空间区域存在着匀强磁场,磁感应强度.B=0.5T,方向垂直于导轨平面向上(取g=10m/s2,sin37o=0.6,cos37o=0.8)。求:
x)m与x轴所围空间区域存在着匀强磁场,磁感应强度.B=0.5T,方向垂直于导轨平面向上(取g=10m/s2,sin37o=0.6,cos37o=0.8)。求:
(1).当金属棒a b下滑的速度为![]() m/s 时,电阻R上消耗的电功率是多少?
m/s 时,电阻R上消耗的电功率是多少?
(2)若金属棒a b从静止开始运动到Xo=6 m处,电路中消耗的电功率为0.8w,在这一过程中,安培力对金属棒a b做了多少功?
26(14分).已知A、C、D、E均为单质气体,G、H均为化合物气体,B、M均为金属单质,常温下W是无色无味的液体。请回答下列问题:
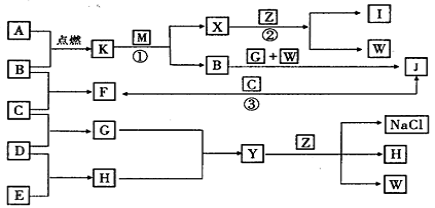 |
(1)写出下列物质的化学式:
A 、E 、Z 、Y ;
(2)若反应①转移24mole-时,生成还原产物的质量为 g;
(3)写出反应②的化学方程式: ;
(4)写出反应③的离子方程式: ;
(5)把I溶液加热、蒸发、蒸干,再加强热后,得到的固体产物中一定有_________ (填化学式);
(6)某金属与稀硝酸恰好完全反应生成NO,消耗金属和硝酸的物质的量之比为1∶3,则该金属可能是M和B中的 (填化学式)。
27(14分).已知A、B、C是第二周期的非金属元素,其原子序数依次增大,且它们之间可以形成AC和BC以及AC2和BC2分子,D元素是一种短周期元素,它与A、B、C可分别形成电子总数相等的三种分子.
请填空:
(1) 写出A、B、C、D对应的元素符号:A.______、B.______、C.______、D._____.
(2) 写出工业生产中BD3与氧气反应的化学方程式:__________________________.
(3) 你认为B、C、D元素形成的化合物之间能否_____________(填:“能”或“不能”)发生下面的反应BC+BD3→DBC2+D2C,得出上面结论的理由是__________________
Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g)![]() 4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
4AC2(g)+B2(g)在上述条件下,向容器中充入AC和BC2各1mol达平衡时,生成AC2和B2共amol,则AC的转化率是_____________(用含a的代数式表示);
Ⅱ.若维持温度不变,在一个与Ⅰ反应前的起始体积相同容积固定的密闭容器中发生Ⅰ中所述的化学反应,开始时仍向容器中充入AC和BC2各1mol,达平衡时生成AC2和 B2共bmol,将b与Ⅰ中的a进行比较,则a_____b(填“>”、“<”、“=”或“不能确定”
 28.(20分)
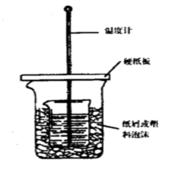
28.(20分)
(1)50mL1.0mol・L-1盐酸跟50mL1.1mol・L-1氢氧化钠溶液
在右图装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热。试回答下列问题:
①该实验装置有3处明显错误,分别是:
A ,B , C 。
②大小烧杯间如果不填满碎纸屑或塑料泡沫,对求得中和热
的数值有何影响?
A.偏低 B.偏高
C.无影响 D.无法判断
③当实验装置改正好后再做实验。
若改用60mL1.0mol・L-1盐酸跟50mL1.1mol・L-1氢氧化钠溶液进行反应,与上述实验相比,所放出的热量将 ,所求中和热数值将 。
A.偏低 B.偏高 C.相等 D.无法判断
④若用相同浓度和体积的氨水代替上述实验中的氢氧化钠溶液,测得中和热的数值
A.偏低 B.偏高 C.相等 D.无法判断
(2)我国化学家侯德榜,成功地改进了国外纯碱的生产工艺,发明了联合制碱法。用其生产线所生产的纯碱中往往含有少量杂质氯化钠。
①为检验产品Na2CO3中含有杂质氯化钠,可取少量试样溶于水后,再滴加 ;观察到的现象是 。
②若起始时取试样ag,U型管(装有碱石灰)的质量为bg,请你利用下列装置完成纯碱试样中Na2C03的质量分数的测定。
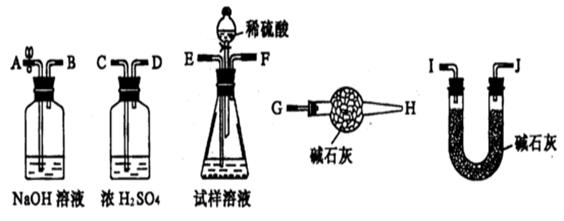
Ⅰ.实验时,各装置管口的连接顺序从左到右依次为A→B→E→F→C→D→1→J→G-→H,其中盛有浓硫酸的装置作用是 ,G→H的干燥管作用是 。
Ⅱ.反应前,先要从A处缓缓鼓人一定量的空气后再连接U型管等仪器,其目的是 ;反应后,若不从A处缓缓鼓人一定量的空气,将导致测试结果______(填“偏大”、“偏小”或“不变”)。
Ⅲ。若反应完全后,最终U型管的质量为:99,则试样中纯碱的质量分数的计算式为 。
 29.(12分)
29.(12分)
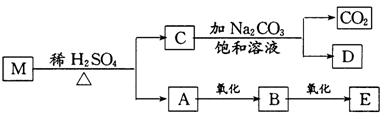
由碳、氢、氧三元素组成的化合物M是预防心血管疾病的一种新药。M可发生如下变化:
已知B的蒸气密度是H2的22倍,并可发生银镜反应,M的相对分子质量为174,化合物C
中氧元素质量分数为54.2%,取一定质量的化合物C完全燃烧生成CO2和水的物质的量之比为4:3。试解答下列问题:
(1)写出下列化合物的结构简式:
B:_______;A:_________;E:________。
(2)化合物C分子中碳、氢、氧原子个数之比为N(C):N(H):N(O)=__________。
(3)M的分子式是:_________________________.
(4)写出符合上述框图转化关系的M的可能有的结构简式:________________________
30、.(22分)1999年4月23日,在广州中山医科大学第一附属医院,我国首例试管婴儿出生,该女婴的父母身体健康。女婴的母亲7年前生下一男婴,孩子一岁后发病,最后死于脑出血。5年后,她第二次怀孕,怀孕6个月时,到医院抽羊水及脐带血诊断,发现胎儿是男孩,而且是血友病患者,遂引产。夫妇二人最后来到中山医院大学附属医院做试管婴儿。医生培养了7个可做活体检查的胚胎,并抽取每个胚胎1―2个细胞进行检查后,选择了两个活体胚胎进行移植,最后一个移植成功。据此资料回答下列问题:
(1)试管婴儿技术作为现代生物技术和母亲正常怀孕、生产的过程的相同之处是______________________ ______________________________
不同点在于____________________________ ____。
(2)血友病的遗传方式为___________________________________,如果用B和b表示正常基因和血友病基因,则父、母亲的基因型分别是______ 和______。如果该夫妇再生一男孩,患血友病的概率是_____________。
(3)医生抽取活检胚胎的1或2个细胞后,可通过观察______________判断早期胚胎的性别,你认为医生应选用_________性胚胎进行移植,原因是 。 应用现代生物技术,现在人们已能够选取最理想的胚胎,其基因型应该是_______。自然状态下,出现这样的胚胎的概率是_______。该实例体现了现代科学技术应用于社会和人类生活的重要意义。
31.(20分)下图表示氮循环与动物体内有机物部分代谢途径,请分析回答:
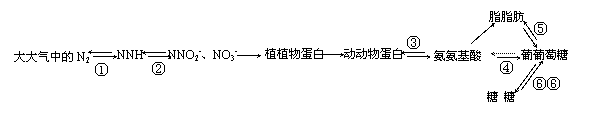
(1)完成①、②过程的微生物分别是_______________、________________。
(2)完成③过程的细胞器是_________________。
(3)进行④过程首先要经过_______作用。促进⑤、⑥过程的激素分别是_____________、
____________________。
(4)某些微生物能够完成①过程,关键是由于有_________酶。
假如科学家想利用基因工程的方法,将编码该酶的基因转移到小麦胚细胞中,获取该基因的途径:一是从微生物的DNA分子直接分离,二是_________________________;
假如已经知道组成该酶的氨基酸序列,从理论上讲能不能准确确定其基因编码区的碱基序列?_____________,原因是______________________________________________,这对于生物体的生存有什么意义?_____________________________________________。
![]() (5)NO3-被吸收进入植物体内后,必须经过下列还原反应,生成NH3才能被植物体利用合成蛋白质:
(5)NO3-被吸收进入植物体内后,必须经过下列还原反应,生成NH3才能被植物体利用合成蛋白质:
①若将水稻幼苗培养在硝酸盐溶液中,则体内生成硝酸还原酶;若将水稻幼苗培养在无硝酸盐的培养液中,硝酸还原酶消失。这种现象说明硝酸还原酶是( )
A.还原酶 B.水解酶 C.组成酶 D.诱导酶
②给你提供两株生长状况相同的植物幼苗及药品、用具,请你设计一个实验,通过可观察现象验证钼是组成硝酸还原酶的必需元素,并预期实验现象。
步骤:
预期现象:
高三理综考前热身练
tx参考答案及评分标准
1、C 2、B 3、A 4、 D 5、B 6.B 7.C 8.B 9.A 10.B 11.B 12.D 13.D
14.B15.D16.D 光梳”是拥有一系列频率均匀分布的频谱,与未知频谱比较测定的未知频谱的具体频率。17.B 18.D 19.AC 20C
21.B 若不计空气阻力,上升过程中,整体发求加速度g,然后对B分析受力,A.B间作用力为零,若考虑空气阻力,上升过程中,整体法求加速度a>g,然后对B分析受力可知A对B的压力向下,反之B对A的压力向上.
22.⑴B μ=a/g
(2).(8分)
|
(2)86.3(1分) 86.3(1分)
(3)C(2分)
(4)B(2分)
23.解:设飞船周期为T1则![]() ……①
……①
在地表任一物体:![]() GM=gR2……②
GM=gR2……②
由①②得:![]() 由
由![]()
![]()
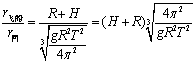
24.M:m=2:1 0.72
25.(20分)解析:考点:动能定理、串联电路、闭合电路的欧姆定律、电功、电功率、电磁感应现象、感应电动势。正弦交流电、交流电的最大值与有效值.。
(1).金属板作切割磁感线运动,产生感应电动势E
E=Byv ① (1分)
由曲线方程
y=0.8sin(![]() x)m
②
(1分)
x)m
②
(1分)
由①②式联解得
E=0.4![]() sin(
sin(![]() x)v 正弦交流电
(1分)
x)v 正弦交流电
(1分)
电动势的最大值 Em=0.4![]() ③
(1分)
③
(1分)
电动势的有效值 E有=![]() ④
(1分)
④
(1分)
电路的总电阻 R总 = R+r ⑤ (1分)
根据闭合电路的欧姆定律 I=![]() ⑥
(1分)
⑥
(1分)
电阻R上消耗的电功率PR
PR=I2R ⑦ (2分)
由① ~ ⑦ 式联解得 PR=0.06w (1分)
(2).金属棒a b从静止开始运动至X0=6m处,曲线方程
y′=0.8sin(![]() X0)m
⑧
(2分)
X0)m
⑧
(2分)
设金属棒在X0处的速度为V′,切割磁感线运动产生感应电动势为E′
E′=B y′V′ ⑨ (1分)
此时电路中消耗的电功率为P′
P′=![]() ⑩
(2分)
⑩
(2分)
此过程中安培力对金属棒做功为W安,根据动能定理
mgsin370•S -μmgcos370
•S- W安 = ![]() m V′2
m V′2 ![]() (3分)
(3分)
由⑧ ~![]() 式联解得 W安 = 3.8 J
式联解得 W安 = 3.8 J
评析:本题以电磁感应现象为背景材料,考查学生力学、电磁学的综合应用能
26.(14分,(1)每空1分,其余每空2分)
(1)A.O2 E。N2 Z。NaOH Y。NH4Cl
(2)504
(3)Al2O3+2NaOH=NaAlO2+H2O
(4)2Fe2++Cl2=2Fe3++2Cl-
(5)NaAlO2
(6)Fe
27.(14分)(1)A.C、B.N、C.O、D.H (2)4NH3+5O2![]() 4NO+5H2O
4NO+5H2O
(3)不能;在此反应关系中,只有失电子的物质,没有得电子的物质
(4)Ⅰ.80a%;Ⅱ.>
28.(20分)
(1)(每空1分)
①无环形玻璃搅拌棒 大小烧杯的口未平齐 大小烧杯间纸屑或塑料泡沫未填满
②A ③B、C ④A
(2)〔②Ⅰ3分,其余每空2分〕
①硝酸酸化的AgN03溶液 有无色无味的气体和白色沉淀生成
②Ⅰ.吸收CO2中水 防止外界CO2和水进入并与外界大气相通
Ⅱ。排出装置内的CO2 偏小
Ⅲ.![]()
29.(1)B:CH3CHO(1分);A:C2H5OH(1分);E:CH3COOH(1分)
(2)N(C):N(H):N(O)=2:3:2(2分)
![]() (3)C8H14O4(3分) COOCH2CH3
(3)C8H14O4(3分) COOCH2CH3
(4)CH2COOCH2CH3(2分)CH3-CH (2分)
![]() COOCH2CH3
COOCH2CH3
CH2COOCH2CH3
解析:(1)由M(B)=2×22=44且能发生银镜反应知B是CH3CHO,由B是CH3CHO可推知A是C2H5OH,E是CH3COOH,由C+Na2CO3→D+CO2知C是羧酸,M是酯。
(2)由n(CO2):n(H2O)=4:3,易知n(C):n(H)=2:3,设n(C)=4 mol,则n(H)=6mol可求出C分子中氧元素质量为:m(O)=![]() ×(48+6)g=64 g,所以,n(O)=
×(48+6)g=64 g,所以,n(O)=![]() =4 mol
=4 mol
所以羧酸C分子中:n(C):n(H):n(O)=4:6:4=2:3:2,C的最简式为C2H3O2,设其分子式为(C2H3O2)n,则C羧酸中N(C):N(H):N(O)=2:3:2。
(3)酯M的相对分子质量为174>羧酸C的相对分子质量,若n=3,则(C2H3O2)3相对分子质量为177,大于酯M的相对分子质量174,故n<3,经讨论n=2符合题意。C的分子式为C4 H6O4。其可能有的结构简式为:
![]()
![]() CH2COOH COOH
CH2COOH COOH
![]() CH3-CH
CH3-CH
CH2COOH COOH
易知酯M的分子式为C8H14O4。
(4)酯M符合题给转化框图关系,可能有的结构简式为:
![]()
![]() CH2COOC2H 5 COOC2H5
CH2COOC2H 5 COOC2H5
![]() CH3-CH
CH3-CH
CH2COOC2H 5 COOC2H5
30、.(22分)
(1)双亲产生的两性生殖细胞融合为受精卵 试管婴儿是“体外受精”后产生的受精卵(1分),初步发育后再进行“胚胎移植”的产物(1分)。
(2)X染色体隐性遗传 XBY XBXb (顺序不能颠倒) 50%
(3)性染色体形态 女 女性胚胎从父亲那里接受XB基因, 表现型正常 XBXB 25%
31. (20分)
(1)固氮菌(根瘤菌) 硝化细菌
(2)核糖体
(3)脱氨基 胰岛素 胰高血糖素(肾上腺素)
(4)固氮酶 人工合成基因 不能 每种氨基酸对应有多种不同密码子
在一定程度上避免个别碱基改变而导致遗传信息的损失
(5)①D
②步骤:(其他回答要包含相关内容)
分别配制含有植物必须矿质元素、不含NH4+的完全培养液(A)和缺钼、缺NH4+的“完全培养液”(B)(2分);
将两株生长状况相同的植物分别培养在A、B培养液中(2分);两组实验给予相同、适宜的外界条件(2分)
预期现象:“A”组:正常生长;“B”组:缺氮现象(植株矮小、叶片发黄,叶脉呈淡棕色)(2分)