中考模拟演练(二)
注意事项:
1.本试题分第I卷和第II卷两部分。第I卷2页为选择题,18分;第II卷4页为非选择题,32分;共50分。考试时间为60分钟。
2.考生答第I卷前务必将自已的姓名、准考证号、考试科目用铅笔涂写在答题卡上,考试结束,试卷和答题卡一并收回。
3.第I卷每题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,必须用橡皮擦干净后,再选涂其它答案,不能答在试卷上。
第I卷(选择题 共18分)
一、选择题(本题包括12小题,1~6小题每题1分,7~12小题每题2分,共18分。每小题只有一个选项符合题意。)
1.下列变化中,属于化学变化的是
A.冰雪融化 B.用石墨制金刚石 C.胆矾研碎 D.空气液化制氧气
2.为了减少大气污染,许多城市推广汽车使用清洁燃料。目前使用的清洁燃料有一类是压缩天然气。下列有关天然气的说法中不正确的是
A.天然气的主要成分是氢气
B.燃烧天然气不是酸雨的重要成因之一
C.天然气是当今世界最重要的三大化石燃料之一
D.天然气与煤、柴油相比是较清洁的能源
3.蔬菜、水果中含有维生素C(C6H8O6),它能促进人体生长发育,增强人体对疾病的抵抗力,下列关于维生素C的说法中错误的是
A.维生素C由6个碳元素,8个氢元素、6个氧元素组成
B.一个维生素C分子由6个碳原子、8个氢原子、6个氧原子构成
C.保持维生素C化学性质的最小粒子是维生素C分子
D.青少年应多吃蔬菜、水果,切忌偏食
4.下列物质的用途与其化学性质无关的是
A.用熟石灰改良酸性土壤 B.用盐酸除去铁制品表面的铁锈
C.用一氧化碳冶炼金属 D.用干冰进行人工降雨
5.某雨水样品刚采集时测得pH值为4.82,放在烧杯中经2h(“小时”的符号)后,再次测得pH值为4.68,原因是雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4。下列关于雨水样品的说法中正确的是
A.雨水样品酸性逐渐减弱 B.雨水样品酸性强弱未变
C.雨水样品酸性逐渐增强 D.无法判断
6.近几年我国的沙尘暴频繁出现,不仅对环境污染,而且也造成了财产的巨大损失。气象学认定:凡水平方向有效能见度小于1km的风沙现象称为沙尘暴,下列关于沙尘暴的说法中不正确的是
A.沙尘暴是尘沙被风吹起所致
B.沙尘暴能造成严重的大气污染,使人易患呼吸道疾病
C.沙尘暴对植物光合作用没有影响,叶片嫩芽的呼吸作用和蒸腾作用正常进行
D.种树种草加大防护林建设,提高森林覆盖率和退耕还林是防治风沙的有效途径
7.粗盐中所含的杂质主要是MgCl2。工业上常把粗盐晶体粉碎后用饱和食盐水浸洗,再滤出食盐,对此,下列说法正确的是
A.浸洗前后,被浸洗的食盐中MgCl2的含量不变
B.浸洗前后,食盐水的组成不变
C.浸洗用的饱和食盐水可以无限次地使用下去
D.粗盐粉碎的颗粒大小,直接影响浸洗后的食盐中MgCl2的含量
8.下列操作或实验装置正确的是

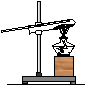

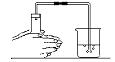
A.制取O2 B.检查装置的气密性 C.CO还原CuO D.制取H2
9.有一瓶无色溶液,可能含有Na2SO4、NaNO3和Na2CO3中的一种或几种,为了鉴别它,做了下列实验:(1)取1—2ml该溶液注入试管中,滴入BaCl2溶液,产生白色沉淀;(2)再取1—2ml该溶液于另一支试管中,滴入稀硫酸,产生气泡。则该溶液中一定含有
A.Na2SO4 B.NaNO3 C.Na2CO3 D.Na2SO4和Na2CO3
10. 食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是:①检验自来水中是否含氯离子 ②鉴别食盐和纯碱 ③检验鸡蛋壳能否溶于酸 ④除去热水瓶中的水垢
A.①② B.①③ C.①④ D.②③④
11.近几年新型抗高血压药不断被研制出来,“寿比山”就是一种新型的常用的抗高血压药,其相对分子质量是365.5。已知该药物中碳的质量分数为52.53%,则每个“寿比山”分子中碳原子个数为
A.12 B.16 C.6 D.无法计算
12.将下列物质各10g分别投入到90g水中,都完全溶解。最终所得溶液中溶质的质量分数为10%的是
A.Na2O B.CuSO4·5H2O C.NaCl D.SO3
第Ⅱ卷(非选择题 共32分)
注意事项:
1.第Ⅱ卷共4页,用钢笔或圆珠笔直接答在试卷上。
2.答卷前将密封线内的项目填写清楚。
| 题 号 | 二 | 三 | 四 | 总 分 |
| 分 数 |
相对原子质量:H-1 C -12 N-14 O-16 S-32 Na-23 Mg-24 Ca-40 Cu-64
Zn-65 Cl-35.5 Ag-108
| 得分 | 评卷人 |
|
|
|
二、填空与简答题(本题共包括6小题,共16分)
13.(2分)实验室制取有毒的氯气时,常用氢氧化钠溶液来吸收多余的氯气,其反应的化学方程式为:Cl2+2NaOH = NaCl+ NaClO(次氯酸钠)+H2O。工业上常用氯气和消石灰为原料制取漂白粉[其主要成分是次氯酸钙Ca(ClO)2]。
(1)在Ca(ClO)2中氯元素的化合价是 价;为保护环境,可用 吸收制漂白粉的废气。
(2)仿照上面的化学方程式,写出氯气和消石灰发生反应的化学方程式:
;
14.(1分)列举家庭日常生活中常见的物质各一种(写化学式):酸 ,盐 。
15.(3分)汽车作为推动人类文明向前迈进的现代社会产物,在给人类带来便捷舒适的同时,对自然生态环境的恶化也有难以推卸的责任。城市中,汽车持有量逐年增长,空气质量面临如汽车污染等问题的考验。同时我国的能源危机也逐步呈现出来,我国2004年的石油进口量超过1亿吨,三分之一对外依存。未来10年净进口需求将按年均10%的速度增长。请回答下列问题:
(1)汽车尾气中的主要大气污染物是 (写化学式) ;
(2)请提出一条我省治理汽车污染的合理化建议 。
(3)为了节约、开发能源,请提出你的一条合理化建议 。
16.(3分)某溶液中仅含有AgNO3和Cu(NO3)2两种溶质,将其分为A、B两份,各加入一定量的铁粉,充分反应后,过滤洗涤,分别得到滤渣和滤液。
(1)将A得到的滤渣加入到稀盐酸中有气泡产生,则该滤渣中含有的物质是:
(填化学式,下同)。
(2)往B得到的滤液中滴稀盐酸,有白色沉淀生成,则对应的滤渣中含有:
,滤液中含有的溶质是
17.(3分)有A、B、C三种物质,已知A为一种氯化物,B为一种钠盐,C为一种可溶性碱。下图表示的是A、B、C的溶液两两反应的实验现象。请根据有关实验现象回答:
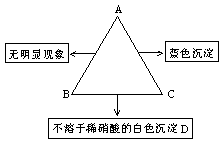
(1)A的化学式__________________;D的化学式__________________;
(2)B与C反应的化学方程式:________________________________________;
(3)A溶液与洁净的铁钉反应的化学方程式:_____________________________。
18.(4分)某学校新建了食堂,为防止使用塑料包装袋、一次性饭盒造成的污染,学校从市场上购买了一批铝制饭盒蒸饭用。为了方便管理需给饭盒编号,并刻上学生姓名,为此学校特向学生征求设计方案。试讨论下列有关的问题。
(1)起初有人建议直接在饭盒上用油漆喷字,但是该建议没有被采纳,你认为没有被采纳的理由是什么?
(2)你能否利用初中化学所学的知识,设计一种最佳的“饭盒留字”方案?
(3)为了教育学生爱惜粮食,学校打算在饭盒上刻上一些“警言”。你有什么创意?
(4)有的老师说,为了保护学生的健康应停止使用铝饭盒。你认为这种观点对吗?为什么?
| 得分 | 评卷人 |
|
|
|
三、实验题(本题包括2小题,共10分)
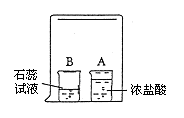
19.(3分)在烧杯A中装入20mL浓盐酸。在烧杯B中装入10mL紫色的石蕊试液。用一只大烧杯把A、B两烧杯罩在一起(如右图)。过几分钟后,看到小烧杯B中装的溶液变成红色。
提出问题:上述现象说明了什么?
对上述现象的看法不一,可能作出不同的假设。请你仔细阅读下表中的示例,然后填写表中空格。
| 作出假设 | 实验探究 | |
| 示例 | B烧杯中的溶液要过一会儿才变色,与A烧杯无关。 | 用洁净烧杯C配好20mL石蕊试液。静置,观察现象。 |
| 1 | 大烧杯壁上沾某种物质,散发出的肉眼看不见的粒子与B烧杯中的溶液接触,使其变红 | |
| 2 |
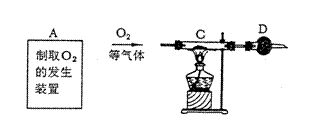 20.(7分)某课外活动小组对红色铜粉(含炭)样品进行实验,所用装置如右图所示(图中部分仪器装置已略去)。
20.(7分)某课外活动小组对红色铜粉(含炭)样品进行实验,所用装置如右图所示(图中部分仪器装置已略去)。
回答下列问题:
(一)实验目的
(二)实验用品
仪器:大试管、硬质玻璃管、干燥管、酒精灯、铁架台等。
药品:红色铜粉(含炭)样品、氯酸钾、二氧化锰、碱石灰(固体NaOH和CaO的混合物,对某些气体如CO2、水蒸气等具有很强的吸收能力)等。
(三)实验内容
| 实验步骤 |
| 化学方程式 |
| 检查装置的气密性。在A中装入制氧气药品,称量wg样品装入C中,称量D(碱石灰和干燥管,下同)的质量为m1g。连接好仪器装置。 |
| |
| 对A进行加热 | ||
| 对C进行加热。当C中药品充分反应后,停止加热。 | ||
| 冷却后,称量D的质量为m2g |
|
|
(四)计算:红色铜粉样品中铜的质量分数= (用含w、m1、m2的代数式表示)
(五)问题和讨论
实验完毕后,老师评议说,按以上设计进行实验,即使C中反应完全,D中吸收完全,也得不出正确结果。经讨论,有同学认为应在A和C之间加一装置,再次实验后,得到了较正确的结果。在A和C之间应加入的装置是 。
| 得分 | 评卷人 |
|
|
|
四、计算题(本题包括2小题,共6分)
21.(1分)由氮、氧两种元素组成的化合物中,其氮、氧元素的质量比为7︰20。通过计算可知化合物的化学式为
22.(5分)小明到三亚旅游,带回一瓶海水。为了知道海水中氯化物(假设以NaCl计算)的含量,他进行了如下操作:取海水样品5g,向其中滴加AgNO3溶液至沉淀不再产生为止。过滤、干燥,得沉淀0.4g。请你根据以上数据,帮助他计算出海水中氯化物(以NaCl计算)的质量分数(计算结果保留2位小数)。
中考模拟演练(二)参考答案
第I卷(选择题 共18分)
| 题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 答案 | B | A | A | D | C | C | D | B | C | D | B | C |
第Ⅱ卷(非选择题 共32分)
13.(1)+1;NaOH溶液 (2) 2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
14.CH3COOH;NaCl(其它答案符合题意也可)
15.(1)CO;(2)使用天然气或乙醇汽油;(3)更多的利用太阳能。
16.(1) Fe、Cu、Ag (2) Ag;AgNO3、Cu(NO3)2、Fe(NO3)2
17.(1)CuCl2;BaSO4 (2)Na2SO4+Ba(OH)2 = BaSO4↓+2NaOH (3)Fe+CuCl2 = FeCl2+Cu
18.(1)油漆易脱落,污染食品。
(2)用毛笔蘸取稀盐酸(或稀硫酸)写上名字,过一会儿用水冲洗干净即可。
(3)节约每一颗粮食。(或谁知盘中餐,粒粒皆辛苦等等符合题意即可)
(4)正确。因为人体摄入铝元素过量,易得痴呆症,1989年世界卫生组织把铝确定为食品污染源之一,而加以控制使用。
19.分子是不断运动的。
| 作出假设 | 实验探究 | |
| 1 | 另取一只烧杯,重新配制紫色的石蕊试液,将其单独放在大烧杯里,观察现象 | |
| 2 | 烧杯A中的浓盐酸,散发出一种肉眼看不见的粒子,慢慢滴溶解到B烧杯紫色的石蕊试液中,使紫色的石蕊试液变红 | 小心闻烧杯A中的溶液的气味,取少量的石蕊试液注入试管中,滴入浓盐酸,观察现象。 |
20.(一)测定样品中铜的质量分数
(三)实验内容
| 实验现象 | 化学方程式 |
|
| |
| 红褐色的粉末变为黑色 | 2Cu+O2 |
(四)![]()
(五)干燥管内装碱石灰(或加干燥装置内装浓硫酸)
21.N2O5
22.3.26%
 实验现象
实验现象