08届高考化学猜题卷
命题人:刘敬 审核人:鹿守亮
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23
P-31 Mg-24 Ca-40 Ba-137 S-32
一、单项选择题(本题包括8小题,每小题3分,共24分。每小题只有一个选项符合题意)
1.下列有关新闻报道你认为基本属实的是
A.最新消息,美国夏威夷联合天文中心的科学家发现了新氢微粒,该微粒是由3个氢原子核(只含质子)和2个电子构成,是氢元素的一种同素异形体
B.研究发现,气体分子中的极性键在红外线的照射下,易像弹簧一样作伸缩和弯曲运动,从而产生热量。所以N2O气体属于温室效应气体
C.“嫦娥一号”成功发射,标志我国已具有深太空探测能力。据科学家预测,月球的土壤中存在着大量的氦元素,其存在方式和地球一样主要是以![]() 的形式存在。
的形式存在。
D.据2007年12月18日的《新民晚报》报道,上海市从12月17日起空气质量日报中增加了氮氧化物这种污染气体的预报
2. 下列表示物质的化学用语正确的是
A.NH4H的电子式:![]() B.硝基苯的结构简式:
B.硝基苯的结构简式:![]()
C.葡萄糖的实验式:CH2O D.甲烷分子的比例模型: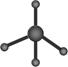
3.下列各组离子可能大量共存的是
A.不能使酚酞试液变红的无色溶液中:Na+、CO![]() 、K+、ClO-、AlO
、K+、ClO-、AlO![]()
B.能与金属铝反应放出氢气的溶液中: K+、NO![]() 、Cl-、NH
、Cl-、NH![]()
C.常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO![]()
D.中性透明溶液:K+、HCO![]() 、NO
、NO![]() 、Fe3+、SO42-
、Fe3+、SO42-
4.分析推理是化学学习方法之一。下列实验推理中,正确的是
A.金属的冶炼方法与金属的活泼性有很大的关系,所以银和汞可以用热分解的方法冶炼
B.某雨水的pH小于5.6,说明雨水中一定溶解了SO2
C.糖尿病人应少吃含糖的食品,某八宝粥中注明未加糖,所以糖尿病人可以放心食用
D.将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼
5.下列实验操作或对实验事实的描述中正确的说法共有( )
①燃着的酒精灯不慎碰翻失火,可立即用湿布盖灭
②滴定用的锥形瓶和滴定管都要用所盛溶液润洗
③分液时,分液漏斗中下层液体从下口流出,上层液体从上口倒出
④配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
⑤不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
⑥用托盘天平称量时,所称药品均可放在纸上,并置于天平的左盘
⑦测定溶液的pH时,可用洁净、干燥的玻璃棒蘸取溶液,滴在pH试纸上,再与标准比色卡比较
⑧浓硝酸与浓盐酸均易挥发,故均应保存在棕色试剂瓶中,并置于阴凉处
⑨配制一定物质的量浓度的溶液,定容时俯视容量瓶的刻度线,会使所配溶液的浓度偏高
⑩可以用酸式滴定管量取20.00mL0.1000mol·L-1KMnO4溶液
A.4个 B.5个 C.6个 D.7个
|
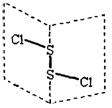
A.S2Cl2的电子式为![]()
B.S2Cl2为含有极性键和非极性键的非极性分子
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2与H2O反应的化学方程式可能为:
2S2Cl2+2H2O=SO2↑+3S↓+4HCl
7.用下列四种装置制备和收集Cl2:
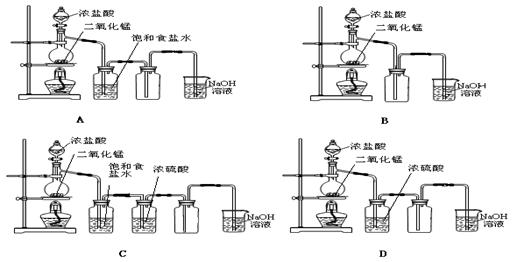
将收集到Cl2置于天平上称量,若四个集气瓶体积相同、质量相等,则称量结果是
A.A最重 B.B最重 C.C最重 D.D最重
8.已知同一碳原子连有两个羟基不稳定: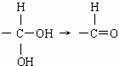 。有机物
。有机物 是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快。下列有关该有机物的说法不正确的是
是选择性内吸传导性除草剂,俗称稗草烯,主要用于水稻田防除稗草,温度和湿度对药效影响大,温度高、湿度大药效发挥快。下列有关该有机物的说法不正确的是
A.属于卤代烃,能使酸性高锰酸钾溶液和溴水褪色
B.该物质既有对映异构,也有顺反异构
C.在碱性条件下充分水解,可生成羧酸盐
D.1mol 该物质在一定条件下可与4molH2发生加成反应
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给2分,选两个且都正确的给4分,但只要选错一个,该小题就为0分。)
9.下列离子方程式书写正确的是
A.氨水吸收少量的二氧化硫:NH3·H2O + SO2 = NH4+ + HSO3-
B.用两个铜片作电极电解盐酸:Cu + 2H+ ![]() H2↑+ Cu2+
H2↑+ Cu2+
C.用石墨作电极电解AlCl3溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.Na2O2加入到足量H218O中:2Na2O2+2H218O = 4Na++4OH-+18O2↑
10.“XYn”表示不同卤素之间靠共用电子对形成的卤素互化物 (非金属性:X<Y), 其化学性质和卤素单质相似。下列说法中,正确的是
A.ICl与水反应可生成 HCl 和 HIO,则1mol ICI 参加反应转移电子为 1mol
B.某温度,液态 IF5电离:2IF5≒ IF4+ +IF6-, 则 c (IF4+)×c (IF6-) 是一个常数
C.BrCl与 Zn 反应生成 ZnCl2 和 ZnBr2 D.XYn 与卤素单质一样都是非极性分子
11.下列比较中,正确的是
A.已知0.1 mol/L的二元酸H2A溶液的pH = 4.0,则在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
B.0.2 mol•L-l NH4CI 和 0.l mol•L-l NaOH 溶液等体积混合后:
c(NH4+) > c (Cl―)) > c (Na+) > c (OH-) >c (H+)
C.0.1mol/L的醋酸的pH=a,0.01mol/L的醋酸的pH=b,则a+1>b
D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,
[c(Na+)-c(F-)]< [c(K+)-c(CH3COO-)]
12.设NA为阿伏加德罗常数,下列说法中正确的是
A.标准状况下,1L液态水中含有的H+ 数目10-7NA
B.足量Zn与一定量的浓硫酸反应,产生22.4L气体时,转移的电子数为2NA
 C.常温常压下,含有NA 个NO2分子的气体质量为4.6g
C.常温常压下,含有NA 个NO2分子的气体质量为4.6g
D.14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
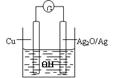
13.普通水泥在固化过程中自由水分子减少并产生,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的是
A.工业上以黏土、石灰石为主要原料来制造水泥
B.测量原理示意图中,Ag2O为负极
C.负极的电极反应式为:2Cu+2OH—-2e—=Cu2O+H2O
D.电池工作时,OH-向正极移动
 14.合成氨反应:N2(g)
+ 3H2(g)
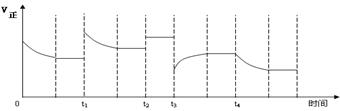
14.合成氨反应:N2(g)
+ 3H2(g) ![]() 2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
2NH3(g) △H=-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
下列说法正确的是
A.t1时升高了温度
B.t2时使用了催化剂
C.t3时减小了压强
D.t4时降低了温度
三、(本题包括2小题,共22分)
15.(10分)从含银、铜、金和铂的金属废料中提取金、银、铂的一种工艺如下:
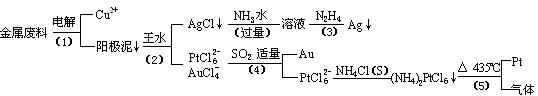
根据以上工艺回答下列问题:
(1)电解时,以金属废料为阳极,纯铜为阴极,CuSO4溶液为电解液,写出电解反应的阳极方程式: :
(2)写出步骤(4)的离子反应方程式:
;
(3)金和浓硝酸反应的化学方程式为:Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O
但该反应的平衡常数很小,所以金和浓硝酸几乎不反应,但金却可以溶于王水,试简要解释之: 。
(4)我们知道,稀盐酸与铜不反应。在稀盐酸中加入H2O2等氧化剂后,则可使铜顺利溶解。某同学未加入氧化剂,而是设计了一个实验装置,也能使铜溶于稀盐酸。请在方格中画出该装置:
(5)分别将等质量的铜片与分别等体积、过量的浓硝酸、稀硝酸反应,所得到的溶液前者呈绿色,后者呈兰色,甲同学提出可能是Cu2+浓度不同引起的,乙同学提出溶液呈“绿色”是溶液中Cu2+与NO2共存的结果,请你设计实验探究甲乙两同学的说法谁更正确(简述实验方案和实验现象及由此得出的结论:
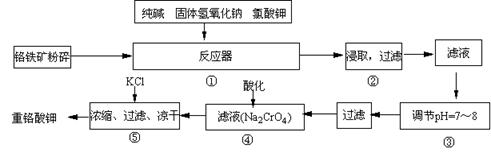
16.(12分)重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3
+ 24NaOH +7KClO3![]() 12Na2CrO4
+ 3Fe2O3 +7KCl + 12H2O,
12Na2CrO4
+ 3Fe2O3 +7KCl + 12H2O,
试回答下列问题
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
。
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: 。
(3)操作③的目的是什么,用简要的文字说明: 。
(4)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①判断达到滴定终点的依据是: ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品的中重铬酸钾的纯度(设整个过程中其它杂质不参与反应) 。
四、(本题包括2小题,共18分)
17.(10分) (1) 水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
(2)随着人类对水的研究的不断深入,水的应用也越来越广泛。研究人员最近发现,在一定的实验条件下,给水施加一个弱电场,在20℃、1个大气压下,水可以结成冰,称为“热冰”。“热冰”有许多实用价值,如开发新药、用于纳米打印机等,还可能用来
(填写序号)
A.代替干冰 B.防止冰川熔化 C.在室温下制作冰雕 D.建室温溜冰场
(3)在灾害性事故中,骨折时有发生,通常用石膏来固定骨折部位。石膏可分为熟石膏(CaSO4·![]() H2O,一种白色粉末)和生石膏(CaSO4·2H2O,一种坚硬的固体)两种,医生使用的石膏是 (填分子式或名称)。石膏定型时发生的化学反应方程式
。
H2O,一种白色粉末)和生石膏(CaSO4·2H2O,一种坚硬的固体)两种,医生使用的石膏是 (填分子式或名称)。石膏定型时发生的化学反应方程式
。
(4)火星探测车在火星大气中检测到了气体A。资料显示,A分子是三原子分子,其相对分子质量为60,在地球环境下A易分解。粉未状的KSCN与浓硫酸在一定条件下可得到气体A和二种硫酸氢盐,,生成物的物质的量之比是1∶1∶1。则气体A的结构式是 。
(5)新型离子化合物[HC60]+[CB11H60Cl60]-是一种功能材料。它可以用超酸H(CB11H60Cl60)和C60反应,使C60得到质子来制取。该反应类型跟中学课本中的一个化学反应类似,课本中的这个反应是(写一个化学方程式) 。
18.(8分)甲醇(CH3OH)是一种重要的化工原料,合成甲醇的主要反应为:
CO(g)+2H2(g)![]() CH3OH(g) ΔH
< 0。
CH3OH(g) ΔH
< 0。
Ⅰ.在一定条件下,上述反应在一密闭容器中达到平衡。
(1)体积不变的条件下,下列措施中有利于提高CO的转化率的是 _______(填字母)。
A.升高温度 B.增大压强 C.通入CO D.通入H2
(2)在保证H2浓度不变的情况下,增大容器的体积,平衡____________(填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的理由是________________________
Ⅱ.原料气的加工过程中常常混有一定量CO2,为了研究不同温度下CO2对该反应的影响,以CO2、CO和H2的混合气体为原料在一定条件下进行实验,结果表明,原料气各组分含量不同时,反应生成甲醇和副产物甲烷的碳转化率是不相同的。实验数据见下表:
| CO2%-CO%-H2% (体积分数) | 0–30–70 | 2–28–70 | 4–26–70 | 8–22–70 | 20–10–70 | |||||||||||
| 反应温度/℃ | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | 225 | 235 | 250 | |
| 碳转化率(%) | CH3OH | 4.9 | 8.8 | 11.0 | 36.5 | 50.7 | 68.3 | 19.0 | 33.1 | 56.5 | 17.7 | 33.4 | 54.4 | 8.0 | 12.0 | 22.6 |
| CH4 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 2.8 | 2.8 | 2.8 | |
(3)由上表数据可得出多个结论。
结论一:在一定条件下,反应温度越高,碳转化率__________。
结论二:_____________________________________________
(4)为了验证结论二,有科学家又用以下五组不同组成的原料气再次进行实验。
| 组别 | 体积分数(%) | |||
| CO | CO2 | H2 | N2 | |
| 第1组 | 19.7 | 0.0 | 59.1 | 21.2 |
| 第2组 | 20.7 | 0.3 | 62.1 | 16.9 |
| 第3组 | 16.9 | 1.3 | 50.7 | 31.1 |
| 第4组 | 19.8 | 5.5 | 59.4 | 15.3 |
| 第5组 | 20.3 | 10.9 | 60.9 | 7.9 |
进行该验证实验时,控制不变的因素有________________、_________________、____________________________________________等。
五、(本题包括1小题,共12分)
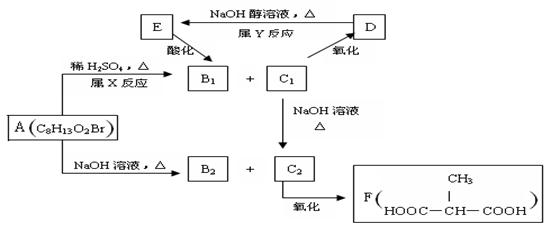
19.(12分)Ⅰ.某化合物A在一定条件下能发生如下图所示的转变:
其中只有B1既能使溴水褪色,又能与Na2CO3 溶液反应放出CO2 ,回答下列问题:
(1)指出反应类型:X 反应,Y 反应。
(2)物质A的结构简式为 。
(3)写出C1 ![]()
![]() C2的化学方程式
。
C2的化学方程式
。
(4)与F互为同分异构体且核磁共振氢谱只有一种峰的有机物的结构简式有 。
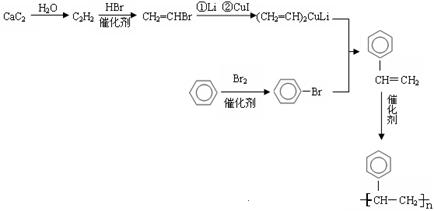
Ⅱ.已知,卤代烃之间能发生反应:
C4H9Cl ![]() (C4H9)2CuLi
(C4H9)2CuLi![]() C4H9-C2H5
C4H9-C2H5
聚苯乙烯是一种生活中常见的塑料,试以碳化钙、苯为基本有机原料,无机原料自选,在下列方框中用合成反应流程图合成聚苯乙烯
流程图示例:A ![]()
![]() B
B
六、(本题包括1小题,共8分)
20.自然界存在着一种白云石的矿石,其化学式是xCaCO3·yMgCO3。以它为原料,可制取耐火材料等。
(1)称取27.6g白云石,加热到质量不再变化,可以生成耐火材料MgO多少mol?(用x、y的代数式表示)
(2)若在上述反应中,收集到CO26.72L(标准状况下),试写出白云石的化学式(取x、y的最小正整数比)。
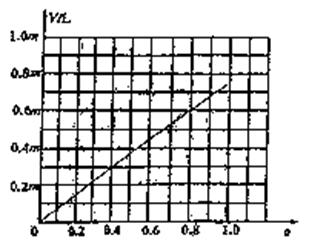
![]() (3)若称取白云石mg,研碎后与过量炭粉混合,放在特定仪器中隔绝空气强热一段时间后,测得白云石分解率为a,生成VL(标准状况)一氧化碳。试计算V为多少L(标准状况)?(用m、a代数式表示)
(3)若称取白云石mg,研碎后与过量炭粉混合,放在特定仪器中隔绝空气强热一段时间后,测得白云石分解率为a,生成VL(标准状况)一氧化碳。试计算V为多少L(标准状况)?(用m、a代数式表示)
![]()
|
2MgO+5C Mg2C3+2CO)
请在下图中画出V和a的关系图。
八、(本题包括1小题,共12分)
下列两题分别对应于“物质结构与性质”和“实验化学”两个选修课程模块的内容,请你选择其中一题作答,如果两题全做,则按A题评分。
|
|
21.(A)【物质结构与性质】
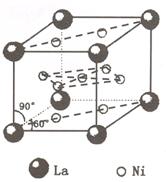
氢是新型清洁能源,但难储运。研究发现,合金可用来储藏氢气。镧(![]() ) 和镍(
) 和镍(![]() ) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,
) 的一种合金就是储氢材料。该合金的晶胞如右图,镍原子除一个在中心外,
其他都在面上,镧原子在顶点上。储氢时氢原子存在于金属原子之间的空隙中。
(1)一定条件下,该贮氢材料能快速、可逆地存储和释放氢气,若每个晶胞可吸收 3 个 H2, 这一过程用化学方程式表示为: 。
(2)下列关于该贮氢材料及氢气的说法中,正确的是 ( 填序号 )
A.该材料中镧原子和镍原子之间存在化学键,是原子晶体
B.氢分子被吸收时首先要在合金表面解离变成氢原子,同时放出热量
C.该材料贮氢时采用常温高压比采用常温常压更好
D.氢气很难液化是因为虽然其分子内氢键很强,但其分子间作用力很弱
![文本框: I、镍常见化合价为+2、+3, 在水溶液中通常只以+2 价离子的形式存在。 +3价的镍离子具有很强的氧化性,在水中会与水或酸根离子迅速发生氧化还原反应。
II、在Ni2+的溶液中加入强碱时,会生成 Ni(OH)2沉淀,在强碱性条件下,该沉淀可以被较强的氧化剂 (如 NaClO) 氧化为黑色的难溶性物质 NiO(OH) 。
III、镍易形成配合物如 Ni(CO)6、[Ni(NH3)6] 2+ 等。](/attachimg/tkgzhx/08jiegao225/image069.gif) E.己知镧和镍的第一电离能分别为 5.58eV、7.64eV, 可见气态镧原子比气态镍原子更容易变成+1 价的气态阳离子
E.己知镧和镍的第一电离能分别为 5.58eV、7.64eV, 可见气态镧原子比气态镍原子更容易变成+1 价的气态阳离子
(3)某研究性学习小组查阅的有关镍及其化合物的性质资料如下:
①写出 Ni3+ 的核外电子排布式:
②写出将NiO(OH) 溶于浓盐酸的离子方程式:
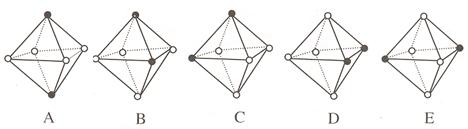
(4)Ni(CO)6为正八面体结构,镍原子位于正八面体的中心,配位体CO在正八面体的六个顶点上。若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是 。 ( 填字母编号,任填一组 )( 图中黑点为NH3,圆圈为CO,Ni略去)
(5)将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式: 。
21.(B)【实验化学】
阿斯匹林(乙酰水杨酸)是由水杨酸和乙酸酐合成的:
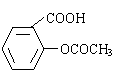
 +
(CH3CO)2O
+
(CH3CO)2O ![]()
![]()
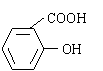
 + CH3COOH
+ CH3COOH
|
在生成乙酰水杨酸的同时,水杨酸分子之间也能发生聚合反应,生成少量聚合物(副产物)。合成乙酰水杨酸的实验步骤如下:
①向150 mL干燥锥形瓶中加入2 g水杨酸、5 mL乙酸酐和5滴浓硫酸,振荡,待其溶解后,控制温度在85℃~90℃条件下反应5~10 min,然后冷却,即有乙酰水杨酸晶体析出。
②减压过滤,用滤液淋洗锥形瓶,直至所有晶体收集到布氏漏斗中。抽滤时用少量冷水洗涤晶体几次,继续抽滤,尽量将溶剂抽干。然后将粗产品转移至表面皿上,在空气中风干。
③将粗产品置于100 mL烧杯中,搅拌并缓慢加入25 mL饱和碳酸氢钠溶液,加完后继续搅拌2~3 min,直到没有二氧化碳气体产生为止。过滤,用5~10 mL蒸馏水洗涤沉淀。合并滤液于烧杯中,不断搅拌,慢慢加入15 mL 4mol / L盐酸,将烧杯置于冰水中冷却,即有晶体析出。抽滤,用冷水洗涤晶体1~2次,再抽干水分,即得产品。
请回答下列问题:
⑴第①步中,要控制温度在85℃~90℃,应采用的加热方法是 ,用这种方法加热需要的玻璃仪器有 。
⑵在第②步中,用冷水洗涤晶体,其目的是 、 。
⑶在第③步中,加入饱和碳酸氢钠溶液的作用是 ,加入盐酸的作用是 。
⑷如何检验产品中是否混有水杨酸? 。
2008年江苏高考猜题卷
参考答案
1、B 2、C 3、、C 4、A 5C 6、B 7、C 8、B 9、B 10、BC 11、C 12、D 13、AC 14、BC
15.题答案:(10分)(每空2分)
(1)Cu—2e— =Cu2+
(2)2AuCl4— + 3SO2 + 6 H2O = 2Au + 8Cl— + 3SO42— + 12H+
(3)王水中含有大量的Cl—,Au3+与Cl—可生成AuCl4—,使该平衡中Au3+浓度降低,平衡正移,金即可溶于王水。
(4)电解装置,铜与电源的正极相连即可.若加硝酸钾或用铜与碳相连构成原电池可给1分.
(5)理论:等质量的铜片与等体积、过量的浓硝酸、稀硝酸反应,所得溶液中Cu2+的浓度基本相等;实验:将一定量的NO2通入铜片与稀硝酸反应后的溶液中,若溶液呈绿色,则乙同学的结论正确,反之,不正确。若加水不给分.(其他合理答案也给分)
16.(12分)
(1)Al2O3 + Na2CO3![]() 2NaAlO2 +CO2↑;(2分)
2NaAlO2 +CO2↑;(2分)
(2)NaFeO2 + 2H2O = Fe(OH)3↓ + NaOH(2分)。
(3)由于溶液在硅酸钠和偏铝酸钠发生水解,降低pH值有利于水解平衡向正反应方向移动,当pH调到7~8时,使它们水解完全,从而除去SiO32-和AlO2-。(共2分)
(4)2CrO42-+2H+ ![]() Cr2O72-+H2O(2分)
Cr2O72-+H2O(2分)
(5)①当滴加最后一滴硫代硫酸钠溶液,溶液蓝色褪去,半分钟内不复现(2分)
②94.08%(2分)。
17、(共10分)
(1)A (2) CD (3) S=C=O(2分)
(4) 熟石灰(1分) 2CaSO4·![]() H2O+3H2O===2CaSO4·2H2O(2分)
H2O+3H2O===2CaSO4·2H2O(2分)
(5) NH3+HCl===NH4Cl(2分)
18.(8分)
(1)BD(2分)
(2)C
(1分) 该反应达到平衡时,平衡常数K=![]() ,增大容器体积时,c(CH3OH)和c(CO)等比例减小,由于H2浓度不变,此时
,增大容器体积时,c(CH3OH)和c(CO)等比例减小,由于H2浓度不变,此时![]() 的值仍然等于K,所以平衡不移动。(1分)
的值仍然等于K,所以平衡不移动。(1分)
(3)越高(1分)
原料气含少量CO2有利于提高生成甲醇的碳转化率,CO2含量过高碳转化率又降低且有甲烷生成。(1分)
(4)温度 压强 CO和H2的体积分数之比 (2分)
19、(共12分)
(1) 取代(或水解) 消去(每空1分)
(2)
|
 (2分)
(2分)
(3)
|
 + NaOH
+ NaOH
|
 +
NaOH (2分)
+
NaOH (2分)
(4)
|

|
 (2分,对1 个即可)
(2分,对1 个即可)
(5)(4分。到(CH2=CH)2CuLi给2分,到苯乙烯给3分,到聚苯乙烯给4 分,漏条件整体扣1 分)
20.(共8分)
(1)(2分)n(MgO)=27.6y/ (100x+84y)
(2)(2分)CaCO3·MgCO3
(4)(4分)∵CaO~CO MgO~CO CO2~2CO
∴CaCO3·MgCO3~6CO
|
21.(共12分)
(1)LaNi5
+ 3H2 ![]() LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
LaNi5H6;(2分,不配平不给分,化学式不正确不给分,可逆符号写等号扣一分)
(2)CE (2分,每选对一个给一分,每错选一个倒扣一分,扣完本小题分为止)
(3)①[Ar]3d7;或![]() (2分,写成3d7不给分)
(2分,写成3d7不给分)
②2NiO(OH) + 6H++2Cl- =2Ni2++Cl2↑+4H2O;(2分,未配平不给分,氯气未写气体符号扣一分)
(4)A和B(或A和C、A和D、B和E、C和E、D和E任一组均可);(2分,若同组中出现同种物质则不给分,例如AE、BC……等)
(5)Cu2++4H2O=[Cu(H2O)4]2+ (2分)
21(B)
⑴ 水浴(1分); 温度计、酒精灯、烧杯(3分)
⑵除去晶体表面附着的可溶性杂质(1分)、减少阿斯匹林的溶解(1分)
⑶使阿斯匹林转化为可溶性盐(2分); 将阿斯匹林的可溶性盐重新转化为阿斯匹林(2分)
⑷向水中加入少量产品,滴加氯化铁溶液,若有紫色出现,说明产品中含有水杨酸(2分)。