高考化学选择易错题3
1.氢元素与其他元素形成的二元化合物称为氢化物,下面关于氢化物的叙述正确的是
A.一个D2O分子所含的中子数为8 B.沸点:LiH>NaH
C.HCl的电子式为H+[![]() ]- D.熔沸点:HCl<HF
]- D.熔沸点:HCl<HF
2.下列有关说法正确的是
A.H2SO4的酸性比HClO的酸性强,所以S的非金属性比Cl强
B.Mg(OH)2是中强碱,Al(OH)3是两性氢氧化物,所以Al的金属性比Mg强
C.H2O加热到1000℃开始分解,H2S加热到300℃开始分解,则O的非金属性比S强
D.用Na、Mg分别做与水反应的实验,可以比较它们的金属性强弱
3.能证明CH3COOH为弱电解质的实验是
① 分别测定浓度均为0.1mol·L-1的HCl溶液和CH3COOH溶液的pH;② 分别向浓度均为1mol·L-1的HCl溶液和CH3COOH溶液中投入大小外观基本相同的Zn粒;③ 测定一定浓度的CH3COONa溶液的pH;④ 将1.0mol·L-1的HCl溶液和1.0mol·L-1的CH3COOH溶液分别稀释100倍,并分别测定两种溶液稀释前后的pH;⑤ 将等浓度盐酸和醋酸分别滴加到等浓度的Na2CO3溶液中。
A.除⑤外均可以 B.只有①和③ C.全部 D.只有②和⑤
4.2.8gFe全部溶于一定浓度、100mL的HNO3溶液中,得到标准状况下的气体1.12L,测得反应后溶液的pH为1。若反应前后溶液体积变化忽略不计,则下列有关判断不正确的是
A.反应前HNO3溶液的浓度为2.0mol·L-1 B.1.12L的气体全部为NO
C.反应后溶液中c(NO3-)=1.6mol·L-1 D.反应后的溶液最多还能溶解1.61gFe
5.Na2O2、CaC2、CaH2、Mg3N2都能与水反应,且反应中均有气体放出。下列说法中正确的是
A.都属于氧化还原反应
B.Na2O2、CaC2与水反应时水作氧化剂
C.CaC2、Mg3N2与水反应属复分解反应
D.CaH2与水反应时产生H2,它既是氧化产物又是还原产物
6.现有两种不含结晶水的盐,它们在不同温度下的溶解度分别是:
20℃ 50℃
A的溶解度 35.7g 46.4g
B的溶解度 31.6g 108g
下列说法中正确的是:
A.提纯A物质最好可采用重结晶的方法
B.若把108gB的饱和溶液从50℃降到20℃,析出的B是76.4g
C.提纯B物质最好可采用重结晶的方法
D.两种盐在某一温度下可能具有相同的溶解度
7.![]() 在一密闭容器中,反应mM(气) nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则
在一密闭容器中,反应mM(气) nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则
A.平衡逆向移动; B.物质M的转化率增大;
C.n > m D.物质N的质量分数减少
8.在某容积可变的密闭容器中,可逆反应A(g) + B(g) ![]() xC(g) 符合下列图中所示关系。由此推断对图II的正确说法是
xC(g) 符合下列图中所示关系。由此推断对图II的正确说法是
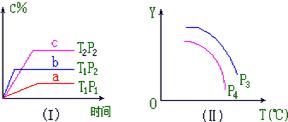 |
A.p3<p4,Y轴表示B的质量分数 B.p3>p4,Y轴表示A的转化率
C.p3>p4,Y轴表示混合气体的平均摩尔质量 D.p3<p4,Y轴表示混合气体的密度
9. 将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果。用数轴表示的下列化学知识中不正确的是
![]() A.常温条件下,酚酞的变色范围:
B.分散系的分类:
A.常温条件下,酚酞的变色范围:
B.分散系的分类:
C.AlCl3和NaOH溶液反应后铝元素的存在形式: D.CO2与NaOH溶液反应的产物:
10.在一定条件下利用电解的方法可以将含有少量的Fe、Zn、Cu、Pt等金属杂质的粗镍提纯。下列叙述正确的是(已知氧化性:Fe2+<Ni2+<Cu2+)
A.纯镍作阴极
B.阳极发生还原反应
C.粗镍连接电源的正极,其电极反应为:Ni2++2e—== Ni
D.电解后,电解槽底部有含有Cu和Pt等金属杂质的阳极泥
11.干燥剂的干燥性能可用干燥效率(1m3空气中实际余留水蒸气的质量)来衡量。某些干燥剂的干燥效率数据如下:
| 物质 | 干燥效率 | 物质 | 干燥效率 |
| MgO | 0.008 | ZnCl2 | 0.8 |
| CaO | 0.2 | ZnBr2 | 1.1 |
分析以上数据,下列有关叙述错误的是
A.MgO的干燥性能比CaO好 B.干燥效率可能与干燥剂的阴、阳离子的半径大小有关
C.MgCl2可能是比CaCl2更好的干燥剂
D.上述干燥剂中阳离子对干燥性能的影响比阴离子小
12.化合物A、B、C、D各由两种元素组成,甲、乙、丙是三种单质。这些常见的化合物与单质之间存在如下关系(已知化合物C是一种有机物),
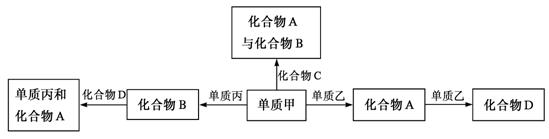 |
以下结论不正确的是
A.上图所示的五个转化关系中,有三个是化合反应
B.上述转化关系所涉及的化合物中有一种是电解质
C.甲、乙、丙三种单质的晶体均是分子晶体
 D.上图所示的五个转化关系中,均为放热反应
D.上图所示的五个转化关系中,均为放热反应
12.A、B两种物质的饱和溶液的质量分数随温度变化的曲线如图。
现分别在50g A和80 g B中各加水150 g,加热溶解后并都蒸发掉水
50 g ,冷却到t1℃,下列叙述正确的是
A.t1℃时溶液中A、B的质量分数相等
B.t1℃时溶液中A的浓度小于B的浓度
C.t1℃时析出固体B
D.t1℃时两者均无固体析出
13.11.9g金属锡跟100mL12mol·L-1HNO3共热一段时间。完全反应后测定溶液中c(H+)为8mol·L-1,溶液体积仍为100mL。放出的气体在标准状况下体积约为8.96L。由此推断氧化产物可能是
A.SnO2·4H2O B.Sn(NO3)4 C.Sn(NO3)2 D.Sn(NO3)2和Sn(NO3)4
14.下列各组物质中,不是按![]() (“→”表示一步完成)关系相互转化的是
(“→”表示一步完成)关系相互转化的是
| 选项 | A | B | C | D |
| A | Na2S2O3 | CH2=CH2 | Al(OH)3 | HNO3 |
| B | SO2 | CH3CH2OH | NaAlO2 | NO |
| C | Na2SO4 | CH3CH2Br | Al2O3 | NO2 |
15.在有乙离子存在的情况下,欲用试剂甲来检验溶液中是否含有乙离子,下表所加试剂甲能够对乙离子进行检验的是:
| 选项 | 试剂甲 | 乙离子 | 丙离子 |
| A | HCl、BaCl2 | SO42- | SO32- |
| B | AgNO3 | Cl― | I- |
| C | KSCN | Fe2+ | Fe3+ |
| D | NH3·H2O | Al3+ | Ag+ |
16.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入HCl气体6.72L(S.T.P),忽略反应过程中溶液得体积变化,则
A.反应过程中得到6.72L(S.T.P)的气体 B.最终得到7.8g的沉淀
C.最终得到的溶液中c(NaCl)=1.5mo/L D.最终得到的溶液中c(Na+)=c(Cl-)+c(OH-)
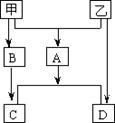 17.甲、乙是两种常见短周期元素的单质,其有关物质转化如图所示,其中C为白色沉淀,D为气体。则下列说法不正确的是
17.甲、乙是两种常见短周期元素的单质,其有关物质转化如图所示,其中C为白色沉淀,D为气体。则下列说法不正确的是
A.若D为酸性气体,则A可能为Al2S3
B.甲、乙两物质生成的化合物发生水解反应不可能生成两种酸
C.D可能为碱性气体
D.B与水反应可能生成Mg(OH)2沉淀
18.可逆反应A(g)+ B(s) ![]() 2C(g)+Q(Q>0)进行至t时刻,发现C的百分含量仍在增大,此时要增大正反应的速率,可采取的措施是
2C(g)+Q(Q>0)进行至t时刻,发现C的百分含量仍在增大,此时要增大正反应的速率,可采取的措施是
A.增大B物质的量 B.升温 C.减压 D.使用适宜催化剂
19.4.下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为
“doggycene”,有关doggycene的说法正确的是
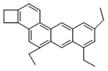
A.该分子中所有碳原子可能处于同一平面
B.doggycene的分子式为:C26H30
C.1mol该物质在氧气中完全燃烧生成CO2和水的物质的量之比为2:1
D.该物质常温为气态.
20.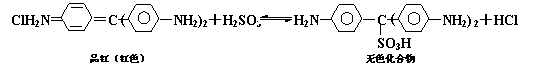 Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:
Cl2、SO2均能使品红溶液褪色。后者因为品红分子结构中的发色团遇到亚硫酸后结构发生改变,生成不稳定的无色化合物。其漂白原理可用下面的反应方程式表示:
下列说法正确的是
A.品红溶液中同时通入Cl2、SO2,漂白效果会更好
B.加热可判断品红褪色是通入SO2还是通入Cl2引起的
C.“无色化合物”分子中,19个碳原子都可能在同一平面上
D.品红分子结构中,19个碳原子都可能在同一平面上