中学化学《化学基本理论》摩尔溶液
基础习题
选择题
1.用CuSO4・5H2O制备0.1摩/升硫酸铜溶液,正确的方法是----------(C)
A.将25克CuSO4・5H2O溶于1升水中
B.把16克CuSO4・5H2O溶于1升水中
C.把25克CuSO4・5H2O溶于适量水中,室温时稀释至1升
D.把25克CuSO4・5H2O加热除去全部结晶水,再配成1升溶液
2.设NA为阿佛加德罗常数,200毫升Ba(NO3)2溶液中含Ba2+和NO3-总数为0.45NA,则该溶液的摩尔浓度为-------------------------------------------------(B)
A.2.25摩/升 B.0.75摩/升 C.1.5摩/升 D.6.75摩/升
3.有三种不同浓度的稀硫酸,体积比依次为3:2:1,它们分别与等物质的量的K2CO3、KHCO3、Al刚好完全反应,此三种硫酸的摩尔浓度比为---(C)
A.1:1:1 B.6:2:3 C.4:3:18 D.2:1:3
4.已知以下两个反应:
![]()
欲从银氨溶液中转化出大量的Ag+,适宜的试剂是----------------------------------(B)
A.H2SO4 B.HNO3 C.HCl D.NaOH
5.在20℃时,K2SO4饱和溶液的摩尔浓度为0.62摩/升,密度为1.08克/厘米3。现取该溶液1升,加热蒸发掉100毫升水后,冷却至0℃,析出K2SO443.52克,则0℃时K2SO4的溶解度是----------------------------------------------------(C)
A.43.52克 B.0.62克 C.7.38克 D.10.5克
6.25℃1.01×105帕下,使V升氯化氢气体溶于水得V升水溶液,关于这种溶液的叙述正确的是---------------------------------------------------------------(D)
A.溶液的摩尔浓度为1摩/升
B.溶液中[H+]=![]() 摩/升
摩/升
C.溶液中水分子数和H+数之比为1:1
D.溶液的摩尔浓度稍小于![]() 摩尔/升
摩尔/升
7.某含氧强酸HmXOn,分子量为A,将它溶于水,测得溶液的氢离子摩尔浓度为2摩尔/升,溶液的质量百分比浓度为20% ,密度为1.5克/厘米3,则m值为-----------------------------------------------------------------------------------(B)
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
8.质量分数为15%的硫酸溶液18毫升,密度为1.102克/毫升,则它的物质的量的浓度最接近下列数值中的-------------------------------------------------〖A〗
A.1.685摩/升 B.3.370摩/升 C.22.49摩/升 D.11.24摩/升
〖提示〗:由于题中给出的各选项之间的数值相差都比较大,所以可以进行近似处理:1.102®1,98®100,代入公式C=![]() ,与A选 项较接近。
,与A选 项较接近。
9.MgCl2溶液与Na2SO4溶液混和后,[Mg2+]=[SO42-],则下列说法不正确的是----------------------------------------------------------------------------------------------- (C)
A.混和液中[Cl-]=[Na+] B.混和液中[Cl-]=2[ SO42-]
C.混和前两溶液体积相等
D.混和前两溶液中MgCl2与Na2SO4物质的量相等
10.将等体积的HnRO3和Hn+1RO4两种酸溶液与定量的NaOH中和都生成正盐,则这两种酸的摩尔浓度比是----------------------------------------------------(D)
A.n:(n+1) B.1:1 C.1:(n+1) D.(n+1):n
填空题
1.
A气体极易溶于水,其分子量为a,在0℃、1.01×105帕时,测得其饱和溶液的物质的量浓度为b摩/升,该溶液的密度为c克/厘米3,求:
(1)A饱和溶液的质量百分比浓度【答:![]() 】
】
(2)0℃、1.01×105帕时,1体积水中可溶解多少体积的A气体?
【答:V=![]() 】
】
2.
计算题
1. 向某氯化钡溶液中,逐滴滴入密度为1.28克/ 厘米3的硫酸溶液,恰好完全反应时,过滤,测得滤液的质量恰好与原氯化钡溶液的质量相等。求硫酸溶液的物质的量的浓度。
〖提示〗:硫酸的质量分数=![]() ×100%=42.06%
×100%=42.06%
硫酸的物质的量的浓度=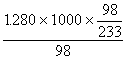 =5.49摩/升
=5.49摩/升
2.