高三年级理科综合上学期期末质量检测
理科综合试题
本试卷分第Ⅰ卷和第Ⅱ卷两部分,满分300分,考试时间150分钟。
注意事项:
1.选择题选出答案后,用2B铅笔涂黑机读卡上对应题目的答案标号。如需改动、用橡皮擦干净后,再选涂其它答案。
3.交卷时只交试卷和机读卡,不交试题,答案写在试题上的无效。
4.可能用到的相对原子质量:H1 N 14 C 12 O 16 Si 28 Fe 56
第 Ⅰ 卷(选择题,共126分)
一、单项选择题:每小题四个选项中只有一个选项正确,每小题6分,共78分。
1.向日葵和番茄都能产生果实和种子,向日葵的果实就是平时我们吃的“瓜子”。在上述两种植物开花期间,遇到了连续的阴雨天,影响了植物的授粉。管理人员及时喷洒了一定浓度的生长素。下列叙述正确的是
A.两种植物都能形成无子果实,产量均未受影响
B.番茄形成无子果实,产量未受影响;向日葵形成无子果实,产量下降
C.两种植物都能形成无子果实,产量下降
D.番茄形成有籽果实,产量上升;向日葵不能形成无子果实
2.甲、乙、丙是3种微生物,下表中Ⅰ、Ⅱ、Ⅲ是培养微生物的三种培养基(+表示含有,-表示不含有)。甲、乙、丙都能在Ⅲ中正常生长繁殖;甲能在Ⅰ中正常生长繁殖,而乙和丙都不能;乙能在Ⅱ中正常生长繁殖,甲、丙都不能。根据表中信息可判断下列说法错误的是
| 粉状硫 10g | K2HPO4 4g | FeSO4 0.5g | 蔗糖 10g | (NH4)2SO4 0.4g | H2O 100mL | MgSO4 9.25g | CaCl2 0.5g | |
| Ⅰ | + | + | + | + | - | + | + | + |
| Ⅱ | + | + | + | - | + | + | + | + |
| Ⅲ | + | + | + | + | + | + | + | + |
A.甲能够在无氮培养基上生长繁殖,很可能是根瘤菌
B.乙能够在无有机碳源的培养基中生长繁殖,是自养微生物
C.丙需要培养基提供有机碳源,肯定是异养微生物
D.3种微生物在正常生长繁殖中可能不需要另外添加生长因子
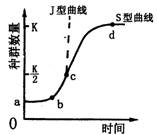 3.右图表示种群数量的动态变化过程,下列有关图中各点的叙述正确的是
3.右图表示种群数量的动态变化过程,下列有关图中各点的叙述正确的是
A.a点时种群由理想环境进入有限的生活环境
B.b点时进行捕捞最有利于该种群的持续生存
C.c点时种群增长速率最快,种群密度达到最大
D.d点时微生物群体的初级代谢产物总量最多
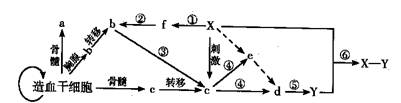
4.下图表示人体内某些淋巴细胞的分化和某种免疫过程,数字表示过程,字母表示细胞或物质。下列叙述错误的是
|
A.由造血干细胞形成的a、b、c细胞内蛋白质的种类有所不同
B.①②③过程都需要细胞膜上糖被的参与
C.④⑤过程属于体液免疫的反应阶段,⑥过程属于效应阶段
D.Y主要在内环境中发挥作用,与Y合成和分泌有关的膜性细胞器有内质网、高尔基体和线粒体
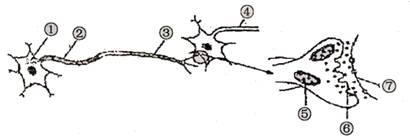
5.乙酰胆碱(Ach)是一种神经递质。实验人员欲研究Ach浓度与反应时间的关系(简图如下),在除去突触小泡的前提下自①处注入不同浓度的Ach,②处给予恒定刺激,③、④处分别为灵敏感应时间测量点。测得不同浓度Ach条件下③、④两处感受到信号所用时间如下表所示。下列各项叙述正确的是
|
| Ach浓度(mmol/-L) | ③处感受信号的时间(ms) | ④处感受信号的时间(ms) |
| 0.1 | 5.00 | 5.56 |
| 0.2 | 5.00 | 5.48 |
| 0.3 | 5.00 | 5.31 |
| 0.4 | 5.00 | 5.24 |
A.图中⑤、⑥与⑦共同构成一个突触
B.实验中除去突触小泡的目的是防止实验结果受到相关因素的干扰
C.表中数据说明高浓度Ach能促进兴奋在神经纤维上的传导
D.表中数据说明Ach浓度的增加对兴奋在神经元之间的传递无明显影响
6.下列叙述从化学角度分析,其中错误的是
A.被蜜蜂蛰咬后,可涂抹稀氨水或小苏打溶液减轻疼痛
B.HgCl2的稀溶液可用于手术器械消毒,原因是可使蛋白质变性
C.燃料煤脱硫后使用,可减少对大气的污染
D.氟利昂(CCl2F2)或NOx都可破坏臭氧层,而导致“温室效应”
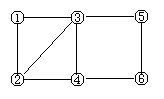 7.如图所示有6个编号,每个编号代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应。供填写的物质有:a.Na2CO3溶液 b.MgSO4溶液 c.BaCl2溶液 d.稀H2SO4e.铁f.Cu(NO3)2溶液。则图中③表示的物质的编号是
7.如图所示有6个编号,每个编号代表下列物质中的一种物质,凡是用直线相连的两种物质均能发生化学反应。供填写的物质有:a.Na2CO3溶液 b.MgSO4溶液 c.BaCl2溶液 d.稀H2SO4e.铁f.Cu(NO3)2溶液。则图中③表示的物质的编号是
A.e B.f C.a D.d
8.原电池的电极名称和电极反应不仅与电极材料有关,也与电解质溶液有关。下列说法中不正确的是
A.由Mg、Al、NaOH溶液组成电池,其负极反应式为:Al-3e—+4OH—=AlO2-+2H2O
B.由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu-2e—=Cu2+
C.由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al-3e—=Al3+
D.由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu-2e—=Cu2+
9.短周期元素W、X、Y、Z 的原子序数依次增大,W与Y、X与Z 位于同一主族。W 与X 可形成共价化合物WX2。Y原子的内层电子总数是其最外层电子数的2.5 倍。下列叙述中不正确的是
A.WX2分子中所有原子最外层都为8 电子结构
B.WX2、ZX2的化学键类型和晶体类型都相同
C.原子半径大小顺序为X <W<Y<Z
D.WX2是以极性键结合成的非极性分子
10.设NA代表阿佛加德罗常数的值,下列说法错误的是
A.7gCnH2n中含有的氢原子数目为NA
B.1mol HNO3见光分解,转移电子数NA
C.46g NO2和 N2O4混合物含有的原子数为3NA
D.常温下,60g SiO2中含有NA个Si-O键
11.可逆反应A(g)+3B(g) ![]() 2C(g);△H<0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
2C(g);△H<0。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1 molA和3 molB,在一定条件到下达平衡时放出热量为Q1 kJ;在相同的条件下,向乙容器中加入2 molC达到平衡后吸收热量为Q2kJ,已知Q1=3Q2。下列叙述不正确的是
A.甲中A的转化率为75%
B.甲、乙中C的体积分数相同
C.达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向生成C的方向移动
D.乙中的热化学反应方程式为2C(g)
![]() A(g)+3B(g);△H=+3Q2
kJ·mol—1
A(g)+3B(g);△H=+3Q2
kJ·mol—1
12.经测定某溶液中离子只有Na+、CH3COO—、H+、OH—四种,且离子浓度大小的排列顺序为:c(CH3COO—)>c(Na+)>c(H+)>c(OH—),其可能的情况是
A.该溶液可能由0.1mol/L的CH3COOH溶液与0.1mol/L的NaOH溶液等体积混合而成
B.该溶液可以由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合而成
C.该溶液中离子浓度的关系符合c(CH3COO—)+c(OH—)>c(Na+)+c(H+)
D.在上述溶液中加入适量NaOH,离子浓度大小可改变为
|
13.新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化。某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:
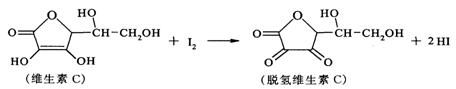
下列说法正确的是
A.维生素C的分子式为C6H8O6
B.维生素C在酸性条件下水解只得到2种产物
C.维生素C不可溶于水,可溶于有机溶剂
D.上述反应为取代反应
二、不定项选择题。共8个小题,每小题6分,共48分。每题至少有一个选项是正确的。完全选对得6分,选对但不全的得3分,不选或有选错的得零分。
14.在下列四个方程中,X1、X2、X3和X4各代表某种粒子
![]()
![]()
![]()
![]() 以下判断中正确的是ACD
以下判断中正确的是ACD
A.X1是中子 B.X2是质子 C.X3是![]() 粒子 D.X4是电子
粒子 D.X4是电子
15.日光灯中有一个启动器,其中的玻璃泡中装有氖气。启动时,玻璃泡中的氖气会发出红光,这是由于氖原子的A
A.外层电子受激而产生的 B.自由电子的周期性运动而产生的
C.内层电子受激而产生的 D.原子核受激而产生的
16.对于一定质量的理想气体,下列说法正确的是AD
A.体积不变,压强减小的过程,气体一定放出热量,内能减少
B.若气体内能增加,则外界一定对气体做功
C.若气体的温度升高,则每个气体分子的速度一定增大
D.若气体压强不变,气体分子平均距离增大,则气体分子的平均动能一定增大
17.关于单摆下列说法正确的是C
A.摆球运动的回复力是摆线张力和重力的合力
B.摆球经过轨迹上的同一点速度是相同的
C.摆球经过轨迹上的同一点加速度是相同的
D.摆球经过平衡位置受力是平衡的
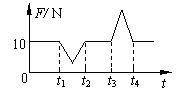 18.某实验小组利用力的传感器和数字化系统,观察超重和失重现象。他们在学校电梯房内做实验,在电梯天花板上固定一个力传感器,传感器的测量挂钩向下,并在挂钩上悬挂一个重为10N的钩码,在电梯运动过程中,计算机显示屏上显示出如图所示图线,根据图线分析可知下列说法中正确的是ABC
18.某实验小组利用力的传感器和数字化系统,观察超重和失重现象。他们在学校电梯房内做实验,在电梯天花板上固定一个力传感器,传感器的测量挂钩向下,并在挂钩上悬挂一个重为10N的钩码,在电梯运动过程中,计算机显示屏上显示出如图所示图线,根据图线分析可知下列说法中正确的是ABC
A.该图线显示了力传感器对钩码的拉力大小随时间的变化情况
B.从时刻t1到t2,钩码处于失重状态,从时刻t3到t4,钩码处于超重状态
C.电梯可能开始在15楼,先加速向下,接着匀速向下,再减速向下,最后停在1 楼
D.电梯可能开始在1楼,先加速向上,后匀速向上,再减速向上,最后停在15楼
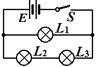 19.在如图甲所示的电路中,电源电动势为3.0V,内阻不计,L1、L2、L3为3个相同规格的小灯泡,这种小灯泡的伏安特性曲线如图乙所示。当开关闭合后,下列关于电路中的灯泡的判断中,正确的是ACD
19.在如图甲所示的电路中,电源电动势为3.0V,内阻不计,L1、L2、L3为3个相同规格的小灯泡,这种小灯泡的伏安特性曲线如图乙所示。当开关闭合后,下列关于电路中的灯泡的判断中,正确的是ACD
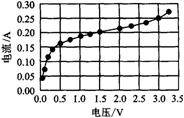 A.灯泡L1的电阻为12Ω
A.灯泡L1的电阻为12Ω
B.通过灯泡L1的电流为灯泡L2的电流的2倍
C.灯泡L1消耗的电功率为0.75W
D.灯泡L2消耗的电功率为0.30W
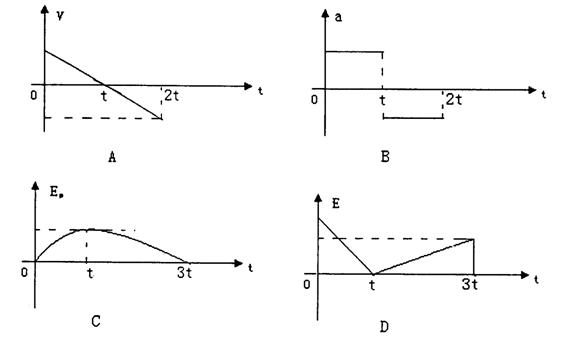 20.质量为m的滑块以初速度v0自固定于地面的斜面底端开始冲上斜面,到达某一高度后又返回斜面底端,斜面与滑块之间有摩擦。下面四图分别表示它在斜面上运动的速度V、加速度a、势能EP和机械能E随时间的变化图线,可能正确的是C
20.质量为m的滑块以初速度v0自固定于地面的斜面底端开始冲上斜面,到达某一高度后又返回斜面底端,斜面与滑块之间有摩擦。下面四图分别表示它在斜面上运动的速度V、加速度a、势能EP和机械能E随时间的变化图线,可能正确的是C
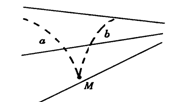 21.如图所示,实线为不知方向的三条电场线,从电场中M点以相同速度飞出a、b两个带电粒子,运动轨迹如图中虚线所示。则C
21.如图所示,实线为不知方向的三条电场线,从电场中M点以相同速度飞出a、b两个带电粒子,运动轨迹如图中虚线所示。则C
A.a一定带正电,b一定带负电
B.a的速度将减少,b的速度将增加
C.a的加速度将减小,b的加速度将增加
D.两个粒子的电势能一个增加一个减小
第 Ⅱ 卷(非选择题,共174分)
22.(16分)
(1)(8分)有一测量微小时间差的装置,是由两个摆长略有微小差别的单摆同轴水平悬挂构成,两个单摆摆动平面前后相互平行。
①现测得两单摆完成50次全振动的时间分别为50.0s和49.0s,则两单摆周期差Δt=__________s。
②具体操作如下:把两摆球向右拉至相同的摆角处,先释放长摆摆球,接着再释放短摆摆球,测得短摆经过若干次全振动后,两摆恰好第一次同时同向通过某位置,由此可得出释放两摆的微小时间差。若测得释放两摆的时间差价Δt=0.165s,则在短摆释放_______s填时间)后,两摆恰好第一次同时向_________(填方向)通过____________(填位置)。①0.02s②8.805s;左;平衡位置。
(2)(8分)在测定一节干电池的电动势和内电阻的实验中,备有下列器材:
A.待测的干电池(电动势约为1.5 V,内电阻小于1.0Ω)
B.电流表G(满偏电流3 mA,内阻Rg=10Ω)
C.电流表A(0~0.6 A,内阻0.1Ω)
D.滑动变阻器R1(0~20Ω,10 A)
E.滑动变阻器R2(0~200Ω,l A)
F.定值电阻R0 (990Ω)
G.开关和导线若干
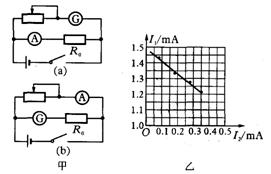 ①某同学发现上述器材中虽然没有电压表,但给出了两个电流表,于是他设计了如图甲的(a)、(b)两个参考实验电路,其中合理的是
图所示的电路;在该电路中,为了操作方便且能准确地进行测量,滑动变阻器应选
(填写器材前的字母代号)。
①某同学发现上述器材中虽然没有电压表,但给出了两个电流表,于是他设计了如图甲的(a)、(b)两个参考实验电路,其中合理的是
图所示的电路;在该电路中,为了操作方便且能准确地进行测量,滑动变阻器应选
(填写器材前的字母代号)。
②图乙为该同学根据①中选出的合理的实验电路利用测出的数据绘出的I1—I2图线(I1为电流表G的示数,I2为电流表A的示数),则由图线可以得被测电池的电动势E= V,内阻r= Ω。
答案:①b;D或R②(1.48士0.02);0.77(0.75~0.80)
23.(15分)人类受小鸟在空中飞翔的启发而发明了飞机,小鸟在空中滑翔时获得的举力可表示为F=KSv2,式中S为翅膀的面积,v为小鸟的速度,K为比例系统,一小鸟质量为120g,翅膀面积为S1,其水平匀速滑翔的最小速度为12m/s,假定飞机飞行时获得向上的举和与小鸟飞行时获得的举力有同样的规律,现有一架质量为3200kg的飞机,它在跑道上加速时获得最大加速度为5m/s2。若飞机机翼面积为小鸟翅膀面积的600倍,则此飞机起飞的跑道至少要多长。
解:(15分)小鸟飞行时获得向上举力与重力平衡,即KS·![]() =m1g 5分
=m1g 5分
同理飞机:K×600S1![]() =m2g
得
=m2g
得![]() =80m/s 5分
=80m/s 5分
根据运动学公式![]() =2as
=2as ![]() 5分
5分
 24.(19分)“神州六号”飞船的成功飞行为我国在2010年实现探月计划——“嫦娥工程”获得了宝贵的经验。假设月球半径为R,月球表面的重力加速度为
24.(19分)“神州六号”飞船的成功飞行为我国在2010年实现探月计划——“嫦娥工程”获得了宝贵的经验。假设月球半径为R,月球表面的重力加速度为![]() ,飞船在距月球表面高度为3R的圆形轨道Ⅰ运动,到达轨道的A点点火变轨进入椭圆轨道Ⅱ,到达轨道的近月点B再次点火进入月球近月轨道Ⅲ绕月球作圆周运动。求:
,飞船在距月球表面高度为3R的圆形轨道Ⅰ运动,到达轨道的A点点火变轨进入椭圆轨道Ⅱ,到达轨道的近月点B再次点火进入月球近月轨道Ⅲ绕月球作圆周运动。求:
⑴飞船在轨道Ⅰ上的运行速率;
⑵飞船在A点处点火时,动能如何变化;
⑶飞船在轨道Ⅲ绕月球运行一周所需的时间。
解:(19分)⑴设月球的质量为M,飞船的质量为m,则
![]() (3分)
(3分)
![]() (3分) 解得
(3分) 解得 ![]() (3分)
(3分)
⑵动能减小 (4分)
⑶设飞船在轨道Ⅲ绕月球运行一周所需的时间为T,则
![]() (3分)
(3分)
∴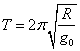 (3分)
(3分)
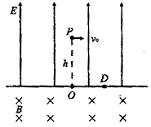 25.(22分)一宇宙人在太空(万有引力可以忽略不计)玩垒球,辽阔的太空球场半侧为匀强电场,另半侧为匀强磁场,电场和磁场的分界面为垂直纸面的平面,电场方向与界面垂直,磁场方向垂直纸面向里,电场强度大小为E=100V/m,宇宙人位于电场一侧距界面为h=3m的P点,O为P点至界面垂线的垂足,D点位于纸面上O点的右侧,OD与磁场的方向垂直,垒球的质量m=0.1kg,电量q=-0.05C,宇宙人从P点以初速度v0=10m/s平行于界面投出垒球,要使垒球第一次通过界面时就击中D点,且能回到出发点P,求:
25.(22分)一宇宙人在太空(万有引力可以忽略不计)玩垒球,辽阔的太空球场半侧为匀强电场,另半侧为匀强磁场,电场和磁场的分界面为垂直纸面的平面,电场方向与界面垂直,磁场方向垂直纸面向里,电场强度大小为E=100V/m,宇宙人位于电场一侧距界面为h=3m的P点,O为P点至界面垂线的垂足,D点位于纸面上O点的右侧,OD与磁场的方向垂直,垒球的质量m=0.1kg,电量q=-0.05C,宇宙人从P点以初速度v0=10m/s平行于界面投出垒球,要使垒球第一次通过界面时就击中D点,且能回到出发点P,求:
(1)O、D两点之间的距离d;
(2)垒球从抛出到第一次回到P点的时间t。
解:(22分)(1)设垒球在电场中运动的加速度大小为a,时间t1,OD=d,有
![]() 3分
3分
得![]()
![]() 3分
3分
(2)垒球运动轨道![]()
![]() 3分
3分
垒球进入磁场时速度大小为![]() 3分
3分
设垒球做匀速圆周运动半径R,磁感应强度大小B,![]() 3分
3分
由洛仑兹力提供向心力,![]() 3分
3分
垒球在磁场中运动时间,![]() 2分
2分
总时间![]() 2分
2分
26.(本题包括两个小题,共16分)
I.(每空2分,共8分)根据下列题目要求,回答下列问题:
(1)硫酸是强酸,中学阶段将硫酸在水溶液中看作完全电离。事实上,硫酸的第一步电离是完全的:H2SO4= H++ HSO4-,第二步电离并不完全:HSO4-![]() H++SO42-
H++SO42-
①则Na2SO4溶液呈__________(填弱酸性、中性或弱碱性),其理由是(用离子方程式表示)______________________________________________。
②写出硫酸与氯化钡溶液反应的离子方程式:_________________________。
(2)在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量稀硫酸,溶液立即变蓝,有关反应的离子方程式是:____________________________________;
II.(每空2分,共8分)有A、B、C、D、E五种短周期元素,它们的原子序数依次递增。已知:A和C ,B和D最外层电子数相同,且B、D的质子数之和是A、C质子数之和的2倍;E在同周期元素中原子半径最小。请回答:
(1)由A、B、C三种元素形成化合物所属的晶体类型为
(2)由C、D两种元素形成化合物的水溶液呈碱性,其原因是 。(用离子方程式及必要的文字加以说明)
(3)由A、B、C、D四种元素形成的两种化合物X和Y,其中X的溶液呈强酸性,其原因是 。
(4)由C、D两元素的最高价氧化物对应的水化物在溶液中反应生成2molH2O时,放出114.6kJ热量,写出该离子反应的热化学方程式 。
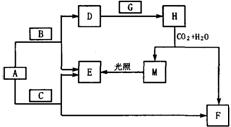 27.(每空2分,共10分)现有A、B、C、D、E、F、G、H、M九种物质,其中A、B、C均为氧化物, G、E为气体单质,F的水溶液与石灰水混合可制得D的溶液。它们之间相互转化关系如右图,其他与题无关的生成物均已略去。请回答下列问题:
27.(每空2分,共10分)现有A、B、C、D、E、F、G、H、M九种物质,其中A、B、C均为氧化物, G、E为气体单质,F的水溶液与石灰水混合可制得D的溶液。它们之间相互转化关系如右图,其他与题无关的生成物均已略去。请回答下列问题:
(1)写出化学式:H ,C 。
(2)写出下列反应的化学方程式:
A+C→F+E 。
F→D 。
(3)写出离子反应方程式:
D+G→H 。
28.(本题包括两个小题,共22分)
I.(每空2分,共8分)甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。
(1)甲组:沉淀分析法
把一定量的混合物溶解后加入过量CaCl2,然后将所得沉淀过滤、洗涤、烘干、称量。确定CaCl2溶液过量的方法是___________________________________________,判断沉淀洗净的操作是_________________________________________________。
(2)乙组:气体分析法
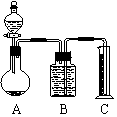 把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_________________,选用该溶液后实验结果还是不准确,主要原因是_____________________________________。
把一定量的混合物与足量盐酸反应后,用如图装置测定产生的CO2气体的体积,为减小CO2的溶解,B中溶液应是_________________,选用该溶液后实验结果还是不准确,主要原因是_____________________________________。
| A | B | C | D | E | F | G | |
| A | - | - | - | - | - | - | ↓ |
| B | - | - | - | - | ↓ | ↓ | ↓ |
| C | - | - | ― | ↓ | - | ↓ | ↓ |
| D | - | - | ↓ | - | ↓ | ↓ | ↓ |
| E | - | ↓ | - | ↓ | - | ↓ | - |
| F | - | ↓ | ↓ | ↓ | ↓ | - | ↓ |
| G | ↓ | ↓ | ↓ | ↓ | - | ↓ | - |
II.(每空2分,共14分)有A、B、C、D、E、F、G7瓶不同物质的溶液,它们各是Na2CO3、Na2SO4、KCl、AgNO3、MgCl2、Ca(NO3)2和Ba (OH)2溶液中的一种。为了鉴别,各取少量溶液进行两两混合,实验结果如表所示。表中“↓”表示生成沉淀或微溶化合物,“-”表示观察不到明显变化。写出这七种物质的化学式:
A: ,B: ,C: ,D: ,E: ,F: ;G 。
29.(每空2分,共12分)有机物A是芳香族化合物,其分子式为CxHyOz,它的苯环上的一元取代物只有2种,有关A的一系列转化关系如下图所示:
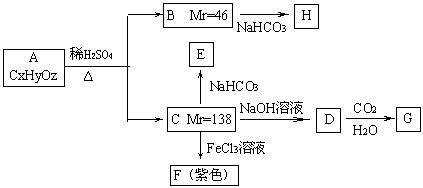
(1)C中所含的官能团有 。
(2)A的结构简式: 。
(3)书写化学反应方程式:
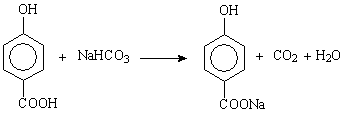
C → E: 。
D →G: 。
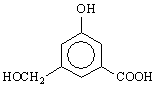
(4)化合物M也是一种芳香族化合物,其分子式中比A多2个氢原子,为CxHy+2Oz,它的苯环上有3个互为间位的取代基。等量的M分别和Na、NaOH、NaHCO3完全反应,消耗的Na、NaOH、NaHCO3物质的量之比为3:2:1,则:
M的结构简式为 。
两个M分子间脱水成环状酯的结构简式为________________________。
30.(一)(共10分)下图是人体内糖代谢过程的示意图,请据图回答:
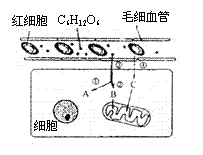 (1)图中B所示的物质是
,C所示
(1)图中B所示的物质是
,C所示
的物质是 。
(2)如果图示的细胞是肝细胞,则图中A所示的物质
最可能是 。如果图示的细胞是肌细胞,
则图中A所示的物质最可能是 。
(3)如果图示的细胞是神经细胞,那么,在显微镜下能
观察到染色体吗? ,为什么 。
(4)图示中的④过程,会使细胞中ADP的含量上升吗? ,请叙述理由 。
(5)如果人体内甲状腺激素浓度过高,则图中②过程将加快,这是因为
。
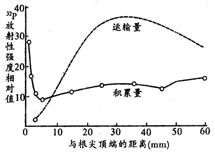 (二)(共8分)科学家用大麦幼苗进行实验,探究根尖吸收矿质元素最活跃的区域,测量结果如下图:
(二)(共8分)科学家用大麦幼苗进行实验,探究根尖吸收矿质元素最活跃的区域,测量结果如下图:
(1)实验分析:
①科学家用________________培养大麦幼苗,获得上述数据。
②数据表明,距根尖1~2mm比30~40 mm区域吸收32P的量___________。
③根尖某区域吸收32P的量等于____________。
(2)该实验原理是:_____________________________________________________。
(3)放射性同位素标记法一般不应用于
A.基因诊断 B.修复有缺陷的基因
C.分泌蛋白分泌过程的研究 D.探究C3、C4植物固定CO2的途径
31.(24分)某高中生物老师准备用玉米(2N=20)作实验材料,让同学们进行自主学习和探究,来验证生物学的基本知识及基本原理,同时提高同学们的生物实验技能。为了提高同学们的探索积极性,老师将全班同学等分成两组,每组分配等量的玉米种子若干,其中有非甜玉米和甜玉米,均为纯种,分开包装(种子数量满足实验需求)。实验场地为生物实验室和学校生物实验基地。实验设备、仪器、药品等为生物实验室现有(满足高中生物实验要求)。要求从种子萌发时开始,在玉米的自然生长周期内进行实验,实验可在玉米的两个生长周期内完成。回答下列问题。
(1)如果你是其中的一员,你准备在种子萌发时,不伤害根的情况下可进行哪两个实验? 、 (答案合理给分)。
(2)待根长出1~2cm时,可用根尖来做 。观察发现玉米体细胞含20条染色体,有 个染色体组。
(3)在植株的幼苗期,两组同学都用溶液培养法验证了一种 对植物生长的影响。甲组发现其实验组的幼叶最先受损,乙组发现其实验组的老叶最先受损,为了不影响植物的正常生长,甲组立即向溶液中补充了 ,症状很快得到纠正,未影响到植物的正常生长发育。
A.Mg (NO3)2 B. Na2SiO3 C. Ca(NO3)2 D. KH2PO4
(4)接着甲组用玉米叶制成叶脉横切临时装片,观察了叶脉的结构。发现维管束鞘细胞结构特点是: 。
(5)为了验证基因的分离定律,甲、乙两组同学都将非甜玉米和甜玉米种植,采用下图中某个操作程序,然后按孟德尔的实验过程进行实验,验证F2的分离比。甲组同学的实验结果是:F1全为非甜玉米,F2有非甜和甜两种玉米,甜玉米约占1/8。乙组同学的实验结果是:F1全为非甜玉米,F2有非甜和甜两种玉米,甜玉米约占1/4。
①用简图表示两组同学的实验过程:(用该题材料表示)
②请预测该实验中F2的预期值。 。
③在下图中选出甲、乙两组在用亲本杂交时的授粉过程。甲组: ,乙组 。
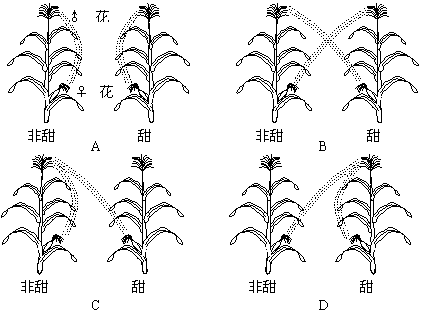 |
④如果按甲组的杂交方法不改进,后续实验要如何进行才能得到正确的性状分离比? 如果对甲组的实验进行改进,将如何改进: 。
(6)同学们还准备用玉米来作一些细胞工程和基因工程方面的实验,但受中学实验条件的限制而未做。用玉米可做的这方面的实验有(答两种): 、 。
高三理综物理部分期末考试答案
14.ACD 15.A 16.AD 17.C 18.ABC 19.ACD 20.C 21.C
22.(1)(8分)①0.02s②8.805s;左;平衡位置。
(2)(8分)①b;D或R②(1.48士0.02);0.77(0.75~0.80)
23.解:(15分)小鸟飞行时获得向上举力与重力平衡,即KS·![]() =m1g 5分
=m1g 5分
同理飞机:K×600S1![]() =m2g
得
=m2g
得![]() =80m/s 5分
=80m/s 5分
根据运动学公式![]() =2as
=2as ![]() 5分
5分
24.解:(19分)⑴设月球的质量为M,飞船的质量为m,则
![]() (3分)
(3分) ![]() (3分)
(3分)
解得 ![]() (3分)
(3分)
⑵动能减小 (4分)
⑶设飞船在轨道Ⅲ绕月球运行一周所需的时间为T,则
![]() (3分) ∴
(3分) ∴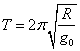 (3分)
(3分)
25.解:(22分)(1)设垒球在电场中运动的加速度大小为a,时间t1,OD=d,有
![]() 3分
3分
得![]()
![]() 3分
3分
(2)垒球运动轨道![]()
![]() 3分
3分
垒球进入磁场时速度大小为![]() 3分
3分
设垒球做匀速圆周运动半径R,磁感应强度大小B,![]() 3分
3分
由洛仑兹力提供向心力,![]() 3分
3分
垒球在磁场中运动时间,![]() 2分
2分
总时间![]() 2分
2分
化学答案
一、选择题
6.D 7.C 8.B 9.C 10.D 11.D 12.B 13.A
二、非选择题
26.(本题包括两个小题,共16分)
I.(每空2分,共8分)
(1) HSO4-![]() H++ SO42- 。
H++ SO42- 。
①.弱碱性,SO42-+H2O![]() OH-+HSO4- ②. Ba2+ +HSO4-= H++ BaSO4↓。
OH-+HSO4- ②. Ba2+ +HSO4-= H++ BaSO4↓。
(2)2H++2I-+ClO- = Cl-+H2O+ I2
II.(每空2分,共8分)
(1)离子晶体
(2)因为溶液中存在S2—+H2O![]() HS—+OH—,使得C(OH—)>c(H+),所以溶液呈碱性
HS—+OH—,使得C(OH—)>c(H+),所以溶液呈碱性
(3)NaHSO4 =Na+ + H+ + SO42-,因为c(H+)>C(OH—) ,所以溶液呈酸性。
(4)H+(aq)+OH—(aq)=H2O(1);△H=-53.7kJ/mol
27.(每空2分,10分)
(1)NaClO
CO2
(2)2Na2O2+2CO2=2Na2CO3+O2↑ Na2CO3+Ca(OH)2=2NaOH+CaCO3↓
(3)2OH-+Cl2=Cl-+ClO-+H2O
28.本题包括2小题,每空2分,共22分
I.(每空2分,共8分)
(1)静置,向上层清液中继续滴加CaCl2溶液,若无沉淀说明CaCl2已过量;沿玻棒向过滤器中的沉淀上加蒸馏水至淹没沉淀,静置使其全部滤出,重复2~3次,然后向滤液(洗涤液)中滴加AgNO3溶液无沉淀,则洗净。
(2)饱和NaHCO3溶液;从A出来的气体中混有HCl,会与NaHCO3反应生成CO2
II.(每空2分,共14分)
A:KCl B:Na2SO4 C:MgCl2 D:Na2CO3 E:Ca(NO3)2 F:Ba(OH)2 G:AgNO3
29.(每空2分,共12分)
(1)羟基(写结构简式也对)
(2) ![]()
(3)
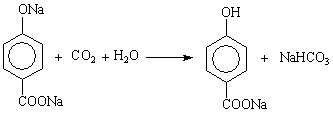
(4)
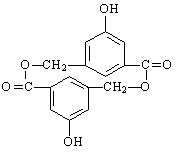
高三理综生物部分期末考试答案
1----5 BADCB
30.(共18分)
(一)(共10分)
(1)丙酮酸 氧气(或O2)(2分)
(2)肝糖元 肌糖元(2分)
(3)不能 因为神经细胞是高度分化的细胞,不具备细胞分裂能力,故不具备细胞周期。(2分)
(4)不会 O2的跨膜运动是自由扩散的过程,不需要消耗ATP。(2分)
(5)甲状腺激素促进新陈代谢,如果甲状腺激素过多,则体内物质氧化分解速度加快。(2分)
(二)(共8分)
(1)含32P的完全培养液(1分) 少 (1分) 运输量加积累量(1分)
(2)放射性同位素可用于追踪物质运行的过程,通过测定根尖不同区域矿质元素吸收量(运输量加积累量)的多少可以确定吸收最活跃区域(4分)
(3)B(1分)
31.(共24分)
(1)种子的吸胀吸水实验;根的渗透吸水实验;根的向性实验(向地性)(2分)
(2)观察植物细胞的有丝分裂实验 2 (2分)
(3)必需矿质元素 C (2分)
(4)维管束鞘细胞比较大,且含有许多大而没有基粒的叶绿体(2分)
(5)
![]() ① P 非甜玉米 × 甜玉米(4分)
① P 非甜玉米 × 甜玉米(4分)
F1
F2
②非甜玉米∶甜玉米 = 3∶1(2分)
③ C B(4分)
④只将甜玉米植株上所结种子种下自交,统计其后代分离比 (2分)
用牛皮纸袋将玉米的雌花序和雄花序分别套住并固定,防止自然授粉过程(2分)
(6)单倍体育种;植物体细胞杂交;转基因玉米培育(2分)
![]()
 高三年级上学期期末质量检测
高三年级上学期期末质量检测
理科综合试题
| 科目 | 物理 | 化学 | 生物 | 总 成绩 | |||||||
| 题号 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | |
| 得分 | |||||||||||
| 总分 | |||||||||||
22.(1) ①__________ ②_________,________,___________
(2)①__________;_________ ②___________,_________
23.解:
24.解:
25.解:
26.(本题包括两个小题,共16分)
I.(每空2分,共8分)
(1)①Na2SO4溶液呈________,
理由是(用离子方程式表示)______________________________________________。
②硫酸与氯化钡溶液反应的离子方程式:_________________________。
(2)离子方程式是:____________________________________;
II.(每空2分,共8分)
(1)晶体类型为 。
(2)原因是 。
(3)原因是 。
(4)离子反应的热化学方程式 。
27.(每空2分,共10分)
(1)写出化学式:H ,C 。
(2)写出下列反应的化学方程式:
A+C→F+E 。
F→D 。
(3)离子反应方程式:
D+G→H 。
28.(本题包括两个小题,共22分)
I.(每空2分,共8分)
(1)确定CaCl2溶液过量的方法是_________________________________
________________,判断沉淀洗净的操作是_________________________________
_______________________________________________________________________。
(2)B中溶液应是_____________________________________________,主要原因是_____________________________________。
II.(每空2分,共14分)
A: ,B: ,C: ,D: ,E: ,F: ;G 。
29.(每空2分,共12分)
(1)C中所含的官能团有 。
(2)A的结构简式: 。
(3)书写化学反应方程式:
C → E: 。
D →G: 。
(4)
M的结构简式为 。
两个M分子间脱水成环状酯的结构简式为________________________。
30.(共18分)
(一)(共10分)
(1) , 。
(2) 。
(3) , 。
(4) ,
。
(5) 。
(二)(共8分)
(1)__________ 、 、
(2)___________ 。
(3)________________
31.(共24分)
(1) 、 (答案合理给分)。
(2) 、 。
(3) 、 。
(4) 。
(5)①用简图表示两组同学的实验过程:(用该题材料表示)
② 。③甲组: ,乙组 。
④ 、 。
(6) 、 。