08年高考理综生物诊断考试能力测试
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。满分300分,考试时间150分钟。
第Ⅰ卷
注意事项:
1.选择题每小题选出答案后请填写在第Ⅱ卷上方表格对应题号的空格中。
2.本卷共21题,每小题6分,共126分。
以下数据可供解题时参考:
相对原子质量(原子量):H 1 N 14 O16
一、选择题(本题包括13小题。每小题只有一个选项符合题意)
1.有关减数分裂的叙述,正确的是 ( )
A.从精原细胞到初级精母细胞的过程中DNA复制、基因加倍、染色体加倍
B.精原细胞的增殖是有丝分裂,精原细胞通过两次减数分裂产生了精子
C.减数第一次分裂,同源染色体分离,同时非同源染色体自由组合
D.减数第一次分裂同源染色体分离,减数第二次分裂非同源染色体自由组合
2.下面是四位同学的实验操作方法或结果,其中错误的一项是 ( )
A.剪去胚芽鞘尖端的燕麦胚芽在单侧光下向光侧弯曲生长
B.用纸层析法分离叶绿体中的色素,扩散最快的一条色素带呈橙黄色
C.蛋白质与双缩脲试剂作用产生紫色反应
D.显微镜下观察根尖的有丝分裂,在细胞呈正方形的区域易找到分裂期的细胞
3.当人体处与寒冷环境中,为抵御严寒,体内激素的分泌会发生变化,其中分泌量增加的( )
①促甲状腺激素 ②胰岛素 ③生长激素 ④肾上腺素 ⑤甲状腺激素
A.①②③ B.①③⑤ C.②④⑤ D.①④⑤
4.向日葵种子粒大(B)对粒小(b)为显性,含油少(S)对含油多(s)为显性,某人用
粒大油少和粒大油多的向日葵植株进行杂交,结果如图所示。下列叙述正确的是( )

A.亲本的基因型是BbSs和BbSs
B.杂交后代的基因型比是1︰1︰2︰2︰1︰1
C.杂交后代的表现型比是3︰1︰1︰1
D.杂交后代的基因型比是3︰1︰3︰1
5.下表是关于4种生物的能源、C源、N源和代谢类型的描述,其中描述正确的一组是
( )
| 硝化细菌 | 乳酸菌 | 根瘤菌 | 衣藻 | |
| 能源 | 氧化NH3 | 分解乳酸 | 固定N2 | 利用光能 |
| C源 | CO2 | 糖类 | 糖类 | CO2 |
| N源 | NH3 | N2 | N2 | NO3- |
| 代谢类型 | 自养需氧型 | 异养厌氧型 | 异养需氧型 | 自养需氧型 |
A.硝化细菌、乳酸菌 B.乳酸菌、根瘤菌
C.根瘤菌、衣藻 D.硝化细菌、衣藻
6.已知NH4H和H2O反应时放出H2。下列说法不正确的是 ( )
A.该反应的化学方程式为:NH4H + H2O ==== H2 ↑+ NH3·H2O
B.H2既是氧化产物,又是还原产物
C.0.1molNH4H参加反应时,得到0.1mol电子
D.NH4H属于离子晶体,其晶体中含有离子键和共价键
7.下列离子方程式书写正确的是 ( )
A.铜溶于氯化铁浓溶液中:Cu+Fe3+=Cu2++Fe2+
B.向氯化铁溶液中加入过量氨水:3NH3·H2O+Fe3+===3NH4++Fe(OH)3↓
C.向碳酸钠溶液中加入过量的醋酸溶液:CO32-+2H+====H2O+CO2↑
D.向苯酚钠溶液中通入二氧化碳:
8.设NA表示阿伏加德罗常数,下列叙述正确的是 ( )
A.23gNO2和23gN2O4所含原子数目均为1.5NA
B.18gD2O所含电子数目为10NA
C.标准状况下,
D.
9.元素周期表中同周期的ⅡA族与ⅢA族元素的原子序数之差不可能为 ( )
A.1
B.
10.某有机化合物的结构简式:

推断它可以发生的反应类型有 ( )
①取代 ②加成 ③消去 ④水解 ⑤酯化 ⑥中和 ⑦加聚
A.①③⑤⑥ B.②④⑥⑦
C.①②④⑤⑥ D.①②③⑤⑥
11.现有0.1mol/L的醋酸溶液和0.1mol/L的氢氧化钾溶液,下列说法中正确的是( )
A.若混合后溶液恰好呈中性,则所需醋酸溶液的体积小于KOH溶液的体积
B.若混合后溶液呈酸性,则c(K+)>c(CH3COO-)
C.混合前醋酸溶液、氢氧化钾溶液中:c(H+)= c(OH-)
D.若两溶液等体积充分反应后,溶液中:c(K+)>c(CH3COO-)>c(OH-)>c(H+)
12.下列关于工业生产说法不正确的是 ( )
A.电解精炼铜时,用粗铜做阴极,纯铜做阳极
B.在硫酸工业和合成氨工业中,皆采用循环操作提高原料利用率
C.在氯碱工业中,电解槽被阳离子交换膜隔成阴极室和阳极室
D.在侯氏制碱工业中,向饱和氯化钠溶液中先通氨气,后通二氧化碳
13.可逆反应:3X(g)![]() 3Y(?)+Z(?)ΔH>0 ,随着温度的升高,气体物质的平均相对分子质量逐渐减小,则下列判断中正确的是
( )
3Y(?)+Z(?)ΔH>0 ,随着温度的升高,气体物质的平均相对分子质量逐渐减小,则下列判断中正确的是
( )
A.Y和Z可能都是固体 B.Y和Z一定都是气体
C.若Z是固体,则Y一定是气体 D.Y和Z不可能都是气体
二、选择题(本题包括8小题。每小题给出的四个选项中,有的只有一个选项正确,有的有多个选项正确,全部选对的得6分,选对但不全的得3分,不选或有选错的得0分。将正确答案的序号写在题后的括号内)
14.下列核反应中表示核聚变过程的是 ( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
15.下面关于光的说法中正确的是 ( )
A.红光光子的能量比紫光光子能量大
B.红光和紫光相遇能产生干涉现象
C.在真空中红光的波长比紫光的波长短
D.红光照射某金属时有电子向外发射,紫光照射该金属时一定也有电子向外发射
 16.如图所示,在光滑平面上以水平恒力F拉动小
16.如图所示,在光滑平面上以水平恒力F拉动小
车和木块,一起做无相对滑动的加速运动,若小车
质量为M,木块质量为m,加速度大小为a,木块
和小车间的动摩擦因数为μ。对于这个过程某同学
用了以下4个式子来表达木块受到的摩擦力的大小
正确的是 ( )
A.![]() B.μma C.μmg
D.Ma
B.μma C.μmg
D.Ma
17.根据分子动理论,当分子间距离为r0时分子所受的引力和斥力相等,以下说法正确的
是 ( )
A.分子间距离越大,分子所受引力和斥力越大,
B.分子间距离越小,分子所受引力和斥力越小
C.分子间距离是r0时分子具有最小势能,距离增大或减小时势能都变大
D.分子间距离是r0时分子具有最大势能,距离增大或减小时势能都变小
18.波源S从平衡位置开始向上运动,形成向左右两侧传播的横波,S、a、b、c、d、e和a’、
b’、c’是沿波传播方向上的间距为
A.质点c的加速度正在增大

| |
C.质点a的速度正在增大
D.质点c’已经振动了1.6s
19. 如图所示的图象能正确反映下面哪两个量的变化规律 ( )
 A.路端电压与外电阻,y表示路端电压,x表示外电阻
A.路端电压与外电阻,y表示路端电压,x表示外电阻
B.匀变速直线运动速度与时间,y表示速度,x表示时间
C.匀变速直线运动加速度与时间,y表示加速度,x表示
时间
D.做简谐运动物体,y表示回复力,x表示物体离开平衡
位置的位移
20.科学家在研究地月组成的系统时,从地球向月球发射激光,测得激光往返时间为t,若
还已知万有引力恒量为G,月球绕地球旋转(可看成匀速圆周运动)的周期为T,光速c(地球到月球的距离远大于它们的半径)。则可以求出 ( )
A.月球受到的引力 B.月球到地球的距离
C.地球的质量 D.月球的质量
21.如图所示,在光滑绝缘平面上有一正方形,其a、b、c三个顶点上分别放置等量的正点
电荷Q,将一电量为 q的正试探电荷分别放在正方形中心O点和正方形的另一个顶点
d处,则以下叙述正确的是 ( )
A.
 q在d点具有的加速度方向与在O点所具有的加速度方
q在d点具有的加速度方向与在O点所具有的加速度方
向相同
B. q在d点具有的加速度大小与在O点所具有的加速度大小相同
C.q在d点所具有的电势能等于其在O点所具有的电势能
D.q在d点所受的电场力大于其在O点所受的电场力
第Ⅰ卷选择题答题卡
| 题号 | 1 | 2 | 3 | 4 | 5 | 生 物 得 分 | |||
| 答案 | |||||||||
| 题号 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 化学 得分 |
| 答案 |
| ||||||||
| 题号 | 14 | 15 | 16 | 17 | 18 | 19 | 20 | 21 | 物理 得分 |
| 答案 |
| ||||||||
第Ⅱ卷
注意事项:
1.用钢笔或圆珠笔直接答在试题卷中。
2.本卷共10题,共174分。
 22.(18分)
22.(18分)
(1)图中给出的是用螺旋测微器测量一圆柱形工件的直径时
的示数,此读数应为 mm。
(2)某电压表的内阻在20~50kΩ之间,现要测量其内
阻,实验室备有下列器材:
A.待测电压表(量程3V); B.电流表(量程200μA);
C.电流表(量程5mA); D.滑动变阻器(最大电阻1kΩ);
E.电源(电动势4V); F.开关及导线若干。
①在所提供的电流表中,应选 (填写器材前面的字母代号)。
②为了尽量减小误差,要求多测几组数据,请在下面空白处画出符合要求的实验电路图。
23.(14分)“神舟”六号飞船自去年10月12日9时发射升空,历时5天5夜,于17日凌晨返回主着陆场。飞船在返回过程中,当返回舱下降到距地面大约

24.(20分)电子自静止开始经M、N板间(两板
间的电压为U)的电场加速后从A点垂直于
磁场边界射入宽度为d的匀强磁场中,电子
离开磁场时的位置P偏离入射方向的距离为
L,如图所示.求匀强磁场的磁感应强度(已知
电子的质量为m,电量为e)。
25.(20分)在建筑工地上,我们常常看到工人用重锤将柱桩打入地下的情景。对此,我们建立这样一个力学模型:重锤质量为m,从H高处自由下落,柱桩质量为M,重锤打击柱桩的时间短且不反弹,不计空气阻力,柱桩与地面间的平均阻力为f。利用这一模型,有位同学求出了重锤一次打击柱桩进入地面的深度:
设柱桩进入地面的深度为h,则对重锤开始下落到锤与柱桩一起静止这一全过程运用动能定理有:
![]()
得出 ![]()
(1)你认为该同学的解法是否正确?请说出你的理由。
(2)假设每一次重锤打击柱桩时的速度为一定值,要使每一次重锤打击后柱桩能更多地
进入地下,则重锤的质量与柱桩的质量应满足什么关系?
26.(13分)
“神州六号”的推进系统,用以推进必要的轨道修正和姿态控制。推进器中燃料是双氧水和一种液态氮氢化合物。已知氮氢化合物中氢元素的质量分数为12.5% ,相对分子质量为32,分子结构中只有单键。
(1)该氮氢化合物的结构式为 。
(2)若
物质,并放出75kJ的热量。则该燃烧反应的热化学方程式为 。
(3) “神州六号”上有固定的太阳帆板及小的氢氧燃料电池。氢氧燃料电池是用氢氧化
钾作电解质溶液,电池的总反应式是2H2 + O2 === 2H2O,则该电池在放电时:
负极的电极反应式为________________________________________,
正极的电极反应式为________________________________________。
27.(20分)常温下甲醛是一种无色、有特殊刺激性气味的气体,易溶于水,是世界卫生组织(WHO)确定的致癌物和致畸形物之一。我国规定:居室空气中甲醛的最高允许浓度为0.08mg/m3。
某研究性学习小组设计用如下方法测定某居室空气中甲醛的含量(假设空气中无其它还原性气体):
Ⅰ.测定原理: KMnO4(H+)溶液为强氧化剂,可氧化甲醛和草酸,其反应离子方程式为: 4MnO4—+ 5HCHO + 12H+ == 4Mn2+ + 5CO2↑+ 11H2O
2MnO4—+ 5H
 Ⅱ.测定装置:部分装置如下图所示(a、b为止水夹)
Ⅱ.测定装置:部分装置如下图所示(a、b为止水夹)
![]()
Ⅲ.实验步骤:
①检查装置气密性(气密性良好)。
②用A仪器准确移取25.00 mL 1.00×10-3mol·L—1的高锰酸钾溶液(过量)于广口瓶中并滴入3滴6mol·L—1H2SO4溶液备用。
③将2.00×10—3mol·L—1的草酸标准溶液置于A仪器中备用。
④打开a,关闭b,用注射器抽取100mL新装修的室内空气。关闭a,打开b,再缓缓推动注射器,将气体全部推入酸性高锰酸钾溶液中,使其充分反应。再如此重复4次(共5次)。
⑤将广口瓶中的溶液转入锥形瓶中(润洗广口瓶2~3次,并将洗涤液全部转入锥形瓶)。⑥用标准草酸溶液滴定锥形瓶中的溶液,记录滴定所消耗的草酸溶液体积。
⑦再重复实验2次。
Ⅳ.数据处理:分别于装修完工后的第1天、第7天、第30天(室内始终保持通风换气状况)对室内空气进行取样,通过实验测得以下三组数据(每次实验所取的KMnO4溶液均为 25.00mL):
| 装修后 第n天 | 草酸溶液(mL) | 甲醛的浓度 mg/m3 | |||
| 1 | 2 | 3 | 平均值 | ||
| 1 | 15.86 | 15.72 | 15.67 | 15.75 | |
| 7 | 26.17 | 26.36 | 26.38 | 26.27 | |
| 30 | 30.90 | 30.67 | 30.81 | 30.79 | |
请回答问题:
(1)A仪器名称是 ;
(2)步骤④如果压送气体时速度过快,可能会产生什么不利后果?
_________________________________________________________;
(3)步骤⑤如果没有润洗,所测甲醛的含量将 (填“偏高”、“偏低”、“无影响”);
(4)本实验是否需要指示剂?(如果需要,请写出指示剂的名称;如果不需要,试说明终点时的实验现象)。 。
(5)假设 KMnO4溶液的物质的量浓度为c1 mol·L—1,所取KMnO4溶液的体积为V1mL;
草酸溶液的物质的量浓度为c2 mol·L—1,消耗草酸溶液的平均体积为V2mL。
则:计算室内空气中甲醛浓度(mg/m3)的代数式为 ,第30天室内空气中甲醛浓度为_____________,并判断此时主人________(填“能”或“否”)入住。
 28.(15分)如图中每一方框中的字母代表一种反应物或生成物。已知A、B、C、D均为元素周期表中前三周期元素的单质,也是中学化学常见的物质。其中A、B为固体,且B是良好的半导体材料;C、D为气体。电解H的饱和溶液生成X、C和D,此反应是一个重要的工业生产反应。0.1mol·L—1Y溶液的pH=1 (图中物质间相互转化时水已略去)
28.(15分)如图中每一方框中的字母代表一种反应物或生成物。已知A、B、C、D均为元素周期表中前三周期元素的单质,也是中学化学常见的物质。其中A、B为固体,且B是良好的半导体材料;C、D为气体。电解H的饱和溶液生成X、C和D,此反应是一个重要的工业生产反应。0.1mol·L—1Y溶液的pH=1 (图中物质间相互转化时水已略去)
请填空:
(1)D的化学式为 ,Y溶液的名称是 。
(2)B单质为 晶体(填晶体类型)
(3)A和X溶液反应的离子方程式为 ________ ;
(4)
29.(12分)丙酸丙酯是一种香料,可以用下面的设计方案合成:
 |
(1) A的结构简式为 。
(2)写出下列反应的和的化学方程式:
①A——→C
②D+NaOH——→
(3)D有很多同分异构体,在含有羧基的同分异构体中,烃基上一氯取代物有2种的同
分异构体的结构简式是 。
30.(28分)请根据下列Ⅰ、Ⅱ、相关材料回答相关的问题:
Ⅰ.将水稻幼苗培养在不同氧气浓度的黑暗环境中,分别测得其无氧呼吸释放的二氧化碳量与有氧呼吸消耗的氧气量,获得如图所示结果。
(1)写出水稻无氧呼吸的反应式 。
(2)若水稻秧苗长时间被水淹没,易发生烂秧现象。请简要说明导致烂秧的原因:___
__ __ 。
(3)在图中添加水稻释放的二氧化碳总量曲线。

Ⅱ.某些动物和人存在着白化现象,他们的皮肤、毛发、眼睛中普遍缺乏黑色素。黑
色素是酪氨酸在酪氨酸酶催化下形成的。研究表明,白化个体体内不能合成黑色素并不是因为它们缺乏酪氨酸,而是体内不能合成酪氨酸酶。请据此情境回答:
(1)控制肤色、毛发正常的遗传信息储存在细胞的 中(要求答细胞结
构)。
(2)基因A与a的结构都由 和 两部分组成。基因A突变
为a则不能合成酪氨酸酶,基因A突变的具体部位是 。
(3) 请模拟中心法则描述形式写出肤色正常这一性状的表达过程:
。
(4) 酪氨酸酶的合成是受基因控制的,当基因型为aa时表现为白化,而基因型为Aa(杂
合子)的个体却表型正常。杂合体表现正常的原因是
。
31.(14分)完成下列Ⅰ、Ⅱ两小题。
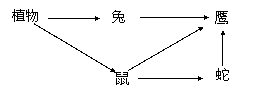
Ⅰ、下图为温带草原食物网部分图解
 |
请回答:
(1)鹰与蛇两个种群之间的关系为 。
(2)草原生态系统和森林生态系统相比恢复力稳定性较 。
(3)具测定,生产者在黑暗中每小时释放出44mg的CO2,而在光照充足的条件下,每小
时释放出32mg的O2,则生产者每小时实际产生的O2量为 mg。
(4)此为该草原生态系统的能量流动示意图
 |
能量流动的特点是 ,图中的A、B分别表示的含
义是 。
Ⅱ、某校生物兴趣小组想设计两个实验:
(一)探究尿液中是否含有葡萄糖; (二)证明血液中存在葡萄糖。
现提供:新取尿液样品、加有柠檬酸钠的鸡血、清水、试管、离心机、三脚架、大烧杯、
火柴、酒精灯、石棉网等。
回答:实验(二)比实验(一)复杂,其原因是______________________________
。
参考答案及评分标准
Ⅰ卷包括21小题,每小题6分,共126分。
一、选择题:选对的得6分,选错或未选的得0分
1.C 2.A 3.D 4.B 5.D
6.C 7.B 8.A 9.B 10.D 11.D 12.A 13.C
二、选择题:全部选对的得6分,选对但不全的得3分,不选或有选错的得0分
14.B 15.D 16.A 17.C 18.CD 19.B 20.BC 21.A
Ⅱ卷包括10小题,共174分。
22.本题共18分。
 (1)(4分)填
(1)(4分)填
(2)(14分)
①(4分)B
②(10分)电路如右图所示。
23.本题共14分。
假设第一次打开减速伞后飞船做匀减速直线运动,则
![]() m/s2=
m/s2=
由牛顿第二定律得: ![]() ②
②
则 ![]() ③
③
评分标准:①式5分,②式5分,③式4分,共14分。
24.本题共20分。
 电子在M、N间加速后获得的速度为v,由动
电子在M、N间加速后获得的速度为v,由动
能定理可得:
![]() mv2-0=eU ①
mv2-0=eU ①
电子进入磁场后做匀速圆周运动,设其圆周
运动的半径为r,则:
evB=m![]() ②
②
电子在磁场中的轨迹如图所示,由几何关系得:
 =
=![]() ③
③
由以上三式得: B=![]() ④
④
评分标准:①至④式每个式子5分,共20分.
25.本题共20分。
(1)不对。因为重锤与柱桩碰撞的过程中系统有动能的损失。
(2)设重锤每次打桩时的速度都为v1,碰撞后的共同速度为v2,则由动量守恒定律有
![]() ①
①
则碰撞后二者的共同动能为
![]() ②
②
当m>>M 时,碰撞后二者的动能趋于![]() ,即动能在碰撞中的损失趋向于零,而在柱桩打进地面的过程中,由功能关系又有
,即动能在碰撞中的损失趋向于零,而在柱桩打进地面的过程中,由功能关系又有
![]() ③
③
阻力f一定,Ek越大,柱桩进入地下的深度越深,所以要求m>>M。
评分标准:
(1)共7分 回答正确给3分,正确说明原因再给4分
(2)①式3分,②式3分,分析正确3分,③式2分,结论2分,共13分。
 26.(13分)
26.(13分)
(1) (3分)
(2)N2H4(l) + 2H2O2(l) == N2(g) + 4H2O(g) ⊿H= -1500kJmol-1 (4分)
(3)负极:2H2 + 4OH --4e-== 4H2O (3分) 正极:O2 + 2H2O + 4e-== 4OH - (3分)
27.(20分)
(1)酸式滴定管 (2分) (2)甲醛吸收不充分,影响测定结果 (3分)
(3)偏高 (3分) (4)不需要,加入最后一滴草酸溶液时溶液褪色且半分钟内不重新
变红(3分)
(5) (75clVl—
28.(每空3分,共15分)
(1)H2 ; 盐酸 (2)原子 (3)2Al+2OH-+2H2O= 2AlO2-+ 3H2↑ (4)14
29.(每空3分,共12分)
 (1)CH3CH2CHO
(1)CH3CH2CHO
(2)①CH3CH2CHO+H2 CH3CH2CH2OH

②CH3CH2COOCH2CH2CH3 + NaOH CH3CH2COONa + CH3CH2CH2OH
 (3)
(3)
30.(28分)
Ⅰ、(1)![]() (酒精)+
(酒精)+![]() +能量 (2分) 注:方程式若不
+能量 (2分) 注:方程式若不
完整(如缺酶),则不能给分。
(2)由于长期淹水,导致秧苗缺氧,进行无氧呼吸。长时间无氧呼吸积累的酒精,使组
织细胞酒精中毒,导致烂秧 (4分)注:答案必须明确说明烂秧的原因是酒精中毒,否则不给分。
(3)答案见图 (4分) 注:![]() 消耗总量与氧气消耗量的相交点应基本垂直于横坐标
消耗总量与氧气消耗量的相交点应基本垂直于横坐标
18%的位置(P点);曲线的起点不应低于纵坐标1的高度。其它不作过多要求,但不能画直线或上拱线。

Ⅱ、(1)细胞核(或染色体) (2分)
(2) 编码区 (2分) 非编码区 (2分) 编码区上游的非编码区(或RNA聚合
酶结合位点) (2分)
(3) ![]()
![]() (4分)
(4分)
(4) ①体细胞中基因成对存在;②只要有一个A(或显性基因)存在,便可控制合成酪氨
酸酶;③a基因不能控制合成酪氨酸酶 (6分)注:本题的核心答案是第②点,答出此点即可得满分。若仅答出第①③点,则不得分。注:答案未写出基因A、酪氨酸酶及表达性状一正常肤色,均不扣分。若仅写基因A,未写DNA,也不扣分。其它部分则不得缺少,若缺少,则不给分。若增加DNA复制,可不扣分。若增加逆转录或RNA复制,则不给分。
31.(14分)
Ⅰ、(1)竞争、捕食 (2分) (2)大 (2分) 64 (2分)
单向流动和逐级递减 (2分) 分解者 呼吸(或热能) (2分)
Ⅱ、血液呈红色,若直接用斐林试剂检测葡萄糖,则产生的砖红色沉淀与血液颜色相近。而尿液的颜色不会干扰显色反应 (4分)