九年级科学第一学期第一次月考试题
(第一、二章)
命题:章国刚
一、选择题(每题2分,共60分)
1.小煜同学所做的下列家庭小实验中,主要发生物理变化的是 ( )
 A.用蜡烛制取炭黑 B.自制汽水
C.用简易净水器净水 D.鸡蛋壳加入食醋中
A.用蜡烛制取炭黑 B.自制汽水
C.用简易净水器净水 D.鸡蛋壳加入食醋中
2、对人体中的葡萄糖的叙述正确的是( )
A、葡萄糖在人体中主要是作为提供能量的物质
B、葡萄糖是构成人体的组织的基本物质
C、葡萄糖在人体中主要是贮存能量的物质
D、以上说法都正确
3、下列关有机物化合物性质的叙述,错误的是( )
A、大多能溶于水 B、大多熔沸点低
C、大多易燃烧 D、大多不导电
4、当前,以下气体可以用固体氢氧化钠来干燥的是( )
A、H2和CO2 B、CO和O2
C、SO2和O2 D、H2和SO3
5.天然气、石油、煤等在地球上的蕴藏量是有限的,因此:(1)可利用电解水的方法得到氢气作能源;(2)可用酒精作能源;(3)砍伐树木作能源;(4)应开发太阳能、核能等新的能源.上述说法正确的是( )
A.只有(1) B.(1)、(2)和(4) C.(2)和(3) D.只有(4)
6.下列物质分别加入适量水中充分搅拌,不能得到溶液的是 ( )
A.小苏打 B.食盐 C.火碱 D.茶油
7.生活中的洗涤问题大都与化学知识有关。下列说法不正确的是( )
A.洗洁精可清洗餐具上的油污 B.汽油可洗掉衣服上的油渍
C.水可洗去铁栅栏上的铁锈 D.食醋可除去热水瓶中的水垢
8.福娃是2008奥运吉祥物。制作它的外部材料为纯羊毛绒,内充物为无毒的合成纤维,下列说法正确的是( )
A.制作福娃的内充物是引起白色污染的主要物质
B.纯羊毛和合成纤维可用燃烧法区别
C.制作福娃的外部材料属于有机合成材料
D.合成纤维的吸水性和透气性比纯羊毛好
|
|
C.H2+CuO====Cu+H2O D.CO+CuO=△=Cu+CO2
10.将酚酞试液滴人碳酸钠溶液中,发现溶液变成了红色。由此可得到的信息是( )
A.碳酸钠是一种碱 B.碳酸钠溶液呈碱性
C.碳酸钠是一种白色固体 D.碳酸钠的化学式为Na2CO3
11.下表记录了物质X的溶液分别加入到另外三种物质的溶液中产生的现象。则物质X的化学式可能是( )
|
| 氢氧化钠 | 碳酸钠 | 石蕊 |
| 物质X | 无明显现象 | 产生气泡 | 溶液变红 |
A.Ca(OH)2 B.CuSO4 C.HCl D.CO2
12、我国商代已经制造出精美的青铜器,春秋战国时期已会冶铁和炼钢,人类开发利用下列金属单质的时间顺序与金属活动性的强弱有着某种内在联系。由此推断,下列金属中,人类开发利用最晚的是:( )
A. Al B.Cu C.Fe D.Zn
13、下列物质在空气中放置一段时间后,质量增加的是( )
A、浓盐酸 B、纯碱 C、固体氢氧化钠 D、食盐
14、对下列物质:①纯碱 ②食盐水 ③石灰水 ④烧碱 ⑤液氧 ⑥小苏打,分类全部正确的是( )
A、碱—①④ B、纯净物—③④⑤ C、混合物—②⑤ D、盐—①⑥
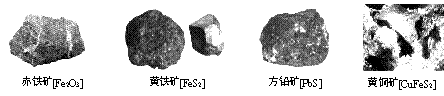 15、以下列矿石(括号内为各种矿石主要成分的化学式)为原料,通过高温冶炼制取金属,相对而言所产生的废气中,含污染空气并易造成酸雨危害的成分较少的是( )
15、以下列矿石(括号内为各种矿石主要成分的化学式)为原料,通过高温冶炼制取金属,相对而言所产生的废气中,含污染空气并易造成酸雨危害的成分较少的是( )
 A.
B.
C.
D.
A.
B.
C.
D.
16、要使右图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①锌和稀硫酸,②石灰石和盐酸,③氯化钠和水,④氧化钙和水
17、合成材料的应用和发展,大大方便了人类的生活。但是,合成材料废弃物的急剧增加也带来了环境问题,废弃塑料带来的“白色污染”尤其严重。为了解决“白色污染”,下列做法不合理的是 ( )
A、建议使用一些新型的、可降解的塑料,如微生物降解塑料和光降解塑料等
B、将已用过的塑料回收利用
C、将塑料集中起来焚烧
D、减少和重复使用某些塑料制品
A、①②③ B、①②④ C、②③④ D、①③④
18、国家决定推广乙醇汽油的应用,所谓乙醇汽油就是在汽油中加入适量乙醇混合而成的一种燃料,下列叙述错误的是( )
A、乙醇汽油是一种新型化合物
B、汽车使用乙醇汽油能减少有害气体的排放
C、用石油可以制得乙醇
D、用玉米、高梁发酵可以制得乙醇
19、厨房中有下列食物,其中含有丰富蛋白质的是( )
A、米饭 B、瘦肉 C、白菜 D、花生油
20、有关高分子的说法正确的是( )
A、高分子就式量超过100的分子 B、高分子就是塑料
C、高分子即聚合物 D、高分子的形状比较单一,仅有线型
21.某物质在纯氧气中充分燃烧后,只生成二氧化碳和水,该物质中( )
A.一定含有碳、氢两种元素 B.可能含有碳、氢两种元素
C.一定含有碳、氢、氧三种元素 D.可能含有碳、氢、氧三种元素
22、稀盐酸中混有少量硫酸,为了除去硫酸,可加入适量( )
A.铁屑 B.硝酸银溶液 C.氯化钡溶液 D.氢氧化钾溶液
23、只需用水就能直接鉴别的一组物质是( )
A.Na2SO4 、CuSO4 、CaSO4 B.AgCl 、BaSO4 、CuSO4
C.NaCl 、CaCl2、BaCl2 D.BaCl2 、AgCl 、CaCO3
24.下列各组物质中,能在同一溶液里大量共存的是( )
A.Na2SO4 Ba(OH)2 HCl B.CuSO4 H2SO4 Ca(OH)2
C.FeCl3 NaOH Ca(OH)2 D.K2SO4 NaOH NaCl
25.下列变化中,只有加入酸才能一步实现的是( )
A.Zn→ZnSO4 B.CaCO3 →CO2 C.Ba(NO3)2 →BaSO4 D.CuO →CuCl2
26、将一定量的镁条投入过量的稀盐酸中,表示反应过程中变化关系的曲线正确的是( )
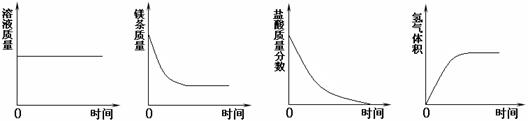 A
B
C
D
A
B
C
D
27.有FeSO4、CuSO4的混合溶液,向其中投入一些锌粉,完全反应后得到一些固体沉淀。过滤,向沉淀中加入少量稀硫酸有气泡产生。对上述固体沉淀有下列说法,其中正确的是( )
① 一定含有Zn ② 一定含有Fe ③ 一定含有Cu
④ 可能含有Zn ⑤ 可能含有Fe ⑥ 可能含有Cu
A.①②③ B.②③④ C.③④⑤ D.①②④
28、小韩知道蛋壳的制药成分是碳酸钙,决定送妈妈一个“无壳鸡蛋”。他从厨房中取来一格鸡蛋及一杯物质,将蛋泡在其中,则见蛋的表面冒出大量气泡,两天后就得到一格没有壳的蛋,她应取下列哪一种物质呢? ( )
A、高粱酒 B、醋 C、酱油 D、食盐水
29.下列关于“颜色”说法不正确的是( )
A 观摩小鱼尾鳍内血液流动现象的实验中看到的红细胞是淡黄色的
B FeCl3溶液中滴入NaOH溶液出现红褐色絮状沉淀
C 氧化铜和稀硫酸微热出现蓝色溶液
D CO2气体通入无色酚酞试液中出现红色
30.将下列两种溶液混合,再加入足量的酸,最终有沉淀生成是 ( )
A.碳酸钾和碳酸钙再加稀硝酸 B.氯化铜和氢氧化钡再加盐酸
C.硝酸银和氯化钠再加稀硝酸 D.硝酸钠再加硫酸
二、分析填空题(每空1分,共40分)
1.高分子的形状有___________、___________、____________三种
2. 当今世界上最重要的三大矿物燃料是 __ 、____________、__________,它们是重要的 ,其中 、 还是重要的化工原料.
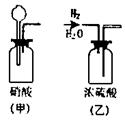
3、浓盐酸有挥发生性,瓶中会产生______,这是因为_______________________。
4、稀释浓硫酸时应把__________慢慢注入___________中,并不断用玻璃棒________,使产生的大量的________迅速散失
5. 完成下列化学方程式并配平。(每个方程式1分)
 (1)
(1)![]()
(2)![]()
(3)![]()
(4)![]()
(5)![]()
6、碳酸钙是_______、_______的主要成分,化学式为_______,可在高温下制得生石灰,化学方程式为__________________________________________。
7.特快电热壶由于快捷方便,被许多家庭、宾馆使用。请据图示回答:
(1)制作材料中属于金属或合金的是 (选填一种
物质编号,下同),属于有机物的是 ;
(2)制作手柄的塑料属于_________塑料,(填“热塑性”或“热固性”);
(3)用铜质材料制作电源插头的插脚是利用铜具有 __________性;
8.某溶液中含有Na+、H+、Cl-、SO42-四种离子,若滴加紫色石蕊试液,则显 色,欲证明两种阴离子确实存在,应先加适量的 溶液,使 完全沉淀过滤除去;再加入 溶液以确定 离子的存在.原溶液中最多可以有 种溶质.
 9.有A、B、C三种无色溶液,已知它们是盐酸、稀硫酸和碳酸钾溶液中的一种,为了鉴别它们进行如下实验
9.有A、B、C三种无色溶液,已知它们是盐酸、稀硫酸和碳酸钾溶液中的一种,为了鉴别它们进行如下实验
 由上述实验现象推断:A是
,B是
,C是
.
由上述实验现象推断:A是
,B是
,C是
.
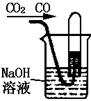 10.如下图所示,把盛满NaOH溶液的小试管倒立在盛有NaOH溶液的烧杯中,用导管往试管里缓缓通入混有少量CO2的一氧化碳气体.
10.如下图所示,把盛满NaOH溶液的小试管倒立在盛有NaOH溶液的烧杯中,用导管往试管里缓缓通入混有少量CO2的一氧化碳气体.
(1)试管内发生反应的化学方程式为 ,收集的气体是 .
(2)如果通入的气体是混有少量CO2、HCl的一氧化碳,则试管内发生反应的化学方程式为 ,收集的气体是 .
三、探究与计算题 (1-3每空1分,共10分,4题6分,5题4分)
1、维生素C俗称抗坏血酸,常用于防治坏血病造成的血管破裂出血。为了解维生素C的化学性质,我们将6片维生素C压碎,溶于l0毫升水,然后过滤,取几毫升滤液,做了下列几个实验:
(1)将滤液滴到蓝色石蕊试纸上试纸呈红色;再用pH试纸测得维生素C溶液的pH在l至2之间。说明维生素C具有_____________性;
 (2)在CuSO4溶液中加入滤液并加热煮沸,发现有红色的铜析出。从氧化还原的角度说明维生素C具有_____________性;
(2)在CuSO4溶液中加入滤液并加热煮沸,发现有红色的铜析出。从氧化还原的角度说明维生素C具有_____________性;
(3) 把滤液加热煮沸5秒至l0秒,再重复做上述2个实验,发现维生素C性质与未加热时的性质一样,即在100℃以下不会发生分解。这说明维生素C的性质比较 。
2、市售塑料袋有的是用聚乙烯 [ (CH2CH2)n ] 制成,有的是用聚氯乙烯 [ (CH2CHCl)n ] 制成,通过查阅资料可知:
(CH2CHCl)n+![]() O2 点燃===== 2nCO2+nH2O+nHCl
O2 点燃===== 2nCO2+nH2O+nHCl
其中n是上千或上万的数值;HCl气体极易溶于水,有刺鼻气味,其水溶液即是盐酸;鉴别盐酸的方法是加入AgNO3溶液,观察是否产生白色沉淀。
① 通过点燃的方法可以鉴别聚乙烯和聚氯乙烯。如果塑料袋点燃时有强烈的刺鼻气味,这种塑料袋可能是由 制成的。
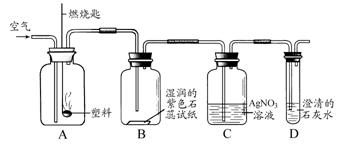
② 某同学设计了如下图所示实验来探究塑料燃烧的产物。
若A瓶燃烧的是聚氯乙烯塑料,在B瓶中可以看到的现象是
,C瓶中发出反应的化学方程式为
。若A瓶中用的是聚乙烯塑料,则在C瓶中能观察到的现象是 。
3、小明家里有一小袋粗盐,有一天他发现敞口放置的粗盐表面有溶解现象。经查阅资料得知,这种现象在化学上叫潮解,原因是粗盐中含有氯化钙和氯化镁。于是他设计了以下实验方案对粗盐进行提纯。 请回答实验中有关问题。
(1)将粗盐全部溶于水,加入过量的氢氧化钠溶液,其主要目的是除去粗盐中的 ;
(2)再加入过量碳酸钠溶液,目的是除去粗盐中的 ;
(3)待充分反应后过滤,所得滤液中的溶质为 ;
(4)向滤液中加入适量的稀盐酸,完全反应后,加热、蒸发、结晶,得到几乎不含其他杂质的NaCl晶体。
4、现有5.6克锌与100克稀硫酸恰好完全反应,
(1)、可生成氢气多少克?
(2)、稀硫酸的溶质质量分数为多少?
(3)、反应后所得溶液中溶质质量分数为多少?
5、实验室要配制500克10%的稀硫酸,求需要98%的浓硫酸多少克?水多少克?