高二化学阶段性测试
可能用到的原子量:H 1 C 12 N 14 O 16
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意。)
1.在相同条件下,等质量(颗粒大小相当 )的下列金属与足量的1mol/L盐酸反应时,速率最快的是
A.镁 B.铝 C.锌 D.铜
2.NO和CO都是大气污染物,主要来自于汽车尾气,为了消除对环境的污染,人们已能将它们相互反应生成N2和CO2,对此反应有关的叙述中不正确的是
A、增大压强能加快化学反应速率 B、使用适当催化剂可以加快化学反应速率
C、升高温度能加快化学反应速率 D、改变压强对化学反应速率没有影响
2. 已知反应A+3B![]() 2C+D在某段时间内以A的浓度变化表示的化学反应速率为1mol/(L·min)以C的浓度变化表示的化学应速率为:
2C+D在某段时间内以A的浓度变化表示的化学反应速率为1mol/(L·min)以C的浓度变化表示的化学应速率为:
A.0.5 mol/(L·min) B.1 mol/(L·min) C.2 mol/(L·min) D.3 mol/(L·min)3.一定温度下,可逆反应A(g) + B(g) ![]() C(g) + D(g)达到化学平衡状态的标志是
C(g) + D(g)达到化学平衡状态的标志是
A、C的生成速率与B的消耗速率相等
B、单位时间内生成a molC,同时生成a molD
C、反应混合物中A、B、C、D分子数目相等
D、反应混合物中A、B、C、D质量分数不再变化
4.下列反应,升高温度或减小压强,都能使平衡向正反应方向移动的是:
A.N2(气) + 3H2(气)![]() 2NH3(气)(正反应为放热反应)
2NH3(气)(正反应为放热反应)
B.H2O(气)+CO(气)![]() CO2(气)+H2(气)(正反应为吸热反应)
CO2(气)+H2(气)(正反应为吸热反应)
C.H2(气)+Br2(气)![]() 2HBr(气)(正反应为放热反应)
2HBr(气)(正反应为放热反应)
D.C(固)+ H2O(气)![]() CO(气)+H2(气)(正反应为吸热反应)
CO(气)+H2(气)(正反应为吸热反应)
5. 在2L的密闭容器中,发生3A(g)+B(g) ![]() 2C(g)的反应,若最初加入A和B都是4mol,测得10s内A的平均速率υ(A)=0.12 mol(L·s),则反应进行到10s时容器中B的物质的量是
2C(g)的反应,若最初加入A和B都是4mol,测得10s内A的平均速率υ(A)=0.12 mol(L·s),则反应进行到10s时容器中B的物质的量是
A.1.6mol B.2.8mol
C.3.2mol D.3.6mol
6.在一定条件下,合成氨达平衡时氨的体积分数为20%,若反应前后条件不变,则反应后缩小的气体的体积与原反应物体积的比:
A.1/4 B.1/6 C.1/3 D.1/2
7. 下列说法正确的是
A.合成氨反应中使用催化剂,使原来不能发生的反应变为可以发生的反应了。
B.对于可逆反应:CH3COOH ![]() CH3COO-+H+,增大压强对平衡几乎没有影响。
CH3COO-+H+,增大压强对平衡几乎没有影响。
C.对于任何达到平衡的可逆反应,改变某个条件,使得正反应速率增大,则平衡一定向正反应方向移动。
D.如果反应是放热的,则反应开始时就不需加热。
9.在温度和压强不变时有反应 2NO2![]() 2NO+O2,1LNO2高温分解,达到平衡时变为1.2L,这时NO2
2NO+O2,1LNO2高温分解,达到平衡时变为1.2L,这时NO2
的转化率为:
A.5% B.40% C.20% D.10%
10. 对于可逆反应2SO3(g) ![]() 2SO2(g)+O2(g)(正反应方向吸热)改变下列条件后,活化分子的百分数增加,同时平衡向正反应方向移动的有:
2SO2(g)+O2(g)(正反应方向吸热)改变下列条件后,活化分子的百分数增加,同时平衡向正反应方向移动的有:
A、增大压强 B、不断补充O2 C、使用合适的催化剂 D、升高温度
二、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个或两个选项符合题意)11.对于反应N2(气)+3H2(气) ![]() 2NH3(气)(正反应为放热反应);能使正反应速率增大的因素有
2NH3(气)(正反应为放热反应);能使正反应速率增大的因素有
A.增加N2或H2的浓度 B.保持容器的体积不变,通入稀有气体使压强增大
C.升高温度 D.减少NH3的浓度
12.可逆反应I2(g)+H2(g)![]() 2HI(g)在一定条件下已达到平衡状态。改变条件可能引起下列变化,这些变化能说明平衡一定向正反应方向移动的是
2HI(g)在一定条件下已达到平衡状态。改变条件可能引起下列变化,这些变化能说明平衡一定向正反应方向移动的是
①I2(g)浓度减小 ②混合气颜色变浅 ③I2(g)转化率增大 ④HI(g)百分含量增大
⑤I2(g)和H2(g)百分含量减少
A、①②③ B、②③④ C、③④⑤ D、①③⑤
13.可逆反应2A(气)+nB(固) ![]() 2C(气)+D(气)中,达平衡后,下列叙述正确的是
2C(气)+D(气)中,达平衡后,下列叙述正确的是
A.若增大压强,平衡不移动,说明n=1
B.若使用催化剂能加快反应的速率,但平衡向正反应方向移动.
C.若保持体积不变,升高温度,如A的浓度增大,说明正反应是放热反应.
D.若加入少量固体B,平衡不移动。
14.将固体溴化铵置于密闭容器中,在某温度下发生下列反应:
NH4Br(s)![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g)![]() H2(g)+Br2(g)两分钟后,反应达到化学平衡,测得氢气的浓度为0.5mol/L, HBr的浓度为4mol/L,则NH3的浓度为
H2(g)+Br2(g)两分钟后,反应达到化学平衡,测得氢气的浓度为0.5mol/L, HBr的浓度为4mol/L,则NH3的浓度为
A. 0.5mol/L B.2.5 mol/L C.2 mol/ L D.5 mol/ L
15.一定温度下,在一体积不变的密闭容器中,放入1摩A和2摩B,发生如下反应:
A(g)+B(g)![]() 2C(g)达平衡时,下列说法正确的是 :
2C(g)达平衡时,下列说法正确的是 :
A.平衡后混合气的密度比反应前增大 B.平衡时,混合气体的总物质的量比反应前减少
C.平衡后A和B的物质的量比小于1:2 D.平衡后体系的压强与反应前相等
16.某温度下,在固定容积的密闭容器中,可逆反应:A(气)+3B(气)![]() 2C(气)达到平衡,测得平衡时A、B、C物质的量之比为1:3:2,若保持温度不变,再充入A、B和C的混合气体(A、B、C的物质的量比为1:3:2),则下列判断正确的是
2C(气)达到平衡,测得平衡时A、B、C物质的量之比为1:3:2,若保持温度不变,再充入A、B和C的混合气体(A、B、C的物质的量比为1:3:2),则下列判断正确的是
A.平衡向正反应方向移动 B.平衡不会发生移动
C.C的的质量分数一定增大 D.C的质量分数一定不变
17.在450℃时,反应N2+3H2![]() 2NH3(正反应为放热反应)达到平衡,N2、 H2、NH3的浓度分别为1 mol/L、3 mol/L、3 mol/L,如保持温度不变,增大压强,使平衡时容器的总体积变为原来的1/2倍,则又达到平衡后的数据正确的是:
2NH3(正反应为放热反应)达到平衡,N2、 H2、NH3的浓度分别为1 mol/L、3 mol/L、3 mol/L,如保持温度不变,增大压强,使平衡时容器的总体积变为原来的1/2倍,则又达到平衡后的数据正确的是:
A.NH3的物质的量浓度不可能超过5mol/L B.N2的浓度在1 mol/L ~ 2mol/L 之间
C.H2的浓度可能超过6mol/L D.N2和H2的浓度比可能不再是1:3
18.在某一密闭容器中,充入一定量的HI气体,发生反应2HI(气) ![]() H2(气)+I2(气);(正反应为吸热反应),在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
H2(气)+I2(气);(正反应为吸热反应),在t1时达到平衡,t2时加热升温并保温,到t3时又达到新平衡,符合这一变化的图像是
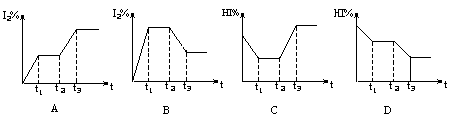 |
19. 1mol X气体跟a rnol Y气体在体积可变的密闭容器中发生如下反应:
X(g)+a Y(g)![]() b Z(g)
b Z(g)
反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
A a=1,b=1 B a=2,b=1 C a=2,b=2 D a=3,b=2
20.下列事实不能用勒沙特列原理解释的是
A.氢气和氮气合成氨的反应中,在加压下有利于氨的生成
B.啤酒瓶开启后,有气体逸出
C.I2(g)+H2(g)![]() 2HI(g)达到平衡加压后体系颜色加深
2HI(g)达到平衡加压后体系颜色加深
D.在含合成洗涤剂的双氧水中加入少量MnO2,产生泡沫的速率大
三 (本题包括3小题,共23分)
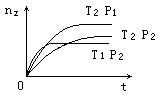 21. 如右图是反应2X(g)+Y(g)
21. 如右图是反应2X(g)+Y(g) ![]() 2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示,试比较下列关系(用“>、<、=”回答)
2Z(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nZ)与反应时间(t)的关系如图所示,试比较下列关系(用“>、<、=”回答)
P1 P2; T1 T2;正反应为_________反应(放热或吸热)
22. 一定条件下的可逆反应A(g)+B(g)![]() 2C(g),测得反应过程中某一时刻c(A)=0.6mol·L-1,c(B)=0.1 mol·L-1,c(C)=1.6 mol·L-1。若起始时A、B、C的浓度分别为a mol·L-1、b mol·L-1、c mol·L-1,平衡时A、B、C的浓度分别为a/ mol·L-1、b/ mol·L-1、c /mol·L-1,试回答:
2C(g),测得反应过程中某一时刻c(A)=0.6mol·L-1,c(B)=0.1 mol·L-1,c(C)=1.6 mol·L-1。若起始时A、B、C的浓度分别为a mol·L-1、b mol·L-1、c mol·L-1,平衡时A、B、C的浓度分别为a/ mol·L-1、b/ mol·L-1、c /mol·L-1,试回答:
(1)a、b应满足的条件是____________________;
(2)a的取值范围是_______________________;
(3)a/的取值范围是_______________________。
23.在一个固定体积的密闭容器中,加入2molA和1molB发生反应: 2A(g) + B(g) ![]() 3 C(g) + D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,用下列物质为起始反应物时,经反应达到平衡后C的浓度(用“>、<、=”回答)
3 C(g) + D(g)达到平衡时,C的浓度为Wmol/L,若维持容器体积和温度不变,用下列物质为起始反应物时,经反应达到平衡后C的浓度(用“>、<、=”回答)
(1)加入1molA和1molB时,C的平衡浓度________Wmol/L
(2)加入1molA和1molB和3molC和1molD ,C的平衡浓度________Wmol/L
(3)加入3molC和1molD, C的平衡浓度________Wmol/L
(4) 加入2molB和3molC和1molD, C的平衡浓度________Wmol/L
四、计算(27分)
24.把0.1molMnO2粉末加入50mL过氧化氢的溶液里(密度为1.1g·mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示。
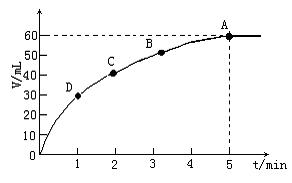
(1)实验时放出气体的总体积是___________________________
(2)放出一半气体所需的时间约为___________________________
(3)A、B、C、D各点反应速率由快到慢的顺序是___________________________
(4)计算初始过氧化氢溶液的质量分数及初始物质的量浓度
25.把氮气和氢气以1:1的物质的量比混匀后分成四等份,分别同时充入A、B、C、D四个装有催化剂的真空容器中(容器的容积固定),在保持相同温度的条件下,四个容器中的合成氨反应相继达到化学平衡状态。分析表中实验数据后通过计算回答问题。
| 容器代号 | A | B | C | D |
| 平衡时混合物的平均相对分子质量 | 16 | 17 | ||
| 平衡时N2的转化率 | 20% | |||
| 平衡时H2的转化率 | 30% |
⑴通过计算填好表比较A、B、C、D中氮气转化率大小
⑵达到平衡时所需时间最长的容器是 。
⑶四个容器容积由小到大的排列次序是 。
高二化学阶段性测试答案
可能用到的原子量:H 1 C 12 N 14 O 16
一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意。)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| A | D | C | D | D | C | B | B | B | D |
二、选择题(本题包括10小题,每小题3分,共30分。每小题只有一个或两个选项符合题意)
| 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| AC | C | CD | D | CD | AC | B | AD | AD | CD |
三 (本题包括3小题,共23分)
21.P1 > P2; T1 > T2;正反应为___放热反应(放热或吸热)
22.试回答:
(1)a、b应满足的条件是_ a-b=0.5;
(2)a的取值范围是____________0. 5≤a≤1. 4___________;
(3)a/的取值范围是_______________0. 5<a<1. 4________。
23. (1)加入1molA和1molB时,C的平衡浓度____<____Wmol/L
(2)加入1molA和1molB和3molC和1molD ,C的平衡浓度___>_____Wmol/L
(3)加入3molC和1molD, C的平衡浓度___=_Wmol/L
(4) 加入2molB和3molC和1molD, C的平衡浓度___>_Wmol/L
四、计算(27分)
24. (10分)
60mL 1min 2min D>C>B>A
0.11mol/L 0.08%
25. (17分)
| 容器代号 | A | B | C | D |
| 平衡时混合物的平均相对分子质量 | 18.75 | 16.67 | 16 | 17 |
| 平衡时N2的转化率 | 20% | 10% | 6.25% | 12% |
| 平衡时H2的转化率 | 60% | 30% | 18.81% | 36% |
⑴通过计算填好表比较A、B、C、D中氮气转化率大小
A>D>B>C.
⑵达到平衡时所需时间最长的容器是 C 。
⑶四个容器容积由小到大的排列次序是 A<D<B<C。(2,3不需过程)